Diagnostisk
träffsäkerhet vid
biopsering av
prostatacancer
HUVUDOMRÅDE: Radiografi
FÖRFATTARE: Nina Andréasson & Clara Eriksson HANDLEDARE:Anna Bjällmark
EXAMINATOR: Britt-Marie Ahlander JÖNKÖPING: 2020 Juni
Sammanfattning
Prostatacancer är den vanligaste cancerformen hos män. Prostatan tillhör de manliga reproduktionsorganen och producerar bland annat prostataspecifikt antigen (PSA) som kan påvisas i blodet. Förhöjda värden av PSA kan bero på prostatacancer. Transrektalt ultraljuds (TRULS)-ledda systematiska biopsier används i högre frekvens än magnetkamera med riktad biopsi. Röntgensjuksköterskans möte med dessa patienter är före, under och efter bildtagningen med magnetkameran. Syftet var att göra en översikt av den diagnostiska träffsäkerheten för TRULS-ledda systematiska biopsier och magnetresonans (MR)-undersökning med riktade biopsier vid misstanke om prostatacancer. Metoden bestod av en litteraturöversikt med systematisk ansats. Inkluderingskriterier var vetenskapliga artiklar skrivna mellan 2015–2020. Artiklarna skulle vara peer-reviewed och etiskt granskade. Databasen Medline användes till sökningen. Kvalitetsgranskning gjordes med granskningsprotokoll hämtade från Avdelningen för omvårdnad på Hälsohögskolan. I resultatet inkluderades 15 artiklar som visade att skillnaden i den diagnostiska träffsäkerheten för prostatacancer hos män inte var stor mellan metoderna. Däremot hittade MR-undersökning med riktade biopsier större andel kliniskt signifikanta cancrar och mindre del insignifikanta cancrar än vad TRULS-ledda systematiska biopsier gjorde. MR-undersökning med riktad biopsi är en bra metod för att öka träffsäkerheten att hitta kliniskt signifikant cancer. Dock går det inte utesluta TRULS-ledda systematiska biopsier då kontraindikationer och missade cancrar på MR-undersökning med riktade biopsier förkommer.
Nyckelord: PSA, magnetresonans, transrektalt ultraljud, klinisk signifikans, klinisk insignifikans.
Summary
Prostate cancer is the most common cancer in men. The prostate belongs to the male reproductive organs and produces, among other things, prostate-specific antigen (PSA) that can be detected in the blood. Elevated levels of PSA may be due to prostate cancer. Transrectally ultrasound (TRULS)-guided systemic biopsies are used at higher frequency than magnetic cameras with directed biopsy. The X-ray nurse's meeting with these patients is before, during and after the imaging with the magnetic camera. The aim was to make an overview of the diagnostic accuracy of TRULS guided systematic biopsies and MRI with targeted biopsies on suspicion of prostate cancer. The method consisted of a literature review with systematic approach. Inclusion criteria were scientific articles written between 2015-2020. The articles would be peer-reviewed and ethically approved. The Medline database was used for the search. Quality review was done with review protocols obtained from the Department of Nursing at the School of Health. The result included 15 articles showing that there was no big difference in the diagnostic accuracy of prostate cancer in men between the methods. In contrast, MRI with targeted biopsies found a greater proportion of clinically significant cancers and a smaller proportion of insignificant cancers than TRULS guided systematic biopsies did. MRI with targeted biopsy is a good method for increasing the accuracy of finding clinically significant cancer. However, TRULS guided systematic biopsies cannot be ruled out as contraindications and missed cancers on MRI with targeted biopsies occur.
Keywords: PSA, magnetic resonance, transrectal ultrasound, clinically significans, clinically insignificans.
Innehållsförteckning
1 Inledning... 1
2 Bakgrund ... 1
2:1 Anatomi och fysiologi ... 1
2:2 Patofysiologi ... 1
2:3 Undersökningsmetoder ... 2
2:3:1 PSA... 2
2:3:2 Transrektal ultraljudsledda systematiska biopsier ... 2
2:3:3 Magnetresonanstomografi med riktade biopsier ... 3
2:3:4 Gleasonsumma ... 5
2:4 Nationella prostataregistret ... 6
2:5 Röntgensjuksköterskans roll ... 7
2:6 Problemformulering ... 7
3 Syfte ... 9
4 Material och metod ... 10
4:1 Urval ...10 4:2 Datainsamling ...10 4:3 Analys ...11 4:4 Etiska överväganden ...12
5 Resultat ... 13
5:1 Upptäckten av prostatacancer ...145:2 Prevalens av insignifikant och signifikant cancer. ...15
6 Diskussion ... 17
6:1 Metoddiskussion ...17
6:2 Resultatdiskussion...20
6:3 Komplikationer av biopsier ...23
6:4 Förslag på vidare forskning ...23
7 Slutsatser ... 25
Referenser ... 26
Bilagor ... 32
Bilaga 1-Granskningsprotokoll ...32
1
1 Inledning
Prostatacancer är den vanligaste cancerformen i Sverige och cirka 10 000 män diagnostiseras varje år. Tumörsjukdomen drabbar oftast män över 50 år och genomsnittsåldern för män med prostatacancer är 70 år. Vilka orsakerna är till cancern är inte klarlagt men 5% anses vara ärftliga (Regionala cancercentrum [RCC], 2018). För att kunna konstatera prostatacancer palperas prostatan och sedan tas ett PSA-prov. Visar det förhöjda värden leder det till vidare utredning där biopsi kan bli aktuellt. Det finns flera biopsimetoder som kan påvisa cancer där de två vanligaste är transrektalt ultraljudsledd biopsi (TRULS) och magnetkameraundersökning (MR)-undersökning med riktade biopsier. Under gruppens verksamhetsförlagda utbildning uppstod ett intresse för ämnet och vilken metod som är mest tillförlitlig när det gäller att diagnostisera cancer i prostatan.
2 Bakgrund
2:1 Anatomi och fysiologi
Prostatan är en körtel som tillhör de manliga reproduktionsorganen. Den är belägen under urinblåsan och omger den övre delen av urinröret. Storleken på prostatan ökar under en livstid. I yngre år är den stor som en golfboll och har formen av en valnöt (Tortora & Derricksson, 2015). Körteln är indelad i tre olika zoner. Den största delen kallas perifiera zonen och utgör den bakre delen som gränsar mot rectum. Transitionszonen är den delen som omsluter urinröret, där det har sitt inträde i prostatan. Bakom transitionszonen, i den övre delen av prostatan ligger den centrala zonen. Den omger höger och vänster ejakulationskanal (American college of radiology [ACR], 2015). Prostatan tillverkar ett sekret som är en mjölkig, sur vätska med ett pH-värde omkring 6,5. Sekretet innehåller citronsyra, vilket används av sperman till adenosintrifosfatproduktion (ATP) via Krebs cycle. 25 % av sperman utgörs av sekret från prostatan. Sekretet innehåller även fosfater och flera proteindirigerande enzymer, till exempel prostataspecifika antigen (PSA) som kan påvisas i blodet (Tortora & Derricksson, 2015).
2:2 Patofysiologi
En förändring i prostatan kan bero på adenom, en godartad tumör, eller karcinom, en elakartad tumör. I den perifera zonen, största delen av prostatan, har 70–80% av all prostatacancer sitt ursprung. Ungefär 20% av all cancer börjar i transitionszonen och i den centrala zonen är det
2
endast en liten del som har sitt ursprung (ACR, 2015). I ett tidigt stadie är sjukdomen symtomfri och efter de första cellförändringarna kan det ta lång tid innan sjukdomen utvecklas till cancer. Om ett förhöjt PSA-värde påvisas i blodet kan cancern upptäckas i ett tidigt stadium. Anledningen till ett stigande PSA-värde är att prostatavävnad bryts ner och PSA läcker ut i blodet. Det förhöjda PSA-värdet behöver inte bero på cancer, utan kan även bero på en godartad prostatahyperplasi. Även vid inflammation i prostatan kan PSA-värdet stiga. Vid en malignitet i prostatan kan tumören upplevas som en förhårdnad. Denna upptäcks genom en ändtarmsundersökning då läkaren palperar prostatan. De första symtomen kan uppstå när spridning av sjukdomen skett vilket vanligtvis visar sig som ryggsmärtor, viktminskning, anemi, blod i urinen och onormal trötthet. Metastaseringen är ofta lokaliserad till skelettet och kan leda till patologiska frakturer (Almås et al., 2011).
2:3 Undersökningsmetoder 2:3:1 PSA
Ett första steg att diagnostisera prostatacancer är att ta ett blodprov för att mäta PSA-värdet. Detta värde ökar något med åldern men framförallt vid sjukdomar i prostatan. En liten förhöjning tyder ofta på en inflammation i prostatan, snarare än cancer. Ett PSA-värde över 3 µg/l för män över 65 år ska enligt rekommendationer utredas för prostatacancer (RCC, 2018). Prostatan palperas och undersöks efter malignitet. Vidare tas nya PSA-värden med några månaders mellanrum. Om de fortsätter att stiga rekommenderas TRULS-ledda systematiska biopsier eller MR-undersökning med riktade biopsier för att påvisa malignitet i prostatan (RCC, 218). Hos män med prostatacancer finns det ett starkt samband mellan PSA-värdet och storleken på prostatan. PSA-värdet dividerat med prostatavolymen i kubikcentimeter ger ett värde för PSA-densiteten. För att uppskatta storleken på prostatan krävs det en ultraljuds- eller MR-undersökning. PSA-densitet under 0,1 µg/l/cm³ talar starkt för att det är en godartad prostataförstoring, medan en PSA-densitet över 0,2 µg/l/cm³ ger en misstanke om prostatacancer (RCC, 2018).
2:3:2 Transrektal ultraljudsledda systematiska biopsier
TRULS-ledd systematisk biopsi bygger på ultraljudsdiagnostik. För att framställa bilder med ultraljud används ljudvågor. Korta ljudpulser sänds in i kroppen och bildar mekaniska vibrationer. För att ljudvågen ska breda ut sig krävs ett medium. Partiklarna i mediet rör sig parallellt med vågens utbredning fram och tillbaka. När en puls skickas ut från ultraljudsgivaren
3
och den träffar en gränsyta reflekteras en del tillbaka mot ultraljudsgivaren. Mottagaren omvandlar tryckvariationerna till elektriska signaler, vilka kan studeras på en bildskärm. Genom att mäta de olika ekona som kommer tillbaka kan djupet mätas och flera olika gränsytor bestämmas (Berglund & Jönsson, 2007).
Prostatans volym kan fastställas med hjälp av transrektalt ultraljud. Dessa mått kan användas till att uppskatta körtelns vikt men även fokala förändringar som hyper- eller hypoekogena partier kan ses i prostatan med metoden. Förmågan att skilja mellan benign hyperplasi och malign tumör är dock begränsad. Ultraljudets största roll är att fungera som guide vid transrektal prostatabiopsi. En ultraljudsstav förs då in i rektum som genom rektalväggen avbildar prostata. Staven är bara ett par centimeter i diameter och i den finns en kanal för biopsinålen. Med hjälp av ultraljudet lokaliseras prostatan och biopsinålen skjuts sedan ut för att ta ett vävnadsprov. Vid biopsin görs ett flertal systematiska biopsier i anatomiskt bestämda områden och i områden som ser misstänkta ut på ultraljudet. För att täcka in alla områden av prostatan tas tio till tolv biopsier vid samma tillfälle. Undersökningen sker i realtid och biopsinålens läge kan lokaliseras med ultraljudet (Aspelin & Pettersson, 2008).
2:3:3 Magnetresonanstomografi med riktade biopsier
MR-kameran består av en magnet, ett sändar- och mottagarsystem för radiofrekventa (RF) pulser, ett gradientsystem och ett datorsystem. Magneten är extremt kraftig och styrkan mäts i enheten Tesla (T). I dagens MR-kameror har magneten oftast en fältstyrka på antingen 1,5 T eller 3 T. Kroppen består till stor del av vatten och väte är därför den vanligaste atomen. Detta gör väteatomen till en utmärkt informationskälla för MR. Vätekärnan består av en enkel proton som har en egenskap kallad spinn, vilket betyder att den roterar runt sin egen axel. Denna rotation ger upphov till ett magnetiskt fält. När kroppens vätekärnor påverkas av ett starkt magnetfält, som en MR-kamera, kommer vätekärnornas samlade magnetisering, på grund av deras magnetiska moment, att peka i fältets riktning. En kort puls av radiovågor skickas in och denna tas upp av vätekärnorna som då börjar rotera i takt med radiovågens frekvens. Kärnorna exciterar energi och under det att vätekärnorna återgår till sitt ursprungliga tillstånd avger de en signal som kan avläsas med hjälp av en mottagare. Upprepade pulser skickas in och flera mätningar av signalen görs. Förutbestämda sekvenser framtagna för prostatadiagnostik avgör hur radiofrekvenserna ska skickas in och avläsas. Med hjälp av en matematisk beräkning kallad fouriertransformen kan rådata från mätningarna omvandlas till en bild synlig för människan i
4
datorn. Olika sekvenser ger olika information om vävnader i kroppen (Berglund & Jönsson, 2007).
När MR-bildtagning används som diagnostiseringsmetod kan zonerna i körteln avbildas tydligt och urskilja frisk och sjuk vävnad. Det gör att magnetkameran kan detektera betydande prostatacancer i någon zon. Vid en prostataundersökning med MR används antingen en endorektal spole eller en abdominell ytspole (Aspelin & Pettersson, 2008). En magnetstyrka på 3 T eller 1,5 T rekommenderas för undersökningen och standardiserade protokoll ska användas. I dessa protokoll ingår T2-viktade bilder och diffusionsviktade (DWI) sekvenser med ADC-karta, ett biparametriskt protokoll. Eventuellt kan tillägg göras med dynamisk kontrastförstärkning, ett multiparametriskt protokoll (RCC, 2018). Efter att patienten har genomgått en MR-undersökning av prostatan, tittar en radiolog på bilderna och skattar området med hjälp av Prostate Imaging- Reporting and Data System (PI-RADS). PI-RADS är ett internationellt verktyg som radiologer använder för att bedöma sannolikheten att fyndet vid en MR-bild är cancer. Bedömningen sker med hjälp av en skala på 1–5 som baseras på en kombination av bilderna och korrelerar med sannolikheten av klinisk signifikant cancer i prostatan (RCC, 2018).
PI-RADS 1 – Mycket låg (mycket osannolikt att kliniskt signifikant tumör föreligger). PI-RADS 2 – Låg (osannolikt att kliniskt signifikant tumör föreligger).
PI-RADS 3 – Intermediär (osäkert att kliniskt signifikant tumör föreligger). PI-RADS 4 – Hög (sannolikt att kliniskt signifikant tumör föreligger).
PI-RADS 5 – Mycket hög (mycket sannolikt att kliniskt signifikant tumör föreligger).
Användningen av PI-RADS baseras endast på bilderna, andra bedömningsinstrument som PSA och klinisk bedömning ska inte påverka. Vid PI-RADS 4–5 och ibland även 3 bör biopsi övervägas men inte för PI-RADS 1 och 2 (ACR, 2015). För de patienter där misstänkta områden har setts på bilderna görs riktade biopsier. Den riktade biopsin kan göras när patienten ligger i MR-kameran (in-bore). Denna metod är väldigt tidskrävande och inte så vanlig. Vanligast är att biopsin görs vid ett senare tillfälle med ultraljudsvägledning. MR-bilden överlagrar då ultraljudsbilden i realtid och på så sätt blir det tydligt var områdena som ska biopseras finns. Detta kan ske med hjälp av en datorbaserad programvara vilket kallas fusion, eller utan att använda programvara, visuell registrering (Drost et al., 2019).
5 2:3:4 Gleasonsumma
Vävnadsprov som tagits från biopsierna skickas för analys till patologen som sedan använder gleasongrader för att bedöma primärtumören vid prostatacancer (RCC, 2018). Denna gradering är mellan 3–5 och identifierar olika grundmönster som framgår av vävnadsprovet. En cancer med gleasongrad 3 liknar prostatavävnad och växer väldigt långsamt och sprider sig inte. Gleasongrad 4 växer från år till år och kan sprida sig till andra organ medan gleasongrad 5 växer från månad till månad och kan sprida sig väldigt snabbt. Prostatacancer har ofta olika gleasongrad i olika delar. Därför lägger patologen ihop den mest utbredda graden cancer med den mest aggressiva graden. Den mest aggressiva graden ska alltid ingå i gleason-summan oavsett mängd. Exempel: Den mest utbredda graden blir gleason 3 + den mest aggressiva graden blir gleason 4 = dessa värden tillsammans blir gleason 7. Lågriskcancer definieras som gleason ≤6 och mellan-/högriskcancer definieras som gleason ≥7 (figur 1). När en behandlingsmetod ska väljas vägs också förväntad kvarvarande livstid in för patienten. Detta tillsammans med patientens egna önskemål avgör hur behandlingen ska se ut. Generellt sett så sätts ingen behandling in för en lågriskcancer, gleason ≤6, eftersom denna cancer sällan sprider sig eller växer. I nuläget finns inga rekommendationer för hur en sådan cancer ska följas upp. En mellan/högriskcancer är generellt sett aktuell för behandling, då den anses vara aggressiv eller benägen att sprida sig (RCC, 2018).
6
Figur 1 Flödesschema över tillvägagångssätt vid biopsering.
2:4 Nationella prostataregistret
Nationella prostataregistret (NPCR) är ett hjälpmedel som används för dokumentation och kvalitetssäkring kring vården av män med prostatacancer. Syftet med NPCR är att främja god vård för alla män, vilket görs med jämförelse av resultat bland vårdenheter som behandlar män med prostatacancer. Behandlingen ska ske i diskussion mellan patient och vårdhavare samt syftar till bästa tumörkontroll och minsta möjliga biverkningar. Innehållet i dokumentationen ska innefatta hur diagnos ställs, utbredning och typ av prostatacancer, väntetider, behandling och behandlingsresultat. För att öka kunskapen om prostatacancer och förbättra behandlingar används även registret för forskning (Nationella prostatacancerregistret [NPCR], u.å).
Varje år tar NPCR fram en nationell kvalitetsrapport utifrån det dokumenterade materialet i registret. I den senaste rapporten från 2018 kan bland annat metod för diagnostisering av prostatacancer utläsas. Utvecklingen av MR som diagnostiseringsmetod har gått snabbt och andelen män som diagnostiseras med prostatacancer av MR med riktade biopsier har ökat. Under 2018 var det 15% med stor spridning i landet: Stockholm 40%, Värmland 0%, Jönköping 9%, Halland 23% och Kronoberg 16%. Under samma år hade 36% av de män som gjort
MR-bildtagning Misstänkta områden- riktade biopsier görs Inga misstänkta områden- inga biopsier görs Vävnadsprov graderas enligt Gleasonsumma TRULS-ledda systematiska biopsier Vävnadsprov graderas enligt Gleasonsumma Signifikant cancer ≥7 Insignifikant cancer ≤6 Insignifikant cancer ≤6 Signifikant cancer ≥7
7
TRULS-ledda systematiska biopsier utretts vidare med en MR-undersökning, även detta med stor spridning: Stockholm 64 %, Värmland 4%, Jönköping 13%, Halland 43% och Kronoberg 24 % (NPCR, 2018).
2:5 Röntgensjuksköterskans roll
Röntgensjuksköterskans huvudområde är radiografi, vilket är ett tvärvetenskapligt kunskapsområde där medicin, omvårdnad, bildtagning och strålningsfysik ingår. En röntgensjuksköterska ska hantera dessa områden och relationen mellan dem (Svensk förening för röntgensjuksköterskor, 2011). Denna litteraturstudie innefattar omvårdnad och bildtagning vid MR innan riktade biopsier. Ultraljud ingår i röntgensjuksköterskans arbete med omvårdnad och diverse förberedelser, men TRULS-ledda systematiska biopsier utförs av urologer och görs inte på röntgenavdelning. Mötet med människor i alla åldrar och sjukdomstillstånd är grunden i arbetet. Röntgensjuksköterskan ansvarar för och genomför bildtagningen på MR vilket gör att mötet med dessa patienter är före, under och efter undersökningen. Patienter med misstänkt prostatacancer är ofta oroliga inför undersökningen. Oro och ångest kan bero på klaustrofobi, långa undersökningstider, högt ljud under undersökningen eller för beskedet som väntar efter (Allisy-Roberts & Williams, 2008). Det gör att bemötande och information är viktigt för att patienten ska känna sig delaktig och trygg vid undersökningen. Undersökningen ska göras utifrån patientens behov och förutsättningar. En viktig del av arbetet är att planera utförandet av undersökningen, för att skapa bilder med hög kvalitet som underlättar diagnostiken. Vid en MR-undersökning är det viktigt med patientsäkerheten på grund av det starka magnetfältet då allt magnetiskt attraheras. Det varierande magnetfältet inducerar ström i kablar och RF-pulsen orsakar uppvärmning av patienten. Röntgensjuksköterskan är ansvarig för att säkerheten följs och att rätt protokoll och sekvenser används för att diagnos ska kunna ställas (Allisy-Roberts & Williams, 2008).
2:6 Problemformulering
I rollen som röntgensjuksköterska ingår det att hålla sig uppdaterad kring aktuell forskning och bilddiagnostik är ett område som ständigt utvecklas. Prostatacancer är den vanligaste cancerformen i Sverige och är ett aktuellt forskningsområde. De senaste åren har det hänt mycket inom forskning på prostatacancer och framförallt inom diagnostiken. Enligt de nationella rekommendationerna bör alla män med malignitetsmisstänkta palpationsfynd eller förhöjda PSA-värden över åtgärdsgränsen erbjudas utredning. Denna ska innefatta TRULS eller
8
en MR-undersökning som står till grund för om det blir systematiska eller riktade biopsier (RCC, 2018). Användningen av metoderna är spridda i landet, där ett övervägande antal regioner i första hand använder sig av TRULS-ledda systematiska biopsier för att ställa diagnos (NPCR, 2018). En tidigare studie av Tangel och Rastinehad (2018) skriver att MR som metod för diagnostisering av prostatacancer utmanar gamla tillvägagångsätt. Författarna menar på att TRULS-ledda biopsier ofta ger ett missvisande resultat eftersom metoden har begränsad sensitivitet och specificitet (Tangel & Rastinehad, 2018). Enligt den yrkesetiska koden för röntgensjuksköterskor (2008) ska röntgensjuksköterskan ta ansvar för utvecklingen av kunskapsområdet utifrån erfarenhet och evidens. Genom att undersöka om den diagnostiska träffsäkerheten skiljer sig mellan TRULS-ledda systematiska biopsier och MR-undersökning med riktade biopsier ökas kunskapsläget för röntgensjuksköterskor.
9
3 Syfte
Syftet var att göra en översikt av den diagnostiska träffsäkerheten för TRULS-ledda systematiska biopsier och MR-undersökning med riktade biopsier vid misstanke om prostatacancer.
10
4 Material och metod
För att kunna svara på syftet gjordes en litteraturstudie med systematisk ansats. Enligt Forsberg och Wengström (2016) beskrivs en litteraturstudie som ett sätt att söka, kritiskt granska och sammanställa litteratur inom ett specifikt område. Metoden syftadetill att uppnå en syntes av data från tidigare genomförda empiriska studier inom prostatabiopsier. Studien utfördes på Jönköping University - School of Health and Welfare.
4:1 Urval
Urvalet av litteratur bestod av kvantitativa artiklar där empiriska studier har gjorts. Studierna skulle innefatta detektionsgraden av malignitet i prostatan för de två olika biopsimetoderna, där upptäckten av signifikant och insignifikant cancer redovisades. Sökningarna av vetenskapliga artiklar gjordes i databasen Medline, där sökorden definierades efter syftet. Inklusionskriterier för sökningen innefattade engelskspråkiga artiklar som var publicerade mellan 2015–2020. Endast artiklar från de senaste fem åren inkluderades för att få med den senaste forskningen inom prostatacancerdiagnostik. Artiklarna skulle vara peer-reviewed och vara publicerade med en vetenskaplig struktur enligt rapportmodellen Introduktion Metod Resultat och (and) Diskussion (IMRAD). Exklusionskriterier för artiklarna var ej etiskt granskade och äldre än fem år. Artiklarna fick heller inte vara en review-artikel, utan skulle vara en originalartikel. Tillsammans började gruppen med att läsa rubrikerna på de artiklar som framkom efter sökningarna. På de artiklar där rubriken stämde överens med syftet, lästes sammanfattningen (abstract). Om artikeln var relevant för syftet, sparades en fulltextkopia för vidare granskning.
4:2 Datainsamling
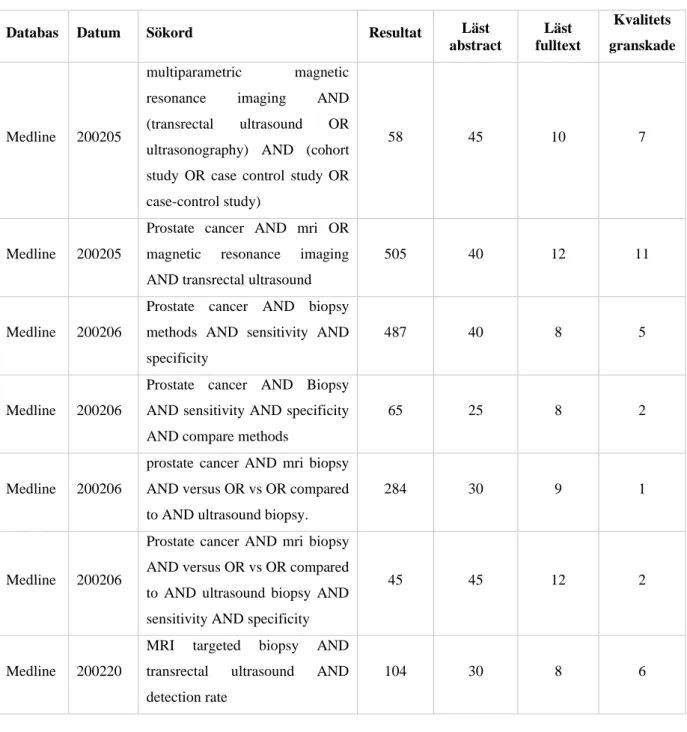
Första sökningen av vetenskapliga artiklar och rapporter till arbetet gjordes i december 2019. Denna sökning ledde inte till några sparade artiklar utan gjordes endast för att gruppen skulle få en överblick av hur mycket material som fanns tillgängligt. I februari 2020 påbörjades den egentliga artikelsökningen. Sökningen gjordes genom Jönköping University biblioteks webbsida där Medline användes som databas. Boolesk sökologi med AND och OR tillämpades då de olika sökorden användes i olika kombinationer (Forsberg & Wengström, 2016). De inledande sökorden var prostate cancer, mri, ultrasound, biopsy, sensitivity, specificity som sedan utökades med MRI targeted biopsy, transrectal ultrasound, detection rate. Redovisning av vilka sökningar som gjordes och hur många artiklar de genererade presenteras i tabell 1.
11
Manuella sökningar gjordes genom kedjesökningar. Detta innebar att gruppen hittade relevanta artiklar i referenslistor till artiklar som framkommit efter sökningar i Medline. Kedjesökningarna resulterade i två artiklar.
Tabell 1. Sammanställning av vilken databas och sökord som har använts. Här presenteras även hur många artiklar som sökningarna resulterat i och hur många som har gått vidare till kvalitetsgranskning.
4:3 Analys
De utvalda artiklarna gick sedan vidare till en kvalitetsgranskning som gjordes med hjälp av granskningsprotokoll hämtade från Avdelningen för omvårdnad på Hälsohögskolan (bilaga 1).
Databas Datum Sökord Resultat Läst
abstract Läst fulltext Kvalitets granskade Medline 200205 multiparametric magnetic resonance imaging AND (transrectal ultrasound OR ultrasonography) AND (cohort study OR case control study OR case-control study)
58 45 10 7
Medline 200205
Prostate cancer AND mri OR magnetic resonance imaging AND transrectal ultrasound
505 40 12 11
Medline 200206
Prostate cancer AND biopsy methods AND sensitivity AND specificity
487 40 8 5
Medline 200206
Prostate cancer AND Biopsy AND sensitivity AND specificity AND compare methods
65 25 8 2
Medline 200206
prostate cancer AND mri biopsy AND versus OR vs OR compared to AND ultrasound biopsy.
284 30 9 1
Medline 200206
Prostate cancer AND mri biopsy AND versus OR vs OR compared to AND ultrasound biopsy AND sensitivity AND specificity
45 45 12 2
Medline 200220
MRI targeted biopsy AND transrectal ultrasound AND detection rate
12
Granskningsprotokollet innehöll två delar. I den första delen skulle samtliga fyra frågor besvaras med ett Ja för att artikeln skulle gå vidare till del två. Del två bestod av sju frågor som behandlade artikelns relevans för syftet. Varje fråga som besvarades med ett Ja gav ett poäng. 1–3 poäng gav artikeln en låg kvalitet och skulle därför exkluderas. 4–5 gav en medelhög kvalitet och 6–7 en hög kvalitet. Målet var att inkludera 15–20 artiklar med hög kvalitet.
De artiklar som gick vidare från kvalitetsgranskningen analyserades enskilt av gruppmedlemmarna och jämfördes sedan med varandra. Artiklarna analyserades med hjälp av en manifest innehållsanalys vilket innebar att gruppen studerade det som direkt uttrycktes i texten utan att göra egna tolkningar (Forsberg & Wengström, 2016). Artiklarna var kvantitativa, så fokus låg på siffror och mätningar. Varje artikel bearbetades sedan grundligt, var och en för sig. Den beskrivande statistiken studerades, där antal och procent användes för kartläggning av männens biopsiresultat. Därefter arbetades en översiktstabell fram där alla valda studier ingick. Tabellen redovisade syfte, metod och resultat och tillförde en struktur på det material som sedan analyserades och inkluderades i resultatet (Bilaga 2). Likheter respektive skillnader mellan valda artiklar sorterades fram, där fokus låg på artiklarnas resultatdel och variablerna som framkom. Det analyserade materialet sammanställdes sedan där undersökningsmetoderna redovisades för varje artikel. Procenten för den totala upptäckten och prevalensen av kliniskt insignifikant och signifikant cancer dokumenterades för de olika diagnostiseringsmetoderna och redovisades med hjälp av tabeller och löpande text (Forsberg & Wengström, 2016).
4:4 Etiska överväganden
Röntgensjuksköterskan arbetar utefter en yrkesetisk kod som innefattar forskning och utveckling där forskningsetiska regler ska följas (Svensk förening för röntgensjuksköterskor, 2008). Därför gjordes en etisk egengranskning där uppgifter om studien fylldes i. Formuläret behövdes inte skickas in till etiska kommittén för granskning då studien baserades på litteratur/artiklar och inga människor eller djur påverkades i studien.
För att artiklarna i litteraturstudien skulle vara relevanta för syftet granskades de med hjälp av ett granskningsprotokoll som fanns framtaget för kvantitativa studier. I de valda artiklarna skulle det finnas med ett godkänt etiktillstånd för att få ingå i studien.
13
5 Resultat
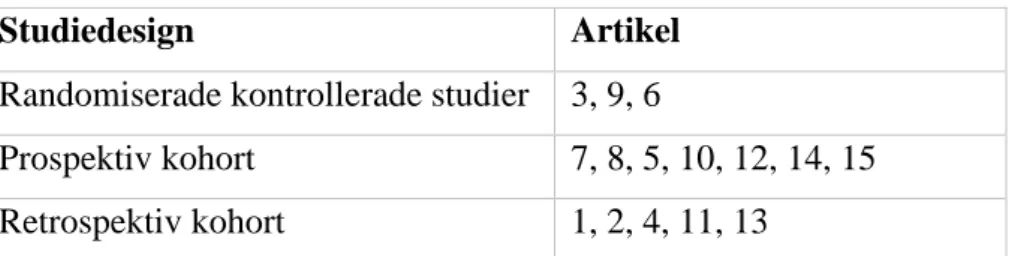
Totalt inkluderades femton artiklar i studien som var publicerade mellan 2015–2020 (bilaga 2). Alla artiklarna som användes i resultatet hade hög kvalité, vilket innebar en poäng mellan sex och sju i kvalitetsgranskningen. Artiklarna bestod av randomiserade kontrollerade studier, pro- och retrospektiva kohortstudier (tabell 2). I texten och tabellerna som följer refereras inkluderade artiklar i resultatet till nummerordning enligt översiktstabell i bilaga 2.
Tabell 2. Sammanställning av artiklarnas studiedesign.
Studiedesign Artikel
Randomiserade kontrollerade studier 3, 9, 6
Prospektiv kohort 7, 8, 5, 10, 12, 14, 15
Retrospektiv kohort 1, 2, 4, 11, 13
Gemensamt för alla studier var att männen som deltog hade ett förhöjt PSA-värde och/eller hade genomgått ultraljud eller datortomografi som visade på misstänkta områden i prostatan. Detta innebar att alla deltagande män hade en klinisk misstanke om prostatacancer. Gränsen för hur högt PSA-värde som männen hade skiljde dock mellan studierna. Alla artiklar satte gränsvärdet för PSA mellan 3-5µg/l, bortsett från artikel 11 där män med PSA mellan 3–30 µg/l inkluderades. I nio av studierna hade samma grupp genomgått båda biopsimetoderna och i sex av studierna hade männen delats in i två olika grupper där de fick genomgå varsin metod, oberoende av varandra. Dessa artiklar är gråmarkerade i tabell 3 och 4. Den diagnostiska träffsäkerheten för TRULS-ledda systematiska biopsier räknades ut på alla män som genomgick metoden. De män som gjorde riktade biopsier startade alltid med en MR-bildtagning för att lokalisera de misstänka områdena. Däremot skiljde artiklarna sig åt i hur den diagnostiska träffsäkerheten räknades ut för de män som gjorde MR-undersökning med riktade biopsier. I artikel 3, 6, 7, 8, 9, 10, 11, 15 räknades detektionsgraden av prostatacancer ut av andel män som hade genomgått MR-bildtagning, trots att inte alla hade genomgått riktad biopsi. Det kan förklaras med att även om inget misstänkt fynd på MR-bilden fanns så inkluderades männen i det totala resultatet. I artikel 1, 2, 4, 5, 12, 13, 14 räknades detektionsgraden av prostatacancer ut av andel män som hade gjort riktade biopsier, där de männen utan misstanke/lågt PI-RADS-värde på MR-bilden exkluderades i det totala resultatet.
14 5:1 Upptäckten av prostatacancer
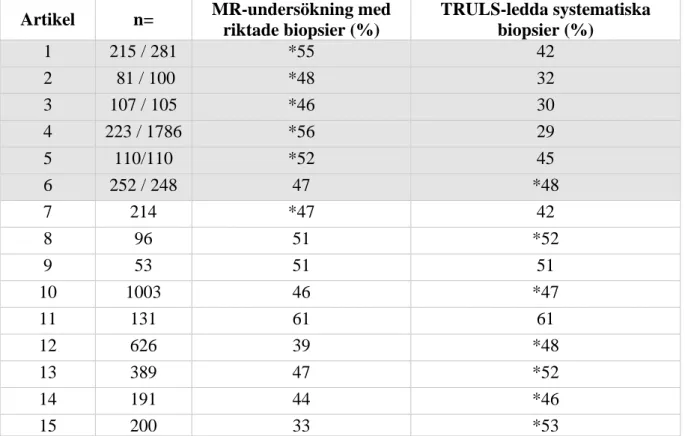
Upptäckten av prostatacancer definierades av andel män vars biopsier visade på malignitet, innan de blivit klassificerade som klinisk signifikant eller insignifikant cancer. Tabell 3 visar antal män som genomgått en MR-undersökning med riktad biopsi och/eller TRULS-ledd systematisk biopsi och hur stor andel av männen som visade sig ha en prostatacancer. I artikel 1–6, där deltagande män har delats in i två olika grupper och genomgått varsin biopsimetod, hittade MR-undersökning med riktade biopsier en högre andel män med prostatacancer. I artikel 7–15, där deltagande män genomgått båda biopsimetoderna, hittade TRULS-ledda systematiska biopsier en högre andel män med cancer. I två av artiklarna hittade båda metoderna lika stor del prostatacancer.
Tabell 3. Sammanställning av upptäckt malignitet (%) för de båda metoderna. Grå markering betyder att det inte är samma grupp av män som har genomgått båda metoderna.
Artikel n= MR-undersökning med
riktade biopsier (%) TRULS-ledda systematiska biopsier (%) 1 215 / 281 *55 42 2 81 / 100 *48 32 3 107 / 105 *46 30 4 223 / 1786 *56 29 5 110/110 *52 45 6 252 / 248 47 *48 7 214 *47 42 8 96 51 *52 9 53 51 51 10 1003 46 *47 11 131 61 61 12 626 39 *48 13 389 47 *52 14 191 44 *46 15 200 33 *53 n= antal försökspersoner.
15
5:2 Prevalens av insignifikant och signifikant cancer.
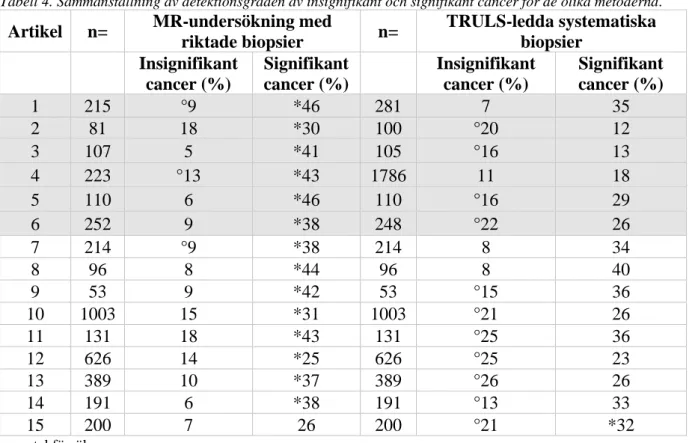
Maligniteterna som hittades av de olika biopsimetoderna i tabell 3, skattades sedan av patologer baserat på mönster i vävnadsproverna med hjälp av gleasonsumman. Klinisk insignifikant cancer, alltså cancer som inte kräver behandling i nuläget, räknades som tumörer med gleasonvärde ≤6 och klinisk signifikant cancer räknades som tumörer med gleasonvärde ≥7. Detta gällde för alla artiklar utom artikel 5, där signifikant cancer räknades från gleasonvärde ≥6. I tabell 4 redovisas hur stor del av den upptäckta cancern hos de deltagande männen som var klinisk insignifikant och klinisk signifikant.
I fjorton av totalt femton artiklar hittade MR-undersökningen med riktade biopsier fler kliniskt signifikanta cancrar. Endast en artikel visade att TRULS-ledda systematiska biopsier hittar ett högre antal kliniskt signifikant cancer än MR-undersökning med riktade biopsier. TRULS-ledda systematiska biopsier har enligt elva artiklar en högre diagnostisk träffsäkerhet när det gäller insignifikant cancer. I artikel 12 skriver författarna att upptäckten av insignifikant cancer ofta leder till överdiagnostisering och onödigt lidande bland män som inte är i behov av behandling för sin prostatacancer. I artikel 15 skriver författarna att signifikant cancer har hittats bland de patienter som fick negativt MR-resultat efter bildtagningen och som därför bara gjorde TRULS-ledda systematiska biopsier. Liknande fynd tas även upp i artikel 3, 7, 11 och 14. I de artiklarna har båda metoderna hittat signifikant cancer som den andra metoden har missat. I artikel 3 fick de män som diagnostiserats med benignt fynd genomgå även den andra metoden. Då hittades cancer som den första metoden missat. TRULS-ledda systematiska biopsier har missat 5–21% signifikant cancer och MR-undersökning med riktade biopsier har missat 1–14 % signifikant cancer. Författarna till dessa artiklar anser därför att män som för första gången ska genomgå en biopsi bör göra både MR-undersökning med riktade biopsier och TRULS-ledda systematiska biopsier. Detta för att inte missa en signifikant cancer och för att få en bild av utgångsläget inför eventuella framtida biopsier.
16
Tabell 4. Sammanställning av detektionsgraden av insignifikant och signifikant cancer för de olika metoderna.
Artikel n= MR-undersökning med
riktade biopsier n= TRULS-ledda systematiska biopsier Insignifikant cancer (%) Signifikant cancer (%) Insignifikant cancer (%) Signifikant cancer (%) 1 215 °9 *46 281 7 35 2 81 18 *30 100 °20 12 3 107 5 *41 105 °16 13 4 223 °13 *43 1786 11 18 5 110 6 *46 110 °16 29 6 252 9 *38 248 °22 26 7 214 °9 *38 214 8 34 8 96 8 *44 96 8 40 9 53 9 *42 53 °15 36 10 1003 15 *31 1003 °21 26 11 131 18 *43 131 °25 36 12 626 14 *25 626 °25 23 13 389 10 *37 389 °26 26 14 191 6 *38 191 °13 33 15 200 7 26 200 °21 *32 n= antal försökspersoner.
*=högst % av signifikant cancer för metoderna. °=högst % av insignifikant cancer för metoderna.
17
6 Diskussion
6:1 Metoddiskussion
Vid val av metod studerades tillvägagångssätt och kriterier för olika typer av litteraturstudier. Metoden som valdes i arbetet var en litteraturstudie med systematiskt ansats, då den ansågs passa bäst för att svara på syftet. En systematisk litteraturstudie kan enligt Forsberg och Wengström (2016) vara för omfattande att göra för ett examensarbete. Resultatet i denna studie omfattar inte all forskning som finns inom ämnet och inte heller allt som har framkommit i artiklarnas resultat, utan endast de delar som innefattar detektionsgrad av cancer. Att endast ha en systematisk ansats passade därför bättre, då det inte var en heltäckande studie som skulle göras. Ett alternativ hade kunnat vara att göra en scoping review, som enligt Forsberg och Wengström (2016) omfattar ett begränsat antal studier och passar bra för studentarbeten. Det är en bra metod att använda för att identifiera lämpliga parametrar till en systematisk litteraturstudie, såsom jämförelse och utfall. Dock lämpar sig en scoping review bättre för en bred forskningsfråga där kvalitetskriterier saknas. Denna studie har ett avgränsat syfte med bestämda kvalitetskriterier, vilket också bidrog till beslutet om att ha en systematisk ansats.
Artiklarna i resultatet är endast hämtade från databasen Medline. Eftersom Medline är en bred databas, så togs beslutet att inleda sökningen där (Forsberg & Wengström, 2016). Den gav genast många träffar och mycket material att börja bearbeta. Några få sökningar gjordes även i PubMed och Cinahl, för att få en överblick av utbudet. Upplevelsen var att de artiklar som var relevanta för syftet, även hade hittats i Medline. För att få ett större urval till studien, så hade sökningarna kunnat utökas i PubMed och Cinahl, vilket hade ökat reliabiliteten. Sökorden skrevs i fritext och kombinerades med både OR och AND vilket resulterade i fler funna artiklar. Vetenskapliga artiklar som var publicerade de senaste fem åren inkluderades i studien. Detta gjorde att den senaste forskningen inom bilddiagnostik för prostatacancer kunde inkluderas. Eftersom det är ett område där mycket forskning pågår och nya metoder arbetas fram, så var inte äldre forskning relevant för syftet. En jämförelse av förmågan att upptäcka prostatacancer mellan TRULS-ledda systematiska biopsier och MR-undersökning med riktade biopsier var givet i artiklarna, för att få en så rättvis bild av detektionsgraden som möjligt. Det fanns mycket forskning inom bilddiagnostik som berörde prostatacancer och olika biopsimetoder. Till en början var syftet att titta på sensitivitet och specificitet för de olika metoderna. Det ändrades med tiden till att det var mer relevant att göra en översikt för träffsäkerheten av klinisk signifikant och insignifikant cancer för de olika metoderna, då det förekom i större utsträckning
18
i de studerade artiklarna.Detta bidrog till att sökningen utökades under arbetets gång med andra sökord för att få ett större material att jobba med och bättre kunna svara på syftet. Sökorden preciserades vilket gjorde att fler relevanta artiklar sparades. Datainsamlingen av artiklar redovisades i tabell 1, vilket gör att det enkelt att följa sökningarna som gjordes. Manuell sökning användes också genom att undersöka referenslistor i redan valda artiklarna. Det genererade fler artiklar som var relevanta för syftet.
De valda artiklarna gick vidare till kvalitetsgranskning där Protokoll för basala kvalitetsregister för studier med kvantitativ metod användes (bilaga 1). Användningen av kvalitetsgranskade artiklar innebar att varje artikel hade relevans för syftet i studien och ett etiskt godkännande som var krav för att användas i resultatet. De artiklar som inkluderades i denna studie hade hög kvalitet vilket innebar att validiteten i studien ökade. Tre av artiklarna i resultatet är randomiserade kontrollerade studier, vilka anses ha ett högt bevisvärde. Dessa anses bäst kunna svara på vilken behandling eller metod som är mest effektiv. Resterande artiklar är kohortstudier, där sju artiklar är prospektiva och fem är retrospektiva. Efter randomiserade kontrollerade studier och icke randomiserade studier anses prospektiva kohortstudier ha det högsta bevisvärdet. Retrospektiva kohortstudier anses ha ett lägre bevisvärde (Forsberg & Wengström, 2016). Reliabiliteten i denna studie stärks av att artiklarna anses ha ett högt bevisvärde.
Målet var att få med 15–20 artiklar i litteraturstudien. Till en början upplevdes språket i artiklarna som utmanande, då gruppen inte var bekant med metoderna och de medicinska termerna som användes. Efter grundlig läsning av artiklarna sågs ett samband i metoder och terminologi och då kom även insikten att biopsimetoderna skiljde sig åt. Den diagnostiska träffsäkerheten av prostatacancer skulle endast bestå av TRULS-ledda systematiska biopsier och MR-undersökning med riktade biopsier och inte innefatta några andra metoder. I de artiklar som exkluderades hade MR-undersökning med riktade biopsier jämförts med systematiska biopsier som inte var ultraljudsledda, utan där biopsikolvarna togs över hela prostatan med 5 mm mellanrum. Detta var snarlikt, men inte helt jämförbart med TRULS-ledda systematiska biopsier. Riktade biopsier efter en MR-undersökning kan göras på olika sätt, antingen direkt i MR-kameran eller i efterhand med fusionmetod. Enligt Drost et al., (2019) förekom det ingen signifikant skillnad mellan metoderna och därför påverkade det inte valet av artiklar till studien. I sex av artiklarna i resultatet var det olika antal deltagare för metoderna och männen i studierna genomgick inte båda biopsimetoderna. Detta kan påverka resultatet då dessa artiklar inte går att
19
ställa mot resterande artiklar där alla män genomgick både TRULS-ledda systematiska biopsier och MR-undersökning med riktade biopsier. Biopsierna i artiklarna gjordes på olika sätt, antingen användes en transperinal eller transrektal metod. Vid transperinala biopsier förs biopsinålen in genom huden in till prostatan och vid transrektala biopsier förs biopsinålen in via tarmen och genom tarmväggen till prostatan. I en studie av Hara et al., (2008) gjordes en jämförelse mellan transperinala och transrektala biopsier. Studien visade ingen signifikant skillnad på den totala upptäckten av prostatacancer. Därför påverkade inte heller biopsimetoden valet av artiklar till litteraturstudien.
Referenssystemet som valdes var APA, då författarna är mest insatta i detta system. I resultatdelen och resultatdiskussionen togs beslutet att frångå detta. I text och tabeller refereras istället artiklarna som inkluderades i resultatet till nummerordningen i översiktstabellen. Detta gjordes för att resultatet skulle bli tydligare och lättare för läsaren att följa med i.
20 6:2 Resultatdiskussion
I studierna biopseras män med ett förhöjt PSA-värde. Detta värde skiljer sig dock mellan de olika studierna, där gränsen ligger på ett intervall mellan 3–30 µg/l. I majoriteten av studier används ett gränsvärde mellan 3–5 µg/l, men artikel 11 har satt intervallet till 3–30 µg/l. Det kan vara en förklaring till att detektionsgraden är så hög i denna studie, då ett högre PSA enligt de nationella rekommendationerna kan kopplas till en större risk för prostatacancer (RCC, 2020). I artikel 5 räknades signifikant cancer för tumörer graderade som gleason ≥6. Tumörer med ett gleasonvärde som andra studier har skattat som insigifikanta räknas som signifikant cancer här. Andelen insignifikant cancer blir därför låg i förhållande till signifikant cancer för denna studie.
Detektionsgraden för MR-undersökning med riktade biopsier har räknats ut på olika sätt i artiklarna. Antingen har andelen män med upptäckt cancer dividerats med alla som genomgick MR-bildtagning, eller så har de dividerats med de som gick vidare till biopsering. Detta trodde gruppen skulle påverka resultatet och ge större skillnader, men resultaten skiljer sig inte nämnvärt åt. För de artiklar där detektionsgraden har räknats på de som endast gjort biopsier, så blir procenten högre än om den hade räknats på alla som gjort en MR-undersökning. Detta betyder att bara de som har synliga förändringar på MR-bilderna biopseras, vilket naturligtvis ger en högre procent detekterad cancer. Att vissa studier har räknat på detta sätt kan kanske trots allt ge ett missvisande resultat i jämförelse med TRULS-ledda systematiska biopsier, där procenten räknas på alla medverkande.
I tabell 3 redovisades den diagnostiska träffsäkerheten vid misstänkt prostatacancer för TRULS-ledda systematiska biopsier och MR-undersökning med riktade biopsier. Den totala upptäckten av malignitet hos männen som genomgick biopsi visade på olika resultat i artiklarna. Sju studier visade att TRULS-ledda systematiska biopsier hittade fler cancrar än MR-undersökning med riktade biopsier. I två artiklar fick metoderna samma värde och sex artiklar visade att MR-undersökning med riktade biopsier hade högre träffsäkerhet av prostatacancer. Varför TRULS-ledda systematiska biopsier hittar flest cancrar där deltagande män har genomgått båda biopsimetoderna, hittas ingen förklaring till. Båda grupperna har samma kliniska misstanke för prostatacancer. Tillvägagångsätt och ordning för biopsimetoderna var detsamma, så det borde inte påverka biopsiresultaten. Utifrån resultatet, kan båda metoderna användas för att upptäcka prostatacancer eftersom skillnaden mellan dem inte var så stor. När
21
dessa maligniteter hade klassats med hjälp av gleasonsumman visade det sig att MR-undersökning med riktade biopsier hittade fler kliniskt signifikanta cancrar än vad TRULS-ledda systematiska biopsier gjorde, med ett undantag som visade motsatt resultat. Däremot hittade TRULS-ledda systematiska biopsier ett högre antal insignifikanta cancrar. Det kan bero på att fler vävnadsprov tas efter anatomiska områden och därför täcker in stor del av prostatan. Riktade biopsier tas endast på det misstänka området med ett färre antal vävnadsprov. Utifrån resultatet kan slutsatsen dras att MR-undersökning med riktade biopsier är en bättre metod för att minska överdiagnostiken av prostatacancer då fler signifikanta cancrar hittas med metoden. Detta kan bero på samma anledning som den som tidigare nämnts. De riktade biopsierna träffar ett misstänkt område direkt och biopsierna tas endast därifrån, men med systematiska biopsier plockas vävnad från hela prostatan och det behöver inte innebära att biopserad förändring är signifikant cancer.
När arbetet startade stod det i de nationella rekommendationerna från 18-12-11 att alla män med misstanke om prostatacancer rekommenderades en utredning med MR-bildtagning eller TRULS för att sedan avgöra om de skulle genomgå riktade eller systematiska biopsier (RCC, 2018). En ny version släpptes 20-03-03 med nya rekommendationer kring bilddiagnostik vid prostatacancer (RCC, 2020). Förändringen innebar att en övergång till MR-baserad diagnostik och riktade biopsier rekommenderades. För män med måttligt höga PSA-värden är evidensen hög att utredningen bör starta med MR-bildtagning för att sedan ta ställning till om biopsi ska göras. Endast personer med kontraindikation för en MR-undersökning bör biopseras med systematiska biopsier. Med denna förbättring besparas en tredjedel av männen biopsi, vilket minskar överdiagnostiken av kliniskt insignifikant cancer, ökar sensitiviteten för kliniskt signifikant cancer och minskar risken för komplikationer (RCC, 2020).
Studien kan sättas i relation till två andra litteraturstudier och metaanalysers resultat. Enligt Forsberg och Wengström (2016) har metaanalyser ett högt bevisvärde där resultaten kan leda till rekommendationer för nya omvårdnadsåtgärder. Kasivisvanathan et al., (2019) gjorde en jämförelse av detektionsgraden för kliniskt signifikant och insignifikant cancer för MR-undersökning med riktade biopsier som ställdes mot TRULS-ledda systematiska biopsier. Författarna menade att det viktigaste i resultatet var att MR-undersökning med riktade biopsier hittade fler kliniskt signifikanta cancrar och mindre insignifikanta cancrar hos män med misstänkt prostatacancer. Denna metod kräver dessutom ett mindre antal biopsier. De menar att MR-undersökning med riktade biopsier är en alternativ diagnostisk metod till TRULS-ledda
22
systematiska biopsier. Schoots et al., (2015) utvärderade fördelarna för MR-undersökning med riktade biopsier jämfört med TRULS-ledda systematiska biopsier där den övergripande detektionen av prostatacancer och klinisk signifikant cancer mot insignifikant cancer undersöktes. Författarna kom fram till att hos män med misstänkt prostatacancer skiljde sig inte metoderna åt i den övergripande detektionen av cancer. Däremot hade MR-undersökning med riktade biopsier en högre träffsäkerhet vad gäller kliniskt signifikanta cancrar och lägre träffsäkerhet för insignifikanta cancrar jämfört med vad TRULS-ledda systematiska biopsier hade. Trots detta kunde inte författarna i studien dra slutsatsen att TRULS-ledda systematiska biopsier kan uteslutas då metoden hittar cirka 12% kliniskt signifikant cancer som visats negativt på MR-bilden (Schoots et al., 2015). Detta är ett ämne som även berörs i denna studies resultat. I fem av artiklarna i resultatet har båda metoderna hittat signifikant cancer som den andra metoden har missat. Vid MR-undersökningarna har det missats 1–14% signifikant cancer och därför har inga biopsier tagits i detta område. En TRULS-ledd systematisk biopsi har sedan fångat upp denna missade cancer eftersom hela prostatan biopseras. Likaså har den TRULS-ledda systematiska biopsin missat 5–21% signifikant cancer som MR-bildtagningen har detekterat. I de nya rekommendationerna står det att tumörer som är bedömda som en PI-RADS 1–2 efter en MR-bildtagning skulle kunna vara en högriskcancer om PSA-densiteten på prostatan överstiger 0,15 µg/l/cm³ (RCC, 2020). En negativ MR-bildtagning där misstänkta områden bedömts som PI-RADS 1–2, kan alltså i samband med ett högt PSA-värde tyda på en högriskcancer. Dessa bör enligt rekommendationerna därför biopseras med TRULS-ledda systematiska biopsier, för att hitta maligna förändringar som enligt MR-bildtagningen är benigna. Detta kan också vara en förklaring till varför båda metoderna missar signifikant cancer i fem av de inkluderade artiklarna och att båda metoderna tillsammans fångar upp de flesta cancrarna. De nya rekommendationerna från 2020 går i linje med gruppens resultat.
När de nya rekommendationerna börjar användas i större utsträckning av klinikerna innebär det också att MR-undersökningar av män med misstänkt prostatacancer kommer att öka (RCC, 2020). Enligt NPCR senaste kvalitetsrapport som nämns i bakgrunden ökade användningen av MR-undersökning med riktade biopsier innan de nya rekommendationerna kom (NPCR, 2018). Det var stor spridning i landet men 15% diagnostiserades med metoden. MR-bildtagningen kommer bli en ännu mer central och viktig del i diagnostiken av prostatacancer, vilket kommer påverka röntgensjuksköterskans roll. Därför är det som röntgensjuksköterska viktigt att ha bra kunskap om sjukdomen för att kunna ge patienten ett bra bemötande med relevant information. Detta skapar i sin tur trygghet för patienten innan, under och efter undersökningen. Samarbetet
23
mellan professionerna är av stor betydelse för att bildtagning och protokoll ska bli optimala. Radiologen får på så sätt en optimal möjlighet att ställa rätt diagnos och hittar kliniskt signifikanta cancrar och minimerar antalet insignifikanta cancrar. När detta görs minskar överdiagnostik och det leder till att de män som inte behöver, slipper genomgå behandling och besparas lidande. Detta arbete behandlar enbart detektionsgraden och det finns andra aspekter som bör vägas in och tas hänsyn till, såsom kostnadseffektivitet, tillgänglighet, smärta och komplikationer.
6:3 Komplikationer av biopsier
När artiklarna bearbetades hittades fynd i artikel 6 som berörde komplikationer. Dessa fynd svarar inte på syftet, men är intressanta att lyfta då de anses vara viktiga ut ett patientperspektiv. Metoden för att diagnostisera prostatacancer bör innefatta så få komplikationer som möjligt för patienten. Författarna beskriver att komplikationerna efter 30 dagar var mindre frekventa för den gruppen som hade genomgått MR-undersökning med riktade biopsier jämfört med TRULS-ledda systematiska biopsier. Komplikationerna innefattade blod i urinen (30% mot 63%), blod i sperma (32% mot 60%), smärta på instickstället (13% mot 23%), rektal blödning (14% mot 22%) och erektil dysfunktion (11% mot 16%). Enligt författarna kan dessa fynd förklaras med att färre biopsier tas vid MR-undersökning med riktade biopsier jämfört med TRULS-ledda systematiska biopsier. Totalt 2% av männen i den MR-riktade biopsigruppen och 2% i gruppen med TRULS-ledda systematiska biopsier hade allvarliga biverkningar. En litteraturstudie av Borghesi et al., (2017) undersökte komplikationer efter TRULS-ledda systematiska biopsier och MR-undersökning med riktade biopsier. Den mest rapporterande komplikationen efter en prostatabiopsi oberoende vilken metod som används var mindre blödningar. Vissa män upplevde även övergående lower urinary tract symtoms (LUTS) eller erektil dysfunktion. Vid MR-undersökning med riktad biopsi jämfört med TRULS-ledda systematiska biopsier minskade andelen LUTS och smärta hos patienterna. Även allvarliga komplikationer, sepsis eller sjukhusvistelse var marginellt när MR-undersökning med riktade biopsier användes (Borghesi et al., 2017). Dessa studier visar en fördel för MR-undersökning med riktade biopsier gentemot TRULS-ledda systematiska biopsier, då färre biopsier behöver tas vid varje tillfälle och minskar därför både smärtan och komplikationerna för patienterna.
6:4 Förslag på vidare forskning
Vidare hade det varit av intresse att undersöka huruvida klinikerna i Sverige arbetar efter de nya nationella rekommendationerna inom prostatacancerdiagnostik. Detta skulle kunna göras
24
med en tvärsnittsstudie där enkätfrågor skickades ut till kliniker i hela Sverige, alternativt en intervjustudie där urologer och radiologer intervjuas om rutinerna vid prostatabiopsier.
25
7 Slutsatser
MR-undersökning med riktade biopsier är en bra metod för att öka den diagnostiska träffsäkerheten för att hitta klinisk signifikant cancer och minska antalet insignifikant cancer hos män med misstänkt prostatacancer. Metoden innehåller även färre antal biopsier vilket minskar komplikationerna hos männen. Dock går det inte att utesluta TRULS-ledda systematiska biopsier då kontraindikationer för att genomgå en MR-undersökning och missade signifikanta cancrar på MR-undersökning med riktade biopsier förkommer. Den ideala metoden för prostatacancerdiagnostisering skulle innehålla få komplikationer för patienten, identifiering av cancern på ett optimalt sätt och minimering av antalet insignifikant cancer för att förhindra överdiagnostik och behandling i onödan för många män.
26
Referenser
Artiklar i resultatet är markerade med *
Allisy-Roberts, P., & Williams, J. (2008). Farr´s Physics for Medical Imaging (2nd ed.). Saunders Elsevier.
Almås, H., Stubberud, D., & Grønseth, R (ed.). (2011). Klinisk omvårdnad 2. (2 uppl.). Liber.
American college of radiology. (2015). Prostate imaging-Reporting and data system (version 2). https://www.acr.org/-/media/ACR/Files/RADS/Pi-RADS/PIRADS-V2.pdf?la=en
Aspelin, P., & Petterson, H. (2008). Radiologi (1:2 uppl.). Studentlitteratur.
*Bansal, S., Gupta, N. P., Yadav, R., Khera, R., Ahlawat, K., Gautam, D., Ahlawat, R., & Gautam, G. (2017). Multiparametric magnetic resonance imaging-transrectal ultrasound fusion prostate biopsy: A prospective, single centre study. Indian Journal of Urology: IJU : Journal of the Urological Society of India, 33(2), 134–139. https://doi-org.proxy.library.ju.se/10.4103/0970-1591.203414
Berglund, E., & Jönsson, B. (2007). Medicinsk fysik (1 uppl.). Studentlitteratur.
Borghesi, M., Ahmed, H., Nam, R., Schaeffer, E., Schiavina, R., Taneja, S., Weidner, W., & Loeb, S. (2017). Complications After Systematic, Random, and Image-guided Prostate
Biopsy. European Urology, 71(3), 353–365.
https://doi-org.proxy.library.ju.se/10.1016/j.eururo.2016.08.004
*Borkowetz, A., Hadaschik, B., Platzek, I., Toma, M., Torsev, G., Renner, T., Herout, R., Baunacke, M., Laniado, M., Baretton, G., Radtke, J. P., Kesch, C., Hohenfellner, M., Froehner, M., Schlemmer, H.-P., Wirth, M., & Zastrow, S. (2018). Prospective comparison of transperineal magnetic resonance imaging/ultrasonography fusion biopsy and transrectal systematic biopsy in biopsy-naïve patients. BJU International, 121(1), 53–60. https://doi-org.proxy.library.ju.se/10.1111/bju.14017
27
*Choi, Y. H., Kang, M. Y., Sung, H. H., Jeon, H. G., Chang Jeong, B., Seo, S. I., Jeon, S. S., Kim, C. K., Park, B. K., & Lee, H. M. (2019). Comparison of Cancer Detection Rates Between TRUS-Guided Biopsy and MRI-Targeted Biopsy According to PSA Level in Biopsy-Naive Patients: A Propensity Score Matching Analysis. Clinical Genitourinary Cancer, 17(1), e19–e25. https://doi-org.proxy.library.ju.se/10.1016/j.clgc.2018.09.007
Drost, F.-J. H., Osses, D. F., Nieboer, D., Steyerberg, E. W., Bangma, C. H., Roobol, M. J., & Schoots, I. G. (2019). Prostate MRI, with or without MRI-targeted biopsy, and systematic biopsy for detecting prostate cancer. The Cochrane Database of Systematic
Reviews, 4, CD012663.
https://doi-org.proxy.library.ju.se/10.1002/14651858.CD012663.pub2
Forsberg, C., & Wengström, Y. (2016). Att göra systematiska litteraturstudier (4 uppl.). Natur & Kultur.
*Fourcade, A., Payrard, C., Tissot, V., Perrouin-Verbe, M.-A., Demany, N., Serey-Effeil, S., Callerot, P., Coquet, J.-B., Doucet, L., Deruelle, C., Joulin, V., Nonent, M., Fournier, G., & Valeri, A. (2018). The combination of targeted and systematic prostate biopsies is the best protocol for the detection of clinically significant prostate cancer.
Scandinavian Journal of Urology, 52(3), 174–179.
https://doi-org.proxy.library.ju.se/10.1080/21681805.2018.1438509
*Fujii, S., Hayashi, T., Honda, Y., Terada, H., Akita, R., Kitamura, N., Ueda, E., Han, X., Ueno, T., Miyamoto, S., Kitano, H., Inoue, S., Teishima, J., Abdi, H., Awai, K., Takeshima, Y., Sentani, K., Yasui, W., & Matsubara, A. (2020). Magnetic resonance imaging/transrectal ultrasonography fusion targeted prostate biopsy finds more significant prostate cancer in biopsy-naïve Japanese men compared with the standard biopsy. International Journal of Urology: Official Journal of the Japanese Urological Association, 27(2), 140–146. https://doi-org.proxy.library.ju.se/10.1111/iju.14149
Hara, R., Jo, Y., Fujii, T., Kondo, N., Yokoyoma, T., Miyaji, Y., & Nagai, A. (2008). Optimal approach for prostate cancer detection as initial biopsy: prospective randomized study comparing transperineal versus transrectal systematic 12-core biopsy. Urology, 71(2), 191–195. https://doi-org.proxy.library.ju.se/10.1016/j.urology.2007.09.029
28
*Kasivisvanathan, V., Rannikko, A. S., Borghi, M., Panebianco, V., Mynderse, L. A., Vaarala, M. H., Briganti, A., Budäus, L., Hellawell, G., Hindley, R. G., Roobol, M. J., Eggener, S., Ghei, M., Villers, A., Bladou, F., Villeirs, G. M., Virdi, J., Boxler, S., Robert, G., … Moore, C. M. (2018). MRI-Targeted or Standard Biopsy for Prostate-Cancer Diagnosis.
The New England Journal of Medicine, 378(19), 1767–1777.
https://doi-org.proxy.library.ju.se/10.1056/NEJMoa1801993
Kasivisvanathan, V., Stabile, A., Neves, J. B., Giganti, F., Valerio, M., Shanmugabavan, Y., Clement, K. D., Sarkar, D., Philippou, Y., Thurtle, D., Deeks, J., Emberton, M., Takwoingi, Y., & Moore, C. M. (2019). Magnetic Resonance Imaging-targeted Biopsy Versus Systematic Biopsy in the Detection of Prostate Cancer: A Systematic Review and Meta-analysis. European Urology, 76(3), 284–303. https://doi-org.proxy.library.ju.se/10.1016/j.eururo.2019.04.043
*Mannaerts, C. K., Gayet, M., Verbeek, J. F., Engelbrecht, M. R. W., Savci-Heijink, C. D., Jager, G. J., Gielens, M. P. M., van der Linden, H., Beerlage, H. P., de Reijke, T. M., Wijkstra, H., & Roobol, M. J. (2018). Prostate Cancer Risk Assessment in Biopsy-naïve Patients: The Rotterdam Prostate Cancer Risk Calculator in Multiparametric Magnetic Resonance Imaging-Transrectal Ultrasound (TRUS) Fusion Biopsy and Systematic TRUS Biopsy. European Urology Oncology, 1(2), 109–117. https://doi-org.proxy.library.ju.se/10.1016/j.euo.2018.02.010
*Mariotti, G. C., Costa, D. N., Pedrosa, I., Falsarella, P. M., Martins, T., Roehrborn, C. G., Rofsky, N. M., Xi, Y., M Andrade, T. C., Queiroz, M. R., Lotan, Y., Garcia, R. G., Lemos, G. C., & Baroni, R. H. (2016). Magnetic resonance/transrectal ultrasound fusion biopsy of the prostate compared to systematic 12-core biopsy for the diagnosis and characterization of prostate cancer: multi-institutional retrospective analysis of 389 patients. Urologic Oncology, 34(9), 416.e9-416.e14. https://doi-org.proxy.library.ju.se/10.1016/j.urolonc.2016.04.008
29
Nationella prostatacancerregistret. (2018). Prostatacancer: Nationell kvalitetsrapport för 2018. https://www.cancercentrum.se/globalassets/cancerdiagnoser/prostatacancer/rapporter/2 0190905_npcr_nationell_rapport_2018.pdf
*Oberlin, D. T., Casalino, D. D., Miller, F. H., Matulewicz, R. S., Perry, K. T., Nadler, R. B., Kundu, S., Catalona, W. J., & Meeks, J. J. (2016). Diagnostic Value of Guided Biopsies: Fusion and Cognitive-registration Magnetic Resonance Imaging Versus Conventional Ultrasound Biopsy of the Prostate. Urology, 92, 75–79. https://doi-org.proxy.library.ju.se/10.1016/j.urology.2016.02.041
*Peltier, A., Aoun, F., Lemort, M., Kwizera, F., Paesmans, M., & Van Velthoven, R. (2015). MRI-targeted biopsies versus systematic transrectal ultrasound guided biopsies for the diagnosis of localized prostate cancer in biopsy naïve men. BioMed Research
International, 2015, 571708. https://doi-org.proxy.library.ju.se/10.1155/2015/571708
*Porpiglia, F., Manfredi, M., Mele, F., Cossu, M., Bollito, E., Veltri, A., Cirillo, S., Regge, D., Faletti, R., Passera, R., Fiori, C., & De Luca, S. (2017). Diagnostic Pathway with Multiparametric Magnetic Resonance Imaging Versus Standard Pathway: Results from a Randomized Prospective Study in Biopsy-naïve Patients with Suspected Prostate Cancer. European Urology, 72(2), 282–288. https://doi-org.proxy.library.ju.se/10.1016/j.eururo.2016.08.041
Regionala cancercentrum. (2018). Prostatacancer: Nationellt vårdprogram (version 4.0).
Hämtad 200128 från
https://www.cancercentrum.se/globalassets/cancerdiagnoser/prostatacancer/vardprogra m/nationellt-vardprogram-prostatacancer.pdf
Regionala cancercentrum. (2020). Prostatacancer: Nationellt vårdprogram (version 5.0).
Hämtad 200422 från
https://www.cancercentrum.se/globalassets/cancerdiagnoser/prostatacancer/vardprogra m/nationellt-vardprogram-prostatacancer.pdf
Schoots, I. G., Roobol, M. J., Nieboer, D., Bangma, C. H., Steyerberg, E. W., & Hunink, M. G. M. (2015). Magnetic resonance imaging-targeted biopsy may enhance the diagnostic
30
accuracy of significant prostate cancer detection compared to standard transrectal ultrasound-guided biopsy: a systematic review and meta-analysis. European Urology, 68(3), 438–450. https://doi-org.proxy.library.ju.se/10.1016/j.eururo.2014.11.037
*Siddiqui, M. M., Rais-Bahrami, S., Turkbey, B., George, A. K., Rothwax, J., Shakir, N., Okoro, C., Raskolnikov, D., Parnes, H. L., Linehan, W. M., Merino, M. J., Simon, R. M., Choyke, P. L., Wood, B. J., & Pinto, P. A. (2015). Comparison of MR/ultrasound fusion-guided biopsy with ultrasound-guided biopsy for the diagnosis of prostate cancer. JAMA, 313(4), 390–397. https://doi-org.proxy.library.ju.se/10.1001/jama.2014.17942
Svensk förening för röntgensjuksköterskor. (2011). Kompetensbeskrivning för legitimerad röntgensjuksköterska. http://www.swedrad.se/f_start/
Svensk förening för röntgensjuksköterskor. (2008). Yrkesetisk kod för röntgensjuksköterskor. http://www.swedrad.se/f_start/
Tangel, M. R., & Rastinehad, A. R. (2018). Advances in prostate cancer imaging. F1000Research, 7. https://doi-org.proxy.library.ju.se/10.12688/f1000research.14498.1
*Tonttila, P. P., Lantto, J., Pääkkö, E., Piippo, U., Kauppila, S., Lammentausta, E., Ohtonen, P., & Vaarala, M. H. (2016). Prebiopsy Multiparametric Magnetic Resonance Imaging for Prostate Cancer Diagnosis in Biopsy-naive Men with Suspected Prostate Cancer Based on Elevated Prostate-specific Antigen Values: Results from a Randomized Prospective Blinded Controlled Trial. European Urology, 69(3), 419–425. https://doi-org.proxy.library.ju.se/10.1016/j.eururo.2015.05.024
Tortora, G., & Derricksson, B. (2015). Introduction to the human body (10th ed.). John Wiley & Sons Inc.
*van der Leest, M., Cornel, E., Israël, B., Hendriks, R., Padhani, A. R., Hoogenboom, M., Zamecnik, P., Bakker, D., Setiasti, A. Y., Veltman, J., van den Hout, H., van der Lelij, H., van Oort, I., Klaver, S., Debruyne, F., Sedelaar, M., Hannink, G., Rovers, M., Hulsbergen-van de Kaa, C., & Barentsz, J. O. (2019). Head-to-head Comparison of Transrectal Ultrasound-guided Prostate Biopsy Versus Multiparametric Prostate
31
Resonance Imaging with Subsequent Magnetic Resonance-guided Biopsy in Biopsy-naïve Men with Elevated Prostate-specific Antigen: A Large Prospective Multicenter Clinical Study. European Urology, 75(4), 570–578. https://doi-org.proxy.library.ju.se/10.1016/j.eururo.2018.11.023
*Washino, S., Kobayashi, S., Okochi, T., Kameda, T., Konoshi, T., Miyagawa, T., Takayama, T., & Morita, T. (2018). Cancer detection rate of prebiopsy MRI with subsequent systematic and targeted biopsy are superior to non-targeting systematic biopsy without MRI in biopsy naïve patients: a retrospective cohort study. BMC Urology, 18(1), 51. https://doi-org.proxy.library.ju.se/10.1186/s12894-018-0361-4
32
Bilagor
Bilaga 1-Granskningsprotokoll
Protokoll för basala kvalitetskriterier för studier med kvantitativ metod
Titel: Författare: Årtal: Tidskrift:
Del I.
Beskrivning av studien
Beskrivs problemet i bakgrund/inledning? Ja Nej Kunskapsläget inom det aktuella området är Ja Nej beskrivet?
Är syftet relevant till ert examensarbete? Ja Nej
Är urvalet beskrivet? Ja Nej
Samtliga frågor ska besvaras med ja för att artikeln ska inkluderas till fortsatt granskning. Vid Nej på någon av frågorna ovan exkluderas artikeln.
Del II
Kvalitetsfrågor
Hänger metod och syfte ihop? Ja Nej
(Kvantitativt syfte – kvantitativ metod)
Beskrivs statistiska metoder/analys? Ja Nej
Beskrivs datainsamlingen? Ja Nej
Beskrivs etiskt tillstånd/förhållningssätt/ Ja Nej ställningstagande?
Diskuteras metoden mot kvalitetssäkringsbegrepp validitet och reliabilitet i diskussionen? Ja Nej Diskuteras huvudfynd i resultatdiskussionen?
Ja Nej
Sker återkoppling till nyare forskning i relation till huvudfynden i diskussionen?
33 Är resultatet relevant för ert syfte?
Om ja, beskriv:
……… ……… ………
Om nej, motivera kort varför och exkludera artikeln:
……… ……… ……… Forskningsmetod/-design (t ex RCT, tvärsnittsstudie) ………. ……… Deltagarkarakteristiska Antal……… Ålder……….... Man/Kvinna………. Granskare sign: ……….