Examensarbete, 15 högskolepoäng, magisterexamen i
Omvårdnad inom Specialistsjuksköterskeprogrammen
Jönköping, juni 2018
Jönköping University
Hälsohögskolan, Avdelning för omvårdnad Box 1026, 551 11 JÖNKÖPING
Preoperativ
näringsdryck och
postoperativt
obehag
FÖRFATTARE: Anne-Marie Karlsson
- En randomiserad studie vid gastric
bypasskirurgi hos kvinnliga patienter
Nursing Science, Thesis, One year Master
15 Credits
Jönköping, June 2018
Jönköping University School of Health and Welfare Box 1026, SE-551 11 JÖNKÖPING
AUTHOR: Anne- Marie Karlsson
Preoperative
nutritional drink and
postoperative
discomfort
- A randomized study in gastric bypass
surgery in female patients
Sammanfattning
Bakgrund: Fetma är ett ökande problem i dagens samhälle. Laparoskopiskt Gastric bypass (LGBP)
utförs för att hjälpa personer med fetma till viktminskning och det är vanligt att dessa patienter upplever postoperativt illamående, buksmärta och huvudvärk efter ett operativt ingrepp. Det råder meningsskiljaktigheter i tidigare studier hur väl preoperativ näringsdryck kan ha ett samband gällande det postoperativa förloppet.
Syfte: Syftet var att jämföra tre olika preoperativa dryckers effekt på postoperativt illamående,
buksmärta och huvudvärk efter LGBP under de 24 första timmarna.
Metod: En randomiserad studie med kvantitativ design utfördes på en av Nordens största kliniker inom
fetmakirurgi. Totalt tillfrågades n=90 kvinnor och tilldelades slutna kuvert med antingen kolhydratdryck, proteindryck eller kranvatten.
Resultat: Illamående toppade ca åtta timmar efter operation, det vill säga kl.19.00 på kvällen, för att
sedan under natten återgå till preoperativa värden uppmätta kl.06.00. Skillnad mellan kolhydratrik- och proteinberikadryck gav p= 0, 2046 och för kolhydratrikdryck och kranvatten p= 0.8722. Buksmärtan var som högst vid ankomst till uppvakningsavdelningen och stabiliserades två timmar senare och minskade något under natten men försvann inte helt. Huvudvärk låg stabilt i alla grupperna med en ökning runt kl. 19:00 på kvällen för att sedan plana ut under natten. Inga skillnader mellan buksmärta och huvudvärk, p= 0,1569. Det sågs ingen statistisk signifikans hos någon av grupperna i de olika variablerna.
Slutsats: Preoperativ vätskebehandling med kolhydratdryck, proteindryck eller kranvatten inför en
LGBP operation påverkar inte signifikant illamående, buksmärta och huvudvärk efter operation.
Summary
Background: Obesity is a growing problem in today’s society. Laparoscopic Gastric bypass is
performed to help people with obesity lose weight and it is common for these patients to experience postoperative nausea, stomach pains, and headaches after a surgical procedure. There are differences in opinion in earlier studies as to the extent that preoperative nutritional beverages can correlate to the postoperative process.
Aim: The aim of this paper was to compare three different preoperative beverages’ effect on
postoperative nausea, stomach pains, and headaches after LGBP during the first 24 hours after surgery.
Method: A randomised study of quantitative design was performed on one of the Nordic countries’
largest clinics specializing in obesity surgery. A total tally of n=90 women were asked to participate and each received sealed packages containing either carbohydrate beverage, protein beverage, or tap water.
Results: Nausea peaked eight hours after surgery, at 7.00 PM, and then returned during the night to
preoperative values measured at 6.00 AM. The difference between the carbohydrate and protein beverages is expressed as p=0.2046, and the difference between the carbohydrate beverage and the tap water is expressed as p=0.8722. Stomach pains peaked at arrival to the recovery ward and stabilized two hours later, followed by a slight drop-off during the night but without subsiding entirely. Headache was experienced at stable values in all groups, with some increase at 7.00 PM only to level out during the night. There were no differences between stomach pains and headaches, as expressed by p=0.1569. No statistical significance was observed in any group in the different variables.
Conclusion: Preoperative fluid treatment with carbohydrate beverages, protein beverages, or tap
water before a LGBP surgery does not significantly affect nausea, stomach pain, or headache after the surgery.
Innehållsförteckning
Inledning ... 1
Bakgrund ... 1
Gastric bypass ... 1
Postoperativt illamående, buksmärta och huvudvärk ... 2
Postoperativ Omvårdnad - Sjuksköterskans roll ... 3
Omvårdnadsteori och personcentrerad vård ... 3
Syfte ... 4
Material och metod ... 4
Design och Setting ... 4
Urval ... 4 Datainsamling ... 4 Mätinstrument ... 5 Dataanalys ... 5 Etiska överväganden ... 6
Resultat ... 6
Diskussion ... 9
Metoddiskussion ... 10 Resultatdiskussion... 10Slutsatser ...12
Kliniska implikationer ...12
Referenser ...13
Bilagor
Bilaga 1. Patientinformation
1
Inledning
Fetma är ett ökande problem i dagens samhälle och antalet patienter som genomgår laporoskopisk Gastric bypass (LGBP) kirurgi har ökat i antal (Näslund, 2011). Postoperativ vård i detta sammanhang fokuseras mot vanliga komplikationer som illamående och kräkningar, smärta och huvudvärk (Fagerberg & Odenstedt Herges, 2016; Valeberg, 2016a). Illamående och kräkningar kan bero på flera orsaker, men ofta har smärta och kirurgiska ingrepp samt vätskestatus ett samband postoperativt (a.a.). Patienter med fetma som genomgår laparoskopisk bukkirurgi har mer illamående efter ett kirurgiskt ingrepp, detta på grund av ökad fettvävnad vilket leder till längre duration av anestesiläkemedel samt på grund av den koldioxid som används för visualiseringen vid laparaskopi (Lee, Lee, Lim & Chang, 2015: Thompson, 1999). LGBP -patienter har oftast kalori- och vätskereduktion under LCD-dieten ca 3-4 veckor innan operation för att minska risken för kirurgiska komplikationer. I tidigare studier med liknande design har patienter som gjort laporoskopisk cholecystectomi och elektiv kirurgi visats att preoperativ uppvätskning med kolhydratrik dryck inför operation har mått bättre postoperativt genom minskat illamående (Hausel, Nygren, Thorell, Lagerkranser, Ljungqvist, 2005;Yilidiz, Gunal, Yilmaz & Yucel, 2013). Däremot har det i Awad, Varadhan, Ljungqvist och Lobo (2012) studie visats att sambandet mellan kolhydratrik dryck preoperativt och postoperativt illamående har låg evidens. Utifrån detta forskningsläge vill författaren jämföra olika preoperativa drycker. Ger preoperativt intag av kolhydratdryck, proteindryck och kranvatten postoperativ effekt på variablerna illamående, buksmärta och huvudvärk? Detta för att ny forskning kan ge bättre förståelse hos sjuksköterskan som därmed kan bedriva en individanpassad personcentrerad vård och därmed öka förutsättningarna för att skapa postoperativt välbefinnande hos LGBP-patienterna.
Bakgrund
Gastric bypass
Enligt Global Health Observatory (GHO) visar statistik att ca 2,8 miljoner människor i världen avlider årligen på grund av fetma och detta fortsätter att öka. Idag anses fetma vara ett av världens allvarligaste hälsoproblem och i Sverige betecknas detta som en folksjukdom och utgör ett stort problem både för individen och för hälso- och sjukvården (Statistiska centralbyrån, 2012). Body Mass Index [BMI] är ett mått som används över hela världen för att räkna ut en persons undervikt respektive övervikt. BMI räknas fram genom att dela kroppsvikten i kg med kroppslängden i meter i kvadrat (kg/m2). Utifrån BMI definieras undervikt som BMI < 18,5, normalintervallet är 18,5-25, övervikt 25-29,5 och därefter klassificeras fetma i tre steg, Klass I 30-34,9, Klass II 35-39,5 och Klass III ≥40 (Nuttall, 2015). Gastric bypass (GBP) uppkom från Edward E. Mason, University of Iwoa, som upptäckte att patienter med magsår som avlägsnat en del av magsäcken gick ner i vikt (American Society fot Metabolic and Bariatric Surgery, 2005; Medicine Alumni Society, 2007). Det gjorde att Mason fick idén att hjälpa patienter med fetma till viktminskning med samma metod då det begränsade patientens matintag. Under 1960-talet utfördes de första operationerna, men metoden utvecklades senare då flera patienter fick problem med gallreflux. Den nya metoden hindrade galla komma upp i matstrupen genom att låta en del av tarmen anslutas till magsäcken (Medicine Alumni Society, 2007). GBP operationer utförs i största möjlig mån laparoskopiskt, men i vissa fall krävs öppen kirurgi (American Society for Metabolic and Bariatric Surgery, 2005). Operationen går ut på att göra magsäcken mindre, ca 97-99 % av magsäcken tas bort så att endast 1-3 % av magsäcken används för att ta emot föda (Aleris, 2016; Järhult & Offenbartl, 2013). Första tredjedelen av tunntarmen kopplas bort så att näringsupptaget sker i den nedre delen av tunntarmen och den lilla magen kopplas till tarm som finns längre ner i tarmkanalen. Näringsämnena koncentreras till den del av tarmen som signalerar mättnad vilket gör att patienten snabbt får en mättnadskänsla vid matintag (Järhult & Offenbartl, 2013).
Den metod som används mest frekvent i Sverige när det gäller fetmakirurgi är LGBP (Järhult & Offenbartl, 2013). Fördelen är att det sker en snabb viktminskning de första sex månaderna efter operationen och efter ca 24 månader har i regel målvikten uppnåtts och stabiliserats (American Society for Metabolic and Bariatric Surgery, 2005). Fetmakirurgin utvecklas konstant och blir allt vanligare och övervägande patienter är kvinnor (Näslund, 2011). År 2002 utfördes ca 700 operationer och redan 2010 hade denna siffra ökat till ca 8000 operationer årligen (a.a.).
2
Förutom förbättrad livskvalitet, ökad rörlighet och förbättrat subjektivt utseende kan många patienter även botas från sin diabetes, hypertoni, höga kolesterolnivåer samt hjärt- och kärlsjukdomar
(Richardsson, Plaisance, Periou, Buguoi & Tillery, 2009; American Society for Metabolic and Bariatric Surgery, 2005). Trots många fördelar finns det en hel del att tänka på efter en LGBP. GBP är inte viktminskande i sig, utan är snarare ett effektivt hjälpmedel. Det krävs även en livsstilsförändring med mindre matportioner och motion. Det är viktigt vad patienten äter för slags mat och för att förhindra brist på näringsämnen måste patienten ta näringstillskott (a.a.).
Enligt Howard och Ashleys (2003) studie visades det att välnutrierade patienter vanligtvis klarar kirurgiska ingrepp bättre och har mindre komplikationer och återhämtar sig snabbare efter en operation. Tidigare var nattlig fasta inför elektiv kirurgi en rutin men under åren har detta ändrats och idag får patienterna klara drycker 2-3 timmar före anestesistart. Orsaken är att minska den stress- framkallande insulinresistensen vilken kan medföra postoperativa komplikationer och långsammare återhämtning (a.a.). Studier visar att kolhydratdryck två till tre timmar före anestesistart vid elektiva operationer startar ämnesomsättningen och ger en metaboliska snabbare återhämtning, bättre välmående och en tidigare hemgång (Ljungqvist, 2004; Yilidiz et al., 2013). Patienter som genomgår bukkirurgi så som LGBP-patienter har ofta mer illamående efter ett operativt ingrepp än andra grupper (Fagerberg & Odenstedt Herges, 2016; Valeberg, 2013).
Postoperativt illamående, buksmärta och huvudvärk
Illamående och smärta är två av de vanligaste problemen i det postoperativa förloppet (Allvin, Ehnfors, Rawal, Svensson & Idvall, 2009; Fagerberg & Odenstedt Herges, 2016; Valeberg, 2016a). Av alla patienter som får generell anestesi drabbas 20-25% av illamående, och högst risk löper unga, icke-rökande kvinnor med benägenhet för åksjuka samt efter vissa användningar av anestesiläkemedel (Valeberg, 2016a). Vad som orsakar postoperativt illamående är inte klarlagt, men det är känt att opioder och anestesigaser samt kirurgiska orsaker som operationstyp och smärta ligger bakom (Fagerberg & Odenstedt Herges, 2016; Valeberg, 2016a; Pimenta & de Auguilar-Nascimento, 2014). Det har visats att vätskebehandling tycks kunna minska illamående vid större och mindre ingrepp och merparten av illamående och kräkningar inträffar under det första dygnet och inom två timmar efter operation (Valeberg, 2016a). Illamåendet i sig är inte livshotande men det kan framkalla kräkningar som kan leda till aspirationspneumoni och dehydrering (Valeberg, 2016b). Förutom att patienten får en negativ och obehaglig upplevelse, har det visats sig att utskrivningen från den postoperativa avdelningen fördröjs. Postoperativt illamående förebyggs främst med adekvat smärtlindring och tillförsel av oxygen samt måttlig höjd huvudända (a.a). Vid postoperativt illamående och kräkningar ökar även smärta (Fagerberg & Odenstedt Herges, 2016). Det har visats i studier att flera patienter upplever måttlig till svår smärta efter operation (Dolin, Cashman & Bland, 2002;Fagerberg & Odenstedt Herges, 2016), och förutom det lidande det innebär för patienten finns risken för uppkomst av kronisk smärta (Fagerberg & Odenstedt Herges, 2016). Vid postoperativa skeendet har patienterna ökad risk för illamående och kräkningar samt smärta (Fagerberg & Odenstedt Herges, 2016).
Buksmärta kan trigga fram eller förvärra illamåendet om den förblir obehandlad (Valeberg, 2016b). De flesta patienterna får som värst smärta det första postoperativa dygnet och därefter minskas den gradvis. Smärta är en subjektiv upplevelse och det är endast patienten som kan säga att smärtlindringen är tillräcklig (a.a.). Det har i en studie visats att förväntningarna av smärta berodde på hur patienten trodde smärtlindringen skulle uppnås, en del förväntade sig snabb lindring medan andra förväntade sig effekt om flera timmar (Eriksson, Wikström, Fridlund, Årestedt & Broström, 2016). Patienterna beskrev en osäkerhet runt hur mycket smärta de förväntades hantera och när de skulle våga fråga om mer smärtlindring (a.a.). På den postoperativa avdelningen ska en individuell plan göras och det ska finnas minst två smärtstillande läkemedel med olika verkningsmekanismer som ska kombineras, vilket i sin tur ger bättre smärtlindring och mindre biverkningar (Fagerberg & Odenstedt Herges, 2016; Valeberg, 2013). Vid smärtskattning med visuell analog skala (VAS) bör det i vila eftersträvas att patienten skattar under fyra på skalan (Fagerberg & Odenstedt Herges, 2016; Valeberg, 2013; Wikström, Eriksson, Fridlund, Årestedt & Broström, 2015). Genom att följa och registrera smärtskattningar underlättas fortsatt mobilisering och smärtlindring (a.a.). Det har även visats att av ca 60 % av de som opereras, däribland för LGBP, upplever huvudvärk i det postoperativa skedet (Fagerberg & Odenstedt Herges, 2016). Det har däremot inte identifierats någon särskild mekanism som orsakar huvudvärken efter generell anestesi (a.a.).
3
Postoperativ Omvårdnad - Sjuksköterskans roll
Sjuksköterskan ansvarar för och leder omvårdnadsarbetet både självständigt, i team och i partnerskap med patienterna och dess närstående (Svensk sjuksköterskeförening, 2017). Sjuksköterskan ska bedöma hälsotillstånd, prioritera och planera omvårdnaden, utföra samt utvärdera omvårdnadsåtgärder. Sjuksköterskan ska i partnerskap med patienten och dess närstående skapa delaktighet och samtidigt se till att värdighet och integritet bevaras (a.a.). På den postoperativa avdelningen sker patientens återhämtning och här övervakas patienten med övervakningsutrustning efter operationen. Under den postoperativa perioden är det viktigt att sjuksköterskan är noggrann och uppmärksam på eventuella komplikationer (Järhult & Offenbartl, 2013), både med hjälp av den kliniska blicken men även med hjälp av skattningsskalor (Wikström et al., 2015). Sjuksköterskans uppgift är även att finnas tillhands för patienten vid såväl fysiska som psykiska behov, som exempel smärta, illamående eller oro (Holm & Hansen, 2000a; Järhult & Offenbartl, 2013). Den postoperativa perioden börjar när patienten rullas ut från operationssalen och avslutas vid utskrivning från sjukhuset (Holm & Hansen, 2000b) och målet är att patienten ska bli återställd samt återfå hälsa (Allvin, Berg, Idvall & Nilsson, 2007). Patienter som vårdas på den postoperativa avdelningen är oftast beroende av vårdpersonalen och därför är sjuksköterskan omvårdnadsarbete viktigt för att skapa självständighet hos patienten (a.a.). På grund av övervakningen kan miljön uppfattas som stressande för patienten, och i många fall är ljudnivån från medicinsk utrustning ett störande moment i återhämtningen (Johnson, Raymond & Goss, 2012). Den postoperativa återhämtningen definieras som en energikrävande process med målet att återvända till normalt tillstånd (Allvin et al., 2009). Det har bland annat visats att effektiv behandling gällande smärtlindring är en förutsättning för postoperativa återhämtningen, likaså att undvika illamående vilket är ett stort problem och en viktig fråga för postoperativa patienter som LGBP- patienter (a.a.). Det har visats att sjukvårdspersonalens attityd och förståelse har en avgörande faktor gällande patienternas förmåga att klara smärta och därmed återhämtning (Eriksson et al., 2016). En del patienter upplevde att de blev förstådda och uppskattade att sjukvårdspersonal uppmanade dem till att ta smärtstillande läkemedel, medan andra inte verkade förstå patientens behov. Patienterna kunde då känna en rädsla att komma i konflikt med sjukvårdspersonal och ses som en olägenhet varav de inte ville störa personalen. Att visa respekt och vänlighet ger patienterna möjlighet att våga beskriva sin smärta och leder till bättre återhämtning (a.a.). En väletablerad väg för förbättrad återhämtning för bl.a. LGBP-patienter är att efter operation följa protokollet Enhanced recovery after surgery (ERAS), (Hauges, Coolsen, Aahlin, Harrison, McNally, Deon, Lassen & Wigmore, 2015). Protokollet ska överbrygga barriärerna mellan teamen från preoperativ, till peroperativa och till sist den postoperativa vården. En studie som undersökt ERAS-protokollet vid mag- och tarmkirurgi visade att både patienter och sjukvårdspersonal skattade frihet från illamående samt frihet av smärta i vila som de två viktigaste punkterna (a.a.).
Omvårdnadsteori och personcentrerad vård
Omvårdnadsforskningens syfte är att utveckla vården till det bättre genom att finna nya metoder och omvårdnadsåtgärder (Svensk sjuksköterskeförening, 2017). Genom att låta patienter och närstående beskriva sina upplevelser kan vården lättare främja individens hälsa och välbefinnande (a.a.). Upplevelser och erfarenheter skapar ett partnerskap mellan patienten och sjuksköterskan och är en del i den personcentrerade vården (Ekman & Norberg, 2016).
Sjuksköterskan på den postoperativa avdelningen har till uppgift att lindra, bota, stödja samt hjälpa patienten med dess basala omvårdnadsbehov (Svensk sjuksköterskeförening, 2017). En omvårdnadsteoretiker som tar upp just om detta är Virginia Henderson (1967) som beskriver om människans behov. Henderson (1967) menar att oavsett om människan är frisk eller sjuk, har han eller hon grundläggande behov. Hon har identifierat 14 komponenter som hon anser är grundläggande åtgärder och som ingår i allmän omvårdnad, däribland att äta och dricka, och därmed minska illamående och kräkningar. Sjuksköterskans arbetsuppgift är att hjälpa en individ att utföra sådana åtgärder som befordrar hälsa och tillfrisknande. Arbetsuppgifterna ska utföras på ett sätt som hjälper individen att så snart som möjligt återvinna sitt oberoende. För varje komponent finns omvårdnadshandlingar, en del kan sjuksköterskan själv ta initiativ till, medan andra ordineras av läkare. Henderson (1967) menar att sjuksköterskan ska träda in när individen behöver stödjande och ersättande åtgärder, men även ge patientundervisning i samråd med läkaren. Därav menar hon att det inte ska göras alltför stora gränsdragningar mellan omvårdnaden och den medicinska behandlingen, då de många gånger är överlappande (a.a.).
4
Den personcentrerade vården innebär att sjuksköterskan sätter patienten och i detta fall LGBP- patienten i fokus och utgår från var och ens individuella behov (Ekman & Norberg, 2016; Svensk sjuksköterskeförening, 2016). Förutsättningen är att sjuksköterskan har en vilja och ett intresse av patienten för att kunna ge den vård och omsorg han eller hon behöver för att kunna ge ökat välbefinnande och ökad delaktighet (a.a.). För att skapa delaktighet krävs det att patienten har kunskap och fått information (Svensk sjuksköterskeförening, 2017), något även Henderson (1967) menar är viktigt för att kunna främja hälsa. Att ge anpassad information till patienterna kräver att sjuksköterskan kontinuerligt uppdaterar sig om ny kunskap och kritiskt granskar forskning för att kunna optimera patientens välmående (Svensk sjuksköterskeförening, 2017). Då det i studier råder meningsskiljaktighet kring sambandet mellan preoperativt näringsdryck och postoperativt obehag görs därmed denna undersökning om olika preoperativa drycker har effekt för patientens välmående postoperativt.
Syfte
Syftet var att jämföra tre olika preoperativa dryckers effekt på postoperativt illamående, buksmärta och huvudvärk efter LGBP under de 24 första timmarna.
Material och metod
Design och Setting
Studien har en kvantitativ design och är en randomiserad studie. En randomiserad studie är när deltagarna slumpmässigt väljs till den behandling som ska utredas (Billhult, 2017a). Där jämförs förändringen mellan grupper som fått olika behandlingar, vilket anses vara det mest tillförlitliga sättet (a.a.). Patienterna randomiserades till tre olika behandlingsgrupper, till att preoperativt dricka kolhydratdryck, proteindryck eller kranvatten
.
Studien gjordes på en av Nordens största kliniker inom fetmakirurgi. Kliniken har operationsdelen på ett centralsjukhus i södra Sverige och en mottagningsdel som ligger i sydvästra delen av Skåne. Resursmässigt har kliniken även samarbete med Skånes Universitetssjukhus och Länssjukhus i Blekinge. Det opereras ca 1000 patienter årligen för LGBP på kliniken, varav 70 % är kvinnor och 30 % män. Datainsamlingen skedde våren 2013 och studien färdigställdes hösten 2013.Urval
Inklusionskriterierna var kvinnor mellan 18-65 år, som skulle förstå och tala svenska samt ha gett sitt samtycke till att delta i studien. Alla deltagarna skulle genomgå en LGBP och alla stod på en preoperativ lågkaloridiet 3 veckor innan operation. Samtliga skulle ha inställelsetid kl. 08:00 på operationsdagens morgon och opererades mellan 09:00-11:30. Exklusionskriterier var kvinnor med diabetes, rökare samt kvinnor med tidigare postoperativt illamående eller åksjuka. Baserat på en tidigare pilotstudie genomfördes en poweranalys med möjlighet att upptäcka en kliniskt signifikant skillnad på mer än 10 VAS-enheter. Totalt var det 90 kvinnor som skulle delta i studien. Ett internt bortfall på 18,8% (n=17) gjorde att studien erhöll 81,2% (n= 73) kompletta dataset. Bortfallet berodde på att fyra stycken deltagare ändrade sin operationstid till eftermiddagen, 13 stycken klarade inte av att dricka eller följa det orala intaget.
Datainsamling
Deltagarna tillfrågades muntligen av sjuksköterskan på mottagningen om medverkan till studien vid första besöket, 3 månader innan operationsdag och gav vid detta tillfälle medgivande eller icke medgivande. Efter skriftligt informerat samtycke randomiserades och tilldelades kvinnorna slutna kuvert och fick antingen kolhydratrik-, proteinberikad dryck eller kranvatten (Bilaga 1). Notering gjordes i operationsprogrammet gällande inställelsetid och medverkan i studien och patienten fick instruktioner och i tillämpliga fall näringslösning. De instruerades att dricka 800 ml dagen innan operation mellan kl.17:00 och 24:00 och 400 ml operationsdagen mellan kl. 04:00 och 06:00 (Tabell 1). Kirurger, anestesipersonal och sjuksköterskor var blinda för vilken behandling som hade blivit given. Patienterna fick rutinmässigt 2 g Alvedon peroralt, 8 mg Betapred intravenöst och 120 mg Arcoxia peroralt preoperativt och hade alla identisk anestetisk teknik under operation med Propofol samt Fentanyl intravenöst. Inga anestesigaser användes under operation och alla patienterna erhöll samma
5
buktryck (18 mmHg). Vid operationens slut gavs rutinmässigt 10 mg Ketogan, Catapresan 22,5 mg och Atrakurium 20 mg intravenöst. Alla patienter opererades före lunch och fick 1500-2000 ml Ringer- acetatlösning intravenöst under 24-30 timmar postoperativ sjukhustid.
Alla data dokumenterades på ett separat formulär. Tre variabler (illamående, buksmärta och huvudvärk) registrerades på 100 mm VAS var fjärde timme under 22 timmar. Sjuksköterskor på uppvaknings- och vårdavdelningen utförde mätningar och första mätningen gjordes preoperativt kl.08.00 operationsdagens morgon. Postoperativt tillbringade patienterna två timmar på uppvakningsavdelningen, där de vanligtvis mottog injektion Rapifen 0,5-1 mg och Dridol 0,5 mg intravenöst. Därefter överfördes patienterna till avdelningen. På avdelningen fick de 1 g Alvedon var 6: e timme. Kompletterande medicinering gavs om patienterna fick VAS > 30 för illamående eller smärta och erbjöds då ytterligare medicinering. Vid illamående gavs 0,5 mg Dridol eller Ondansetron 2 mg och för smärta 10 mg Ketogan intravenöst. All sådan ytterligare medicinering registrerades, om det administrerades. Alla patienterna i studien genomgick en okomplicerad LGBP och gick hem dagen efter.
Tabell 1. Vätskeintag pre och post operativt för de patienter som deltog i studien.
Dagen innan operation
Operationsdagen
Kranvatten
800 ml vatten
400 ml vatten
Kolhydratrik dryck
4 flaskor preoperativt
2 flaskor preoperativt
Proteinberikad
dryck
800 ml vatten med 10 dosmått
Atkins-pulver
400 ml vatten med 5 dosmått
Atkins-pulver
Mätinstrument
Visuell analog skala (VAS) är en smärtskattningsskala som vanligtvis är i skala 0-10 (Katz & Melzack, 1999; Vårdhandboken, 2018). VAS skalan kan användas inom flera områden och har använts i andra studier för att mäta illamående efter anestesi och har visats vara signifikant likvärdig med andra skalor som är numeriska och verbala (Boogaerts, Vanacker, Seidel, Albert & Bardiau, 2000;Li, Xueqin & Keela, 2007). I denna studie modifierades graderingen från 0-10 till 0-100 för att mäta illamående, buksmärta och huvudvärk. Anledningen till att skalan modifierades var att göra det visuellt enkelt och tydligt för patienterna. I nationella riktlinjer för rörelseorganens sjukdomar anges att VAS skalan 0-100 är tillämpbart (Socialstyrelsen, 2018). Det innebar att patienterna markerade någonstans på ett 100 mm streck vad de kände avseende illamående och smärta. En markering längst till vänster betydde ”Inget obehag” och en markering längst till höger betydde “Det värsta du kan föreställa dig”. VAS skalan är ett känt mätinstrument bland sjuksköterskor och övrig vårdpersonal och är lätthanterligt för patienten och enligt Polit och Beck (2012a) användbar för att mäta subjektiva upplevelser så som smärta, trötthet och andnöd.
Dataanalys
Innan dataanalys påbörjades gicks allt materialet igenom för att kontrollera så att ingen notering gjorts gällande avvikande medicinering eller dylikt, och allt noterades som skulle kunna påverka studiens resultat. Data registrerades slutligen i Excel-format, och statistiska bearbetningar gjordes med Winstat for Excel TM. Kontinuerliga variabler analyserades och då de var normalfördelade användes Student t-test. Student t-test bygger på t-fördelning, testet är parametrisk analysmetod och kraven på normalfördelning gäller för den variabel som ska analyseras och lika varians mellan grupperna. Om variablerna inte var normalfördelade skulle Mann-Whitney U-test användas. P-värden < 0.05 ansågs i studien vara statistiskt signifikanta (Billhult, 2016b; Eljertsson, 2003a).
6
Etiska överväganden
Studien ansågs kunna bidra till kunskapsinhämtning och kunskapsspridning inom området samt lindra patientens lidande efter operativt ingrepp. De etiska principerna respektprincipen, göra gott principen och rättviseprincipen har beaktats i studien (Kjellström, 2017). Respektprincipen har följts genom att patienternas frivillighet och autonomi har beaktats. Göra gott principen har följts genom att dels vinnlägga sig om att inte skada patienterna genom val av drycker, dels att syftet med studien är att uppnå ett bättre postoperativt mående för patienterna. Rättviseprincipen slutligen, genom att alla hade möjlighet att inkluderas i studien utifrån de valda kriterierna. Information till patienterna, individuellt samtycke och etikprövning gjordes enligt Etikprövningslagen (SFS 2003:460; Kjellström, 2017) och studien har godkänts av Lunds universitets etiska kommitté, EPN Lund avd. 2 (dnr: 2009/53, dnr:2012/407) som är en av de sex regionala etikprövningsnämnderna som finns i Sverige (Kjellström, 2017). Studien har utförts efter samtycke från alla deltagare i enlighet med principerna om Helsingforsdeklarationen som är en välkänd riktlinje med fokus på medicinsk klinisk forskning och utarbetades av World Medical Association [WMA]. Helsingforsdeklarationen uppdateras kontinuerligt och en av de bärande idéerna i denna riktlinje är att balansera behovet av ny kunskap gentemot deltagarnas hälsa och intresse. Enligt denna riktlinje bör all forskning granskas av oberoende personer för att avgöra om studieplanen är etisk (WMA, 2013; Kjellström, 2017).
Patienterna i denna studie blev informerade om att de när som helst kunde avbryta deltagandet i studien och alla informerades muntligt samt skriftligt och fick skriva på ett samtyckesavtal. Allt material analyserades och deltagarna avidentifierades i statistikprogrammet vilket gör att det inte går att härleda till vilka patienterna är annat än genom en separat inlåst kodlista. Allt material samlades in och sammanställdes och har därefter behandlats på dator med lösenordsskydd.
Resultat
I studien ingick 90 patienter ursprungligen efter samtycke. I bortfallsanalysen hade fyra patienter ändrat sin operationstid till eftermiddagen, 13 patienter hade inte följt protokollet för oralt intag; två stycken som skulle intagit kranvatten, sju stycken som skulle tagit proteindryck och fyra stycken som skulle intagit kolhydratdryck. Bortfallet var inte annorlunda mellan grupperna (p = 0,2821).
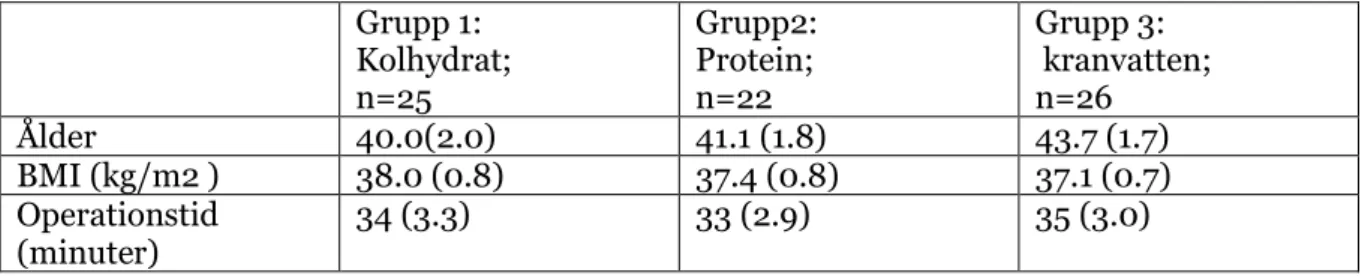
För återstående 73 patienter som deltog i studien slutfördes alla operationer laparoskopiskt och ingen aspiration vid intubation registrerad. Den genomsnittliga operationstiden var kort och likvärdig (Tabell 2).
Tabell 2: Beskrivning av patientgrupperna; medelvärde (SD).
Grupp 1:
Kolhydrat;
n=25
Grupp2:
Protein;
n=22
Grupp 3:
kranvatten;
n=26
Ålder
40.0(2.0)
41.1 (1.8)
43.7 (1.7)
BMI (kg/m2 )
38.0 (0.8)
37.4 (0.8)
37.1 (0.7)
Operationstid
(minuter)
34 (3.3)
33 (2.9)
35 (3.0)
Samtliga patienter hade normal återhämtning och skrevs ut från sjukhuset dagen efter operationen, och ingen patient återvände. Förekomsten av riskfaktorer för illamående skilde sig inte mellan grupperna (data ej visad). Behovet av ytterligare injektioner av medicinering (medelvärde) utanför av protokollet var 2,3 (0,2) injektioner för smärta och 1,7 (0,1) för illamående med ingen signifikant skillnad mellan grupperna i någon variabel.
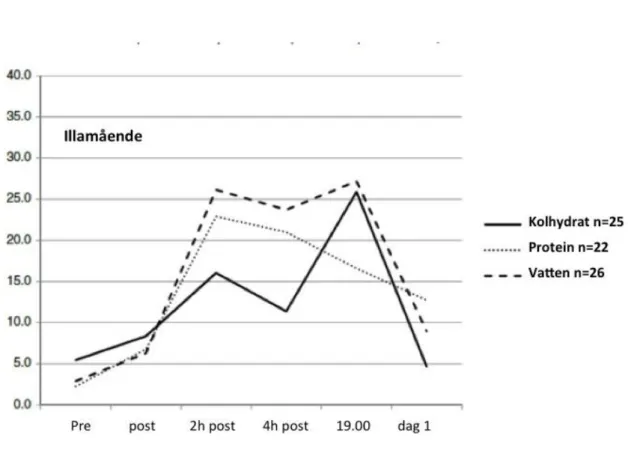
Det högst skattade värdet för illamående sågs ca åtta timmar efter operationen, det vill säga klockan 19:00 (Figur 1), utan skillnader mellan grupperna; skillnaden mellan kolhydratdryck och proteindryck gav p = 0,2046 och för kolhydratdryck och kranvatten gav p = 0,8722. Illamåendet försvann över natten och var inte annorlunda än de preoperativa värden klockan 06:00 på den första postoperativa morgonen. För resultat avseende buksmärta noterades toppvärden vid ankomsten till uppvakningsavdelningen, men förblev stabil efter två timmar till klockan 19:00 och minskade sedan
7
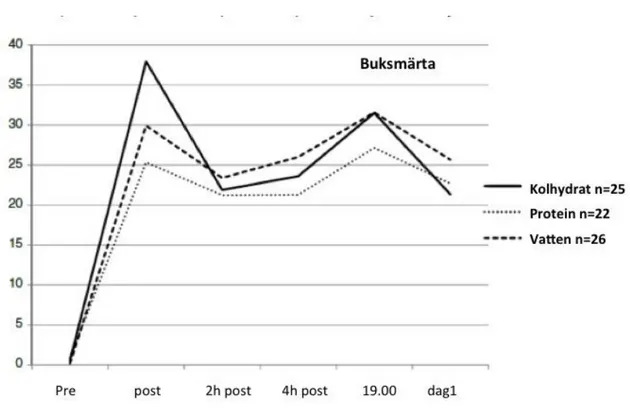
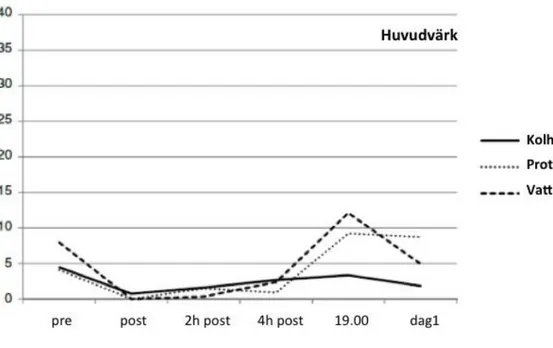
något men försvann inte över natten (Figur 2). Vad det gäller huvudvärk fanns inga signifikanta skillnader (Figur 3; p = 0,1569).
Figur 1: VAS-poäng (mm VAS-skala), som visar illamående för de tre patientgrupperna. Ingen statistiskt signifikant skillnad mellan grupperna identifierades vid någon tidpunkt. Maximalt möjligt värde var 100; Y-axeln formaterad till samma skala som i alla andra figurer. Dag 1= kl. 06:00 dagen efter operation.
8
Figur 2: VAS-poäng (mm VA-skala), som visar nivåer av buksmärta för de tre grupperna. Inga skillnader mellan grupperna identifierades vid någon tidpunkt. Maximal möjligt värde är 100; Y-axeln formaterad till samma skala som i alla andra figurer. Dag 1= kl. 06:00 dagen efter operation
9
Figur 3: VAS-poäng (mm VAS-skala), som visar nivåer av huvudvärk för de tre patientgrupperna. Inga skillnader mellan grupperna identifierades vid någon tidpunkt Maximalt möjligt värde är 100; Y-axeln formaterad till samma skala som i alla andra figurer. Dag 1= kl. 06:00 dagen efter operation.
Även om det inte fanns några signifikanta skillnader beroende av dryck kunde man ändå se tendenser så till vida att de som erhöll kolhydratdryck preoperativt upplevde mindre illamående (2 och 4 timmar efter operation) och huvudvärk (kl.19.00).
10
Diskussion
Metoddiskussion
Designen på studien var en randomiserad studie med en kvantitativ metod vilket ansågs bäst passa till studiens frågeställningar (Polit & Beck , 2012a; Billhult, 2017a). Att använda sig av kvantitativ metod ansågs som bästa metoden för att få fram statistik samt strukturerade data från ett större urval. Studien utfördes enbart på en specialistklinik som enbart opererar LGBP, och ses som en styrka då peroperativa- och postoperativvård var likvärdig, liksom att det var samma anestesimetod och specialistkirurg vid varje operation.
Det är fler kvinnor som genomgår en kirurgisk LGBP och därför inkluderades endast kvinnor för att hålla hög validitet, och de tillfrågades av samma sjuksköterska om medverkan till studien (Lincoln & Guba, 1985). Hade män inkluderats hade kanske resultatet blivit annorlunda med ojämn fördelning vid randomiseringen. Att det var samma sjuksköterska som informerade om studien till alla deltagare stärker validiteten då informationen blev likvärdig (Lincoln & Guba, 1985). Hade olika sjuksköterskor informerat finns det risk att informationen hade varit olika till deltagarna och att tonläget och kroppsspråk hade skiljt sig mellan sjuksköterskorna, något som hade sänkt validiteten Att exkludera kvinnor med diabetes berodde på att resultatet kunde bli missvisade om blodsockernivåerna skulle variera avsevärt och ev. risken för illamående skulle påverkas. Totalt blev det ett bortfall på 18,8% (n=17) och kanske berodde det på att kvinnorna inte förstått informationen de hade fått eller personliga skäl. Men då deltagarantalet var 81,2% anses det inte sänka studiens validitet.
Mätningarna gjordes under sex tillfällen och under samma tidpunkter och utfördes av sjuksköterskor från uppvaknings- och vårdavdelningen. Risken är, när flera personer är inblandade i mätningarna, är den mänskliga faktorn som kan spela en viss roll, bl.a. tonfall, hur frågan ställdes samt tolkningen på svaret (Lincoln & Guba, 1985). Andra faktorer som kan påverkat var t. ex patientens kroppsställning, såsom sängliggande, satt upp eller var uppegående vid mätningen. Det kan i efterhand ses som en svaghet att flera personer var inblandad i mätningarna, det gick dock inte att göra på något annat sätt då mätningarna skulle göras under hela dygnet.
VAS-skalan användes med skalan 0-100 och är en skala för smärtskattning (Katz & Melzack, 1999; Vårdhandboken, 2018). Innan studien framkom att detta instrument var lätthanterligt för patienterna. Skalan modifierades till 0-100 för att få större spridning och tydlighet. Nu i efterhand kan detta instrument diskuteras och om det eventuellt fanns andra mätinstrument som hade kunnat användas istället. Det ansågs dock som lätthanterligt för både patienterna samt sjuksköterskorna på avdelningen att använda sig av samma mätinstrument vid mätningar av illamående, smärta och huvudvärk. VAS- skalan har även använts för patientbedömningar i likande studier (Hausel et al., 2005). Det ökar även reliabiliteten att använda sig av ett känt mätinstrument, då reliabilitet innebär att mätningen är tillförlitlig och fri från mätfel (Polit & Beck, 2012b).
För att öka reliabiliteten användes en känd klassisk analysmetod i form av Student T-test för att analysera variablerna (Billhult, 2017c; Polit & Beck, 2012b). Student T-test användes för att testa om skillnaden mellan normalfördelade grupper var signifikant (Eljertsson, 2003b; Polit & Beck, 2012c). En annan metod som skulle ha kunnat användas är ANOVA för jämförelser av normalfördelade kontinuerliga variabler, för tre eller fler oberoende grupper. Om inte variablerna vore normalfördelade skulle Kruskal-Wallis test för tre eller fler oberoende grupper ha kunnat användas (Polit & Beck, 2012c).
Resultatdiskussion
Syftet med studien var att undersöka om olika preoperativa drycker påverkar kvinnors upplevda obehag avseende illamående, buksmärta och huvudvärk efter LGBP under de första 24 timmarna efter operation. Resultatet visade att preoperativ näringsdryck vid LGBP inte ger någon påverkan på det postoperativa förloppet när det gäller illamående, buksmärta och huvudvärk. Det spelar ingen roll vilken av de tre dryckerna som intogs men det fanns tendens till att kolhydratdryck hade mer positiv effekt jämfört med de andra när det gäller illamående. Resultatet visar således att även om det inte fanns signifikanta skillnader så fanns en antydan i data (figur 1) att de som intog kolhydratdryck hade minskade besvär med illamående på uppvakningsavdelningen, men även vid mätningarna två och fyra timmar efter operation. Mätningen som gjordes på kvällen visade också att gruppen som fick proteindryck hade mindre besvär med illamående jämfört med de andra två grupperna. Hausel et al. (2005) undersökte i en randomiserad kontrollerad studie postoperativt illamående hos 172 personer
11
under en kort tid (12-24h). Där fann de en fördelaktig effekt gällande intag av preoperativ kolhydratdryck vid laporoskopisk gallblåsekirurgi (a.a.). I den här studien visades att varken kolhydratdryck, proteindryck eller kranvatten påverkade någon av variablerna som mättes postoperativt. Det är något som bekräftades i en studie av Lidder et al. (2013) som visade att patienterna varken mår bättre eller sämre med preoperativ näringsdryck. Något som även stärks i Asakura, Milhara och Goto (2015) samt Awad et al. (2012) studier där sambandet mellan kolhydratdryck preoperativt och postoperativt illamående hade låg evidens. Möjligen hade utfallet blivit mer uttalat om urvalet varit större, om vi mätt efter en längre operationstid eller annat kirurgiskt ingrepp. Att minska obehag som illamående har en fördel för patienten och för den postoperativa vården då postoperativt illamående hindrar patienterna från mobilisering samt återgång till oralt matintag (Douglas, Wilmore & Kehlet, 2001). Henderson (1967) beskriver i sin teori att sjuksköterskan måste se till patientens behov och ge stödjande samt ersättande åtgärder. Sjuksköterskan kan på egen hand ta initiativ till omvårdandshandlingar och hjälpa patienten med grundläggande åtgärder. För att lättare återvinna individens självständighet kan sjuksköterskan hjälpa patienten med att äta och dricka, vilket skulle bidra till minskat illamående och kräkningar. Hendersson (1967) teori går ut på att sjuksköterskans speciella arbetsuppgifter och funktion att hjälpa individen att utföra åtgärder som bidrar till tillfrisknad, åtgärder som patienten själv skulle kunna utföra om han eller hon hade haft stryka och kunskap. Resultaten går delvis i linje med en tidigare studie som visat att kolhydratdryck inför operation minskade det postoperativa illamåendet (Hausel, Nygren, Thorell, Lagerkranser, Ljungqvist, 2005;Yilidiz, Gunal, Yilmaz & Yucel, 2013). Dock är evidensen låg för att kolhydratdryck minskar postoperativt illamående (Awad, Varadhan, Ljungqvist och Lobo, 2012). Den kliniska betydelsen av resultatet är svårt att uttala sig om. Möjligen finns en tendens till att kolhydratdryck kan minska postoperativt illamående efter LGBP.
Ingen skillnad sågs mellan de tre dryckesgrupperna när det gällde buksmärta (figur 2). Buksmärtan hade högst uppmätt värde vid ankomst till uppvakningsavdelningen och det var genomgående i alla grupperna, men stabiliserades sedan efter två timmar fram till kvällen (kl.19.00). På kvällen (kl.19.00) kom det åter en topp hos alla grupperna för att sedan minskas något men försvann inte helt. Att alla tre dryckesgrupperna toppade sina värden i buksmärta vid ankomsten till uppvakningsavdelningen kan bero på dålig preoperativ smärtlindring. I studien ingick endast kvinnor och därför vet vi inte om resultatet kan ha varit könsbundet. I Hartwig, Allvin, Bäckström och Stenbergs (2017) studie studerades riskfaktorer för postoperativ smärta de första 24 timmarna efter LGBP. De frågade 192 personer, varav 71,4% var kvinnor och 28,6 var män, och det visade sig att kvinnor (48,9%) rapporterade en större andel tid med svår smärta (VAS 7-10) jämfört med män (34,5%) (a.a.). I en studie med 22 deltagare av Eriksson et al. (2015), vars syfte var att beskriva patientens handlingar och erfarenheter när det gällde beskriva smärta efter operation, visades det sig att många patienter inte vågade fråga om smärtstillande då de tyckte sjuksköterskorna var stressade. Det kan vara en anledning till att patienterna i den studien fick en smärttopp på kvällen, då det på kvällstid enbart arbetar en sjuksköterska och en undersköterska på avdelningen. Det har visats att smärtlindring och mobilisering har en positiv effekt på den postoperativa återhämtningen (Allvin et al., 2009). vilket gör att sjuksköterskan måste vara uppmärksam på patienten. Klinisk betydelse är att som sjuksköterska inse betydelsen av att veta att den postoperativa smärtan är subjektiv, och att skiljer sig mellan olika patienter. Detta stärks i Wood studie (2010) där han beskriver just subjektiv smärta och skillnader mellan olika individer.
Avseende huvudvärk (figur 3) sågs ingen signifikant skillnad mellan dryckesgrupperna under de första timmarna efter operation En intressant upptäckt var att huvudvärken uppstod först på kvällen (kl.19.00) och då sågs en ökad tendens hos dem som intagit proteindryck och kranvatten. Patientgruppen som drack kolhydratdryck hade mindre uttalade huvudvärk än de två övriga grupperna. Att huvudvärken toppade på kvällen (kl.19.00) skulle kunna förklaras med abstinens och avsaknad av koffeinintag. Studier som stärker detta är Shapiro (2007) som menar på i sin studie att vanligt förekommande symtom till huvudvärk är abstinens kopplat till koffein. I hans studie uppkom huvudvärk inom 24 timmar efter koffeinintag (a.a) Hade patienterna tillfrågats innan studien om de var kaffedrickare så kunde denna information varit av stort värde och betydelse för resultatet.
Det är viktigt att se varje individ som unik genom att bedriva personcentrerad omvårdnad (Ekman & Norberg, 2016; Svensk sjuksköterskeförening, 2016). Personcentrerad vård innebär att personen sätts i fokus framför sjukdomen, och att personen inte är sin sjukdom utan har en. Genom ömsesidig respekt för varandras kunskap kan ett partnerskap skapas och leda till ökat välbefinnande (Svensk sjuksköterskeförening, 2016). All behandling måste individ anpassas så även dryck intag (Mottram, 2009). För att kunna bedriva personcentrerad vård krävs det kunskap om personen och genom att
12
lyssna kan sjuksköterskan få en förståelse över patientens situation och därmed skapa delaktighet (Svensk sjuksköterskeförening, 2016), vilket kan göra att patienten återgår till normalt tillstånd fortare. Även om resultatet inte visar på någon statistisk signifikans mellan någon av grupperna avseende postoperativt obehag som illamående, buksmärta och huvudvärk är det av stor vikt att bemöta patienterna som unika individer och att deras upplevelser varierar efter LGBP operation.
Kvinnorna i den här studien kunde dagen efter operation gå hem utan några komplikationer. Kanske är det så att LGBP utförs på ett sådant skonsamt sätt, genom korta operationstider och personcentrerad postoperativ vård, att preoperativ näringsdryck inte ger någon påverkan på det postoperativa förloppet. Att korta operationstider har god effekt på de postoperativa faktorerna stöds även av en studie av Thompson (1999). Han beskriver att korta operationstider, där mindre anestesiläkemedel ges, gör att durationen av läkemedlet är kortvarig vilket leder till mindre illamående postoperativt och gör att tidigare mobilisering med personal kan ske. Hjälp med mobiliseringen, som Henderson (1967) menar är en omvårdnadshandling leder också till minskad smärta och patientens oberoende så att hemgång kan ske.
Slutsatser
Den här randomiserade studien visar att preoperativ dryck med kolhydratdryck, proteindryck eller kranvatten vid LGBP inte verkar ge någon påverkan på det postoperativa förloppet avseende illamående, buksmärta och huvudvärk hos kvinnor de första 24 timmarna efter LGBP. Det fanns dock tendenser i resultatet som visade att kolhydratdryck kunde minska illamående och huvudvärk. Alla kvinnor kunde gå hem dagen efter operation utan vidare åtgärder. Illamående, buksmärta och huvudvärk är subjektiva upplevelser som varje sjuksköterska måste beakta. Genom att aktivt uppdatera sig om forskningsläget och bedriva personcentrerad omvårdnad kan det postoperativa välbefinnandet ökas hos alla patienter som genomgår ett kirurgiskt ingrepp.
Kliniska implikationer
Genom den här studien får sjuksköterskan en ökad kunskap att preoperativ dryck av olika slag inte har ett samband med postoperativt obehag avseende illamående, buksmärta eller huvudvärk hos kvinnor efter LGBP operation. Henderson (1967) menar att sjuksköterskan ständigt ska tolka och förstå patientens kroppsliga och känslomässiga behov för att bl. a. upptäcka smärta, lindra och trösta. Omvårdnaden och den medicinska behandlingen går därmed ihop många gånger och är viktiga utgångspunkter för en välfungerande vård. Det hade varit intressant om liknande studie hade gjorts på kvinnliga patientgrupper med andra kirurgiska ingrepp för att se om resultat blir likvärdigt. Tankar som har uppkommit är varför ingen forskning har genomförts på enbart män? Beror det på att det är mindre antal män som genomgår LGBP än kvinnor? För att mäta skillnaderna mellan män och kvinnor hade en sådan studie varit intressant för att se så inte könsbundna och sociala faktorer spelar in. Studiens resultat har bidragit till att skapa en insikt i att preoperativ dryck inte gav någon effekt gällande postoperativt obehag på denna patientgrupp, vilket kan vara av intresse för andra LGBP-kliniker i Sverige och i övriga världen. Vi ska dock även ta hänsyn till att operationsteknik och anestesimetod kan variera på olika kliniker runt om i världen. Vid framtida forskning bör forskaren beakta att många faktorer kan påverka patientens postoperativa obehag efter operation. Det är också av stor vikt att se till hela människan, båda fysiskt som psykiskt mående postoperativt, för att på så sätt öka patientens välbefinnande och göra omvårdnaden mer personcentrerad.
13
Referenser
Aleris. (2016). Patientinformation Gastric Bypass. Hämtad 2018-05-17, från
https://www.alerisplastikkirurgi.se/globalassets/se-obesitas/obesitas/14-patientinfo_gbp-2017_stockholm.pdf
Allvin, R., Berg, K., Idvall, E., & Nilsson, U. (2007). Postoperative recovery: a concept analysis. Journal of Advanced Nursing, 57(5), 552-558.
Allvin, R., Ehnfors, M., Rawal, N., Svensson, E., & Idvall, E. (2009). Development of a questionnaire to measure patient-reported postoperative recovery: a content validity and intra-patient reliability. Journal of Evolutation in Clinical Practice, 15, 411-419. doi:10.1111/j.1365-2753.2008.01027.x
American Society for Metabolic and Bariatric Surgery. (2005). Brief History and Summary of Bariatric Surgery Chapter 3. Tillgänglig: https://asmbs.org/resources/story-of-obesity-surgery (2018-04-03). Apfel, C.C., Heidrich, F.M., & Jukar-Rao, S. (2012). Evidence-based analysis of risk factors for postoperative nausea and vomiting. British Journal Anaesthesia. 109(5), 742–53. doi:10.1093/bja/aes276.
Asakura, A., Milhara, T., & Goto, T. (2015). The Effect of Preoperative Oral Carbohydrate or Oral Rehydration Solution on Postoperative Quality of Recovery: A Ranomised Controlled Clinical Trial. PloS ONE, 10(8), 1-11.
Azagury, D.E., Ris, F., Pichard, C., Volonté, F., Karsegard, L., & Huber, O. (2014).
Does perioperative nutrition and oral carbohydrate load sustainably preserve muscle mass after bariatric surgery? A randomized control trial. doi: http://dx.doi.org/10.1016/j.soard.2014.10.016. Awad, S., Varadhan, K., Ljungqvist, O., & Lobo, D. (2012). A meta-analysis of randomised controlled trials on properative oral carbohydrate treatment in elective surgery. Clinical Nutrition, (32), 34-44. Awada, SKK., Ljungqvist, O., & Loboa, DN. (2013). A meta-analysis of randomised controlled trials on preoperative oral carbohydrate treatment in elective surgery. Clinical Nutrition, 32(1), 34–44.
Billhult, A. (2017a). Kvantitativ metod och stickprov. I M. Henricson (Red.). Vetenskaplig teori och metod: Från idé till examination inom omvårdnad. (2:2. Uppl., s. 99-110). Lund: Studentlitteratur AB. Billhult, A. (2017b). Analytisk statistik. I M. Henricson (Red.). Vetenskaplig teori och metod: Från idé till examination inom omvårdnad. (2:2. Uppl., s. 275-283). Lund: Studentlitteratur AB.
Billhult, A. (2017c). Mätinstrument och diagnostiska test. I Henricson, M. (Red.). Vetenskaplig teori och metod: Från idé till examination inom omvårdnad. (2:2. Uppl. s. 133-141). Lund: Studentlitteratur AB. Boogaerts, J.G., Vanacker, E., Seidel, L., Albert, A., & Bardiau, F.M. (2000). Assesment of postoperative nausea using a visual analogue scale. Acta Anaesthesiologica Scandinavia, 44(4), 470-474.
Dolin, SJ., Cashman, JN., & Bland JM. (2002). Effectiveness of acute postoperative pain management: I. Evidence from published data. British Journal Anaesthesia, 89(3), s. 409-423.
Douglas, W., Wilmore, DW., & Kehlet, H. (2001). Management of patients in fast track surgery. BMJ. 2001;322:473. doi:10.1136/bmj.322.7284.473.
Ekman, I., & Norberg, A. (2016). Personcentrerad vård- teori och tillämpning. I Edberg, AK., Ehrenberg, A., Friberg, F., Wallin, L., Öhlen, J. (Red.). Omvårdnad på avancerad nivå-kärnkompetenser inom sjuksköterskans specialistområden. (1,5. Uppl., s. 29-53). Lund: Studentlitteratur.
Eljertsson, G. (2003a). Vad är en hypotesprövning? Statistik för hälsovetenskaperna. (1. Uppl., s. 127 -142). Lund: Studentlitteratur.
Eljertsson, G. (2003b). Statistisk analys av kvantitativa variabler- två studiedesigner. Statistik för hälsovetenskaperna. (1.Uppl., s. 201 -220). Lund: Studentlitteratur.
14
Eriksson, K., Wikström., L., Fridlund, B., Aårestedt, K., & Broström, A. (2016). Patients experiences and actions when describing pain after surgery- A critical incident technique analysis. International Journal of Nursing Studies, 56, 27-36. doi: 10.1016/j.ijnurstu.2015.12.008.
Fagerberg, A., & Odenstedt Herges, H. (2016). Postoperativ vård. I S. Lindahl, O.Winsö & J. Åkeson (Red.). Anestesi. (3. Uppl., s. 338-348). Stockholm: Liber AB.
Global health observatory (GHO). (2018). Obesity, situations and trends. Hämtad 2018-04-25, från http://www.who.int/gho/ncd/risk_factors/obesity_text/en/
Hartwig, M., Allvin, R., Bäckström, R., & Stenberg, E. (2017). Factors Associated with Increased Experience of Postoperative Pain after Laparoscopic Gastric Bypass Surgery. Obesity Surgery, 17, 1854- 1858. doi: 10.1007/s11695-017-2570-4.
Hausel, J., Nygren, J., Thorell, A., Lagerkranser, M., & Ljungqvist O. (2005). Randomized clinical trial of the effects of oral preoperative carbo- hydrates on postoperative nausea and vomiting after laparoscopic cholecystectomy. The British Journal of Surgery, 92(4), 415–21. doi: 10.1002/bjs. 4901. Henderson, V. (1967). The nature of nursing. New York: The Macmillan Company.
Holm, S., & Hansen, E. (2000a). Postoperativ övervakning/omvårdnad på vårdavdelning. Pre- och postoperativ omvårdnad. (1. Uppl., s. 89 -102). Lund: Studentlitteratur.
Holm, S., & Hansen, E. (2000b). Övervakning av patient i början av den postoperative perioden. Pre- och postoperativ omvårdnad. (1. Uppl., s. 57 -88). Lund: Studentlitteratur.
Howard, L., & Ashley, C., (2003). Nutrition in the perioperativ patient. Annual Review of Nutrition, (23), 263-282.
Hughes, M., Coolsen, M., Aahlin, E., Harrison, E., McNally, S., Dejong, C., Lassen, K., & Wigmore, S. (2015). Attitudes of patients and care providers to enhanced recovery after surgery programs after major abdominal surgery. Journal of Surgical Research, 193(1), 102-110. doi: 10.1016/j.jss.2014.06.032. Johnson, B., Raymond, S., & Goss, J. (2012). Perioperative music or headsets to decrease anxiety. Journal of Perioperative Anesthesia Nursing, 27, 146-154.
Järhult, J., & Offenbartl, K. (Red.). (2013). Sjukdomar i matstrupe, magsäck, tolvfingertarm och tunntarm. Kirurgiboken Vård av patienter med kirurgiska, urologiska och ortopediska sjukdomar (5. Uppl., s. 264 - 288). Liber: Stockholm.
Katz, J., & Melzack, R. (1999). Measurement of pain. Surgical Clinics of North America, 79(2), 31-252. Kjellström, S. (2017). Forskningsetik. I M. Henricson (Red.). Vetenskaplig teori och metod: Från idé till examination inom omvårdnad. (2:2. Uppl., s. 57-80). Lund: Studentlitteratur AB.
Lee, W., Lee, K., Lim, S., & Chang, Y. (2015). Comparison of palonosteron granisetron and ramosetron for the prevention of postoperative nausea and vomiting after laparoscopic gynecologic surgery: a prospective randomized trial. BMC Anesthesiology, 15 (121), 1-5.
Li, L., Xueqin, L., & Keela, H. (2007). Postoperative Pain Intensity Assessment: A Comparison of Four Scales in Chinese Adults. Pain Medicine, 8(3), 223-234.
Lidder, P., Thomas, S., Flemming, S., Hosie, K., Shaw, S., & Lewis, S. (2013). A randomized placebo controlled trial of preoperative carbohydrate drinks and early postoperative nutritional supplement drinks in colorectal surgery. Colorectal Disease, 15(6), 737-746. doi: 10.1111/codi.12130.
Lincoln, Y. S., & Guba, E. (1985). Naturalistic Inquiry. Beverly Hills, Kalifornien, USA: Sage Publishing. Ljungqvist, O. (2004). To fast or not fast? Metabolic preparation for elective surgery. Scandinavian Journal of Nutrition, 48(2), 77-82.
15
Medicine Alumni Society. (2007). Edward Mason, M.D. The University of Iwoa. Hämtad 2018-04-02, från http://healthcare.uiowa.edu/alumni/interviews/mason_edward.html
Mottram, A. (2009). Therapeutic relationships in day surgery a grounded theory study. Journal of Clinical Nursing, 18, 2830-2837.
Nuttall, F.Q. (2015). Body Mass Index- Obesity, BMI and Health: A Critical Review. Nutrition Today, 50(3), 117-128. doi: 10.1097/NT.0000000000000092
Näslund, I. (2011). Accelererande utveckling av Obesitaskirurgi i Sverige. Läkartidningen, 49(108), 2574-2577.
Pacelli, F., Bossola, M., Rosa, F., Tortorelli, A.P., Papa, V., & Doglietto, G.B. (2008).
Is malnutrition still a risk factor of postoperative complications in gastric cancer surgery? Clinical Nutrition, 27(3), 398–407.
Petry, N.M., Barry, D., Pietrzak, R., & Wagner, J.A. (2008). Overweight and Obesity Are Associated with Psychiatric Disorders: Results from the National Epidemiologic Survey on Alcohol and Related Conditions. Psychosomatic Medicine, 20(3), 288-297. doi: 10.1097/PSY.0b013e3181651651.
Pimenta, G.P., & de Auguilar-Nascimento, J.E. (2014). Prolonged Preoperative Fasting in elective Surgical Patients: why Should We Reduce It? Nutrition in Clinical Practice, 29(1), 22-28.
Polit, D.F., & Beck, CT. (2012a). Data Collection in Quantitative Research. Nursing research: Generating and Assessing Evidence for Nursing Practice. (9. Uppl., s. 293 - 327). Philadelphia: Wolters Kluwer Health.
Polit, D.F., & Beck, C.T. (2012b). Measurement and Data Quality. Nursing research: Generating and Assessing Evidence for Nursing Practice. (9. Uppl., s. 328 - 350). Philadelphia: Wolters Kluwer Health. Polit, D.F., & Beck, C.T. (2012c). Inferential Statistics. Nursing research: Generating and Assessing Evidence for Nursing Practice. (9. Uppl., s. 404 - 432). Philadelphia: Wolters Kluwer Health.
Richardsson, W., Plaisance, A., Periou, L., Buguoi, J., & Tillery, D. (2009). Long-term Management of Patients After Weight Loss Surgery. The Ochsner Journal, 9(3), 154-459.
Scott, K.M., Bruffaerts, R., Simon, G.E., Alonso, J., Angermeyer, M., de Girolamo, G., Demyttenaere, K., … von Korff, M. (2008). Obesity and mental disorders in the general population: results from the world health surveys. International Journal of Obesity, 32(1), 192-200.
SFS 2003:460. Lagen om etikprövning av forskning som avser människor. Stockholm: Utbildningsdepartementet. Hämtad 2018-04-05, från Riksdagen
https://www.riksdagen.se/sv/dokument-lagar/dokument/svensk-forfattningssamling/lag-2003460-om-etikprovning-av-forskning-som_sfs-2003-460
SFS 2014:821. Patientlagen. Hämtad 2018-05-09, från Riksdagen https://www.riksdagen.se/sv/dokument-lagar/dokument/svensk-forfattningssamling/patientlag-2014821_sfs-2014-821
Shapiro, R, E. (2007). Caffeine and headaches. Neurological Science, 28(2), 179- 183. doi: 10.1007/s10072- 007- 0773-5
Smith, M.D., McCall, J., Plank, L., Herbison, G.P., Soop, M., & Nygren, J. (2014). Preoperative carbohydrate treatment for enhancing recovery after elective surgery. Editorial Group: Cochrane Anaesthesia Group. doi: 10.1002/14651858.CD009161.pub2.
Socialstyrelsen (2018). Ordlista för Nationella riktlinjer för rörelseorganens sjukdomar. Hämtad 2018-06-07, från http://www.socialstyrelsen.se/nationellariktlinjerforrorelseorganenssjukdomar/ordlista Statistiska centralbyrån (2012). Vi växer på bredden. Hämtad 2018-04-25, från
16
Svensk sjuksköterskeförening. (2016). Personcentrerad vård. Stockholm: Svensk sjuksköterskeförening. Hämtad 2018-03-25, från https://www.swenurse.se/globalassets/01-svensk-
sjukskoterskeforening/publikationer-svensk-sjukskoterskeforening/ssf-om-publikationer/svensk_sjukskoterskeforening_om_personcentrerad_vard_oktober_2016.pdf
Svensk sjuksköterskeförening. (2017). Kompetensbeskrivning för legitimerade
sjuksköterskor. Stockholm: Svensk sjuksköterskeförening. Hämtad 2018-03-25, från
https://www.swenurse.se/globalassets/01-svensk-sjukskoterskeforening/publikationer-svensk- sjukskoterskeforening/kompetensbeskrivningar-publikationer/kompetensbeskrivning-legitimerad-sjukskoterska-2017-for-webb.pdf
Svensk sjuksköterskeförening. (2017). Forskning och utveckling. Stockholm: Svensk sjuksköterskeförening. Hämtad 2018-03-25, från rån https://www.swenurse.se/Vi-arbetar-med/Forskning-och-utveckling/
Thompson, H.J. (1999). The management of post-operative nausea and vomiting. Journal of Advanced Nursing, 29(5), 1130-1136.
Yildiz, H., Gunal, S.E., Yilmaz, G., & Yucel, S. (2013). Oral Carbohydate Supplemention Reduces Preoperative Discomfort in Laprascopie Cholecytectomy. Journal of Investigative Surgery, (26), 89-95. Valeberg, B. (2016a). Illamående och kräkningar. I I.L Hovind (Red.). Anestesiologisk omvårdnad. (2:2. Uppl., s. 117-126). Lund: Studentlitteratur AB.
Valeberg, B. (2016b). Rapportering och övervakning efter anestesi. I I.L Hovind (Red.). Anestesiologisk omvårdnad. (2:2. Uppl., s. 351-356). Lund: Studentlitteratur AB.
Vårdhandboken. (2018). Smärtskattningsinstrument. Hämtad 2018-03-26, från
http://www.vardhandboken.se/Texter/Smartskattning-av-akut-och-postoperativ-smarta/Smartskattningsinstrument/
Wikström, L., Eriksson, K., Fridlund, B., Årestedt, K., & Broström, A. (2015). Healtcare professionals descriptions of care experiences and actions when assesing postoperative pain- a critical incident technique analysis. Nordic College of Caring Science, 30, 802-812. https://doi.org/10.1111/scs.12308
WMA (2013). WMA Declaration of Helsinki - Ethical Principles for Medical Research Involving Human Subjects. Hämtad 2018-04-04, från
https://www.wma.net/policies-post/wma-declaration-of-helsinki-ethical-principles-for-medical-research-involving-human-subjects/
Wood, S. (2010). Post operative pain 1: Understanding the factors affecting patients' experiences of pain. Nursing Times, 106(45), 10-13.
17