Bestämning av ejektionsfraktion i
vila med ekokardiografi och
myokardscintigrafi
HUVUDOMRÅDE: Biomedicinsk laboratorievetenskap inriktning klinisk fysiologi FÖRFATTARE: Julia Dahl & Lisa Olander
HANDLEDARE:Sven-Åke Starck EXAMINATOR:Rachel De Basso JÖNKÖPING 2017 Maj
Sammanfattning
Myocardial Perfusion Imaging (MPI) och ultraljudskardiografi (UKG) är två viktiga metoder i utredningen av ejektionsfraktion (EF) i vänsterkammaren och tidigare studier har delade åsikter om EF korrelerar eller inte mellan flertalet undersökningsmetoder. Syftet var att jämföra om MPI och UKG skiljde sig åt i EF-bestämning i vila för patienter som genomgått undersökningarna under en tvåmånadersperiod på Länssjukhuset Ryhov i Jönköping. T-test för parvisa observationer användes för statistisk analys på de 91 individer som inkluderades i studien och som utfört såväl UKG som MPI år 2016. Resultatet visar att en statistisk signifikant skillnad i EF-bestämning föreligger för det totala urvalet (p<0,05). Ytterligare uppdelning av datamaterialet uppenbarade att kvinnor inte uppvisade en signifikant skillnad i EF-bestämning mellan de två metoderna och att en lättare kroppsvikt är en anledning till detta resultat. Hög ålder är en känd riskfaktor för hjärtsjukdomar med snabba degenererande tillstånd varvid åldersgrupper granskades ytterligare. Dessa hade dock ingen relevans för studiens slutresultat. Tidigare studier visar att ett mindre hjärta som mer frekvent förekommer hos kvinnor ger en överskattning av EF vid MPI och att användning av åtta bilder per hjärtcykel ger en underskattning av EF. Detta ligger till grund för att kvinnor inte uppvisade en skillnad i EF-bestämning.
Determination of ejection fraction at rest with echocardiography and myocardial perfusion imaging: A comparison of methods.
Summary
Myocardial Perfusion Imaging (MPI) and echocardiography (UKG) are two important methods for evaluating the ejection fraction (EF) in the left ventricular and previous studies have diverged opinions if EF correlates or not between several methods. The purpose was to compare if MPI and UKG differed in EF-determination at rest for patients examined during a two-month period at Länssjukhuset Ryhov in Jönköping. T-test for paired observations was used for statistical analysis on the 91 subjects included in the study, who performed both UKG and MPI in 2016. The result displays that there’s a significant difference in EF-determination for the total sample (p<0,05). Further division of the data revealed that women didn’t show a significant difference in EF-determination between the methods and that a lighter body weight is a reason for this outcome. High age is a risk factor for heart disease with rapid degenerative conditions, whereby age groups were further examined. Though without relevance to the final result. Previous studies showed that smaller hearts appearing more frequently in women gives an overestimation of EF at MPI and the use of eight frames per cardiac cycle gives an underestimation of EF. This is the reason women didn’t show a difference in EF-determination. Keywords: Gated SPECT, systolic left ventricular function, heart.
Innehållsförteckning
Inledning ... 1
Bakgrund ... 1
Ekokardiografi ... 2 Ultraljudsbildens uppbyggnad... 2 Ekokardiografiska snitt ... 3 Myokardscintigrafi ... 4 SPECT ... 4 Radiofarmaka ... 4 Undersökningspraxis ... 5 Hjärtcykeln ... 5 Ejektionsfraktion ... 6Syfte ... 8
Material och metod ... 9
Urval ... 9 Insamling av data ... 9 Ekokardiografi ... 10 Myokardscintigrafi ... 10 Statistiska beräkningar ... 10 Etiska överväganden ... 11
Resultat ... 12
Diskussion ... 16
Metoddiskussion ... 16 Resultatdiskussion ... 17Slutsatser ... 22
Omnämnanden ... 23
Referenser ... 24
Bilagor
1
Inledning
Myokardscintigrafi (Myocardial Perfusion Imaging (MPI)) och ekokardiografi (ultraljudskardiografi (UKG)) är två välkända metoder för utredning av hjärtats vänsterkammarfunktion och således även för bestämning av vänsterkammarens (Left Ventricular (LV)) ejektionsfraktion (EF) [1-2]. EF beskriver globalt den systoliska vänsterkammarfunktionen och definieras som den procentuella delen av den diastoliska kammarvolymen som pumpas ut via aorta under systole. Måttet anses kunna förutsäga sannolikheten för överlevnad vid flertalet hjärtsjukdomar och har en stor betydelse för fortsatt behandling [3-5]. EF mäts i procent (%) och avgörs av den slutdiastoliska- (End-diastolic Volume (EDV)) samt den slutsystoliska volymen (End-systolic Volume (ESV)). Genom både UKG och MPI är det möjligt att få ut ett mått på EF, via olika tekniker, som är en god grund för bedömning av hjärtats vänsterkammarfunktion. Indikationerna för respektive undersökning är många och vida varvid de båda har en viktig roll i utredningen av hjärtats friska eller sjuka tillstånd [1-2]. Önskvärt är att båda undersökningarna åstadkommer en EF-bestämning inom samma referensintervall för att inte, vid ena eller andra undersökningen, friskförklara en sjuk individ eller omvänt. Ytterligare studier kan vid behov utreda vilken undersökningsmetodik som korrelerar bäst med golden standard, hjärtresonanstomografi (Cardiac Magnetic Resonance (CMR) Imaging) [6-7], och varför det skiljer sig mellan de två metoderna.
Tabell 1. Vanligt förekommande förkortningar.
2
Bakgrund
Tidigare studier har granskat korrelationen mellan flertalet undersökningsmetoder för bestämning av EF. De metoder som jämförts har exempelvis varit UKG, MPI, CMR, vänsterventrikulografi och angiografi [4, 8-9]. Studier med fokus på bland annat MPI har utöver detta fördjupat sig i om patientens position vid insamling kan påverka EF, likväl som om programvaran som används för att utvinna EF kan påverka slutvärdet [9-10]. Studier har även diskuterat bestämning av EF på små hjärtan, där skillnad setts mellan UKG och MPI. MPI har enligt studier en tendens att överskatta EF vid små hjärtan [8, 11-12]. Åsikterna kring ämnet varierar där ena sidan menar att EF korrelerar mellan olika undersökningsmetoder och program för bestämning av EF [4, 8-9] medan andra studier istället anser det motsatta: det skiljer mellan undersökningsmetoder och program för bestämning av EF [9-10]. Eftersom en ovisshet förekommer kring om EF korrelerar eller inte och att värdet har en stor betydelse för utredning av vänsterkammarfunktionen, är det av relevans att utreda om EF skiljer sig åt mellan två utvalda metoder: MPI och UKG.
Ekokardiografi
Undersökning av hjärtat kan göras med UKG och är idag en av de viktigaste och vanligaste metoderna för att få information om bland annat storleken på hjärtrummen, myokardiets tjocklek, dess sammandragning samt om klaffapparaten [13]. Metoden är noninvasiv och således lämplig för utredning av den systoliska funktionen i LV och följaktligen även för att få ut mätvärdet EF [12]. Fördelar med metoden är att den är smärtfri, utan risk för patientbestrålning med joniserande strålning [3], flertalet indikationer kan utredas samt att det inte finns några direkta kontraindikationer. Nackdelar är dock att metoden kräver en viss erfarenhet av undersökaren för att exempelvis inte felprojicera de ekokardiografiska snitten, och undersökningen kan utöver detta vara belastande för utövaren. I vissa fall är det, trots erfarenhet, inte möjligt att genomföra en fullständig UKG-undersökning då patienten exempelvis är mycket överviktig eller har emfysem [13].
Ultraljudsbildens uppbyggnad
Metoden bygger på att ultraljud utsändes från en ultraljudsgivare uppbyggd av piezoelektriska kristaller vars funktion är att omvandla elektrisk energi till ljudenergi (ultraljud) vid utsändning och omvänd funktion vid mottagande. Ultraljudet definieras som en frekvens över 20,000 Hertz (Hz) som det mänskliga örat inte kan uppfatta. Grundläggande för att en bild blir till, är att det förekommer varierande densitet i vävnader i kroppen, vilket ger upphov till att ljudenergin, i
3
olika utsträckning, reflekteras beroende på hur stor skillnad som föreligger i densitet mellan vävnaderna. Vid tvådimensionell ekokardiografi (2DE) utsänds flertalet korta ljudpulser (ultaljudsvågor) i en bestämd riktning (ultraljudsstråle) och för att bygga upp en bild krävs det att åtskilliga ultraljudsstrålar utsänds i ett specifikt område. Reflektionspunkterna från varje stråle formateras på ultraljudsbilden i skiftande gråa nyanser, beroende på hur stark reflektion, varvid dessa tillsammans bygger upp en bild av det specifika området. När uppbyggnaden av en bild är färdigställd påbörjas en sammanställning av nästa bild och produkten blir en rörlig ekokardiografisk bild [1].
Ekokardiografiska snitt
Vad som kan studeras är beroende av vilket ekokardiografiskt snitt som har valts. Dessa snitt uppkommer genom en placering av ultraljudsgivaren i olika nivåer runt om hjärtat, tillsammans med en önskvärd vinkel mot det som ska betraktas. Med en transthorakal ekokardiografi (TTE) kan en apikal fyrkammarvy (four chamber (4C)) erhållas genom ett snitt skuret genom högra och vänstra kammarens centrala delar samt genom mitralis- och tricuspidalisklaffarna (Figur 1). Den apikala tvåkammarvyn (two chamber (2C)) framkommer vid rotation av ultraljudsgivaren från 4C varav vänster förmak, mitralisklaffen, apex och vänstra kammarens anteriora och inferiora vägg kan urskiljas (Figur 2). Dessa vyer används frekvent för att mäta EF genom Simpsons biplanmetod. Denna metod innebär att arean i LV mäts i både fyrkammar- och tvåkammarvy samt vid slutsystolisk- och slutdiastolisk volym [1].
4
Myokardscintigrafi
Vid undersökningen MPI är det hjärtmuskeln, det så kallade myokardiet, som undersöks. Patienterna tillhör en grupp med misstänkt kranskärlssjukdom (Coronary Artery Disease (CAD)) och inkommer vanligen med misstanke om myokardischemi. Undersökningsresultatet ger ett starkt prognostiskt värde för senare hjärtinfarkt eller hjärtdöd, vilket gör MPI mycket användbart för bedömning av hjärtats myokardperfusion och hjärtfunktion [2, 4, 8-10, 16].
SPECT
Vid Single-photon Emission Computed Tomography (SPECT) roterar gammakamerans detektor runt det studerade organet för att samla in en serie bilder ur olika vinklar. Detektorn utgörs av en natriumjodidkristall där ena sidan, med hjälp av fotomultiplikatorrör (PM-rör), registrerar den infallande fotonens energi samt var fotonen träffar kristallen [13, 17-19]. Kristallens frontsida täcks av en kollimator med vanligen parallella hål för att fotonerna som växelverkar i kristallen ska länkas med positionen för det radioaktiva sönderfallet i patienten. Parallellhålskollimatorn bestämmer vilka fotonriktningar som slutligen når kristallen [2, 18]. Växelverkan mellan foton och kristall genererar ljusblixtar (scintillation) som är proportionella mot energin i fotonerna varvid PM-röret omvandlar ljuset till elektriska impulser. Dessa impulser, med energi proportionell mot den infallna fotonen, analyseras genom att mäta impulsens spänning. De fotoner som faller inom ett accepterat energiintervall kan särskiljas från sekundära fotoner med lägre energi. De accepterade fotonerna gör det möjligt att utifrån det radioaktiva ämnets fördelning i det studerade organet erhålla en grafisk återgivning [13, 18-19]. Insamling av bilder kan ske på olika vis, däribland via tomografi, SPECT. Via rotation kan alltså tredimensionell information erhållas som vanligen presenteras som transversella snitt [2, 17, 19-20].
Radiofarmaka
MPI kräver en intravenös injektion av ett radioaktivt ämne, ofta teknetium-99m (99mTc), som med hjälp av en biologisk markör binder till myokardiet. De vanligaste använda perfusionsmarkörerna vid MPI är antingen tetrofosmin (Myoview) eller sestamibi (Cardiolite). Dessa markörer är monovalenta lipofila katjoner som medför passage in i cellerna genom passiv diffusion och kommer tas upp av mitokondrierna i cellerna. Upptaget av den radioaktiva isotopen är bland annat beroende av blodflödet och den elektrokemiska gradienten mellan plasma och mitokondrier, varav dessa faktorer avgör hur bra ämnet absorberas [2, 19, 21-22]. Av den totala injicerade aktivitetsmängden av tetrofosmin kommer ca 1,2 % [23] att tas upp av
5
hjärtat vid en undersökning, och frambringa en ögonblicksbild av myokardperfusionen vid injektionstillfället [19, 21-22].
Undersökningspraxis
Patienter som blir kallade till en MPI genomgår i regel två bildtagningar, en vid ansträngning (stress) och en i vila (rest), där båda är beroende av en intravenös injektion av det radioaktiva ämnet. Vid bildtagning av hjärtat i ett stressrelaterat tillstånd får patienten genomgå en farmakologisk provokation eller genomföra ett arbetsprov. En farmakologisk provokation innebär användning av ett vasodilaterande läkemedel på kranskärlen, exempelvis regadenoson (Rapiscan) [2, 20], och orsakar samma fysiska effekt som vedertagen ansträngningsprovokation [24]. Patienten blir vid bildtagning oftast uppkopplad med elektrokardiografi (EKG) med efterföljande bildtagning under ca 20 minuter. Genom uppkoppling med EKG, under SPECT, blir undersökningen synkroniserad eller gated (GSPECT), vilket innebär att bilder av hjärtcykelns olika delar kan erhållas. Ifall det noteras upptagsdefekter vid stresscintigrafin kallas patienten tillbaka för bildtagning i vila. Bildtagningarna vid vila och stress jämförs vid utvärdering, där bilderna rekonstrueras efter längs- och kortaxelsnitt i LV och en tvådimensionell summerad bild av hela LV erhålls (Bullseye-vy). Saknas upptagsdefekter vid stress avfärdar det indikation för ischemi och om hjärtats volymer dessutom är ordinära behöver inte en ytterligare bildtagning i vila ske [2, 19, 22, 25-26].
Hjärtcykeln
Kontraktionsfasen (systole) tillsammans med relaxationsfasen (diastole) utgör två moment som delar upp hjärtfunktionen, varvid vänster kammare är som mest uttänjd vid slutdiastole och som mest ihopdragen i slutsystole. Diastole tar sin början kort efter den isovolumetriska relaxationsfasen när trycket i vänster förmak, efter ett föregående hjärtslag, är högre än i vänster kammare och mitralisklaffen mellan de två hålrummen öppnas. Blodet flödar in i kammaren från förmaket i två omgångar där första delen strömmar ut direkt vid öppning och resterande mängd vid hjärtats förmakskontraktion. Kammaren kommer vid fyllnad att uppnå ett högre tryck än i förmaket vilket medför en stängning av mitralisklaffen som avslutar diastole. När kammarmyokardiet kontraherar i systole ökar trycket i hålrummet snabbt och aortaklaffen öppnas för att pumpa ut blod från hjärtat till övriga delar av kroppen. Kammaren kommer återigen att relaxeras med en följd av att aortaklaffen försluts och ett snabbt tryckfall i kammaren uppstår (isovolumetrisk relaxationsfas). Hjärtcykeln är fullbordad och en ny tar sin början [27-28].
6
Ejektionsfraktion
EF erhålls genom att slagvolymen (EDV-ESV) divideras med den diastoliska volymen, och beräknas med följande ekvation [1-2, 4, 9, 13, 29-30]:
EF (%) = [(EDV – ESV)/EDV] × 100
EF skattas utifrån uppnådd procentsats, där normal EF karakteriseras av ett värde >50 % medan 40-49 % innebär en lätt nedsatt systolisk vänsterkammarfunktion. Mellan 30-39 % föreligger en måttligt nedsatt EF och <30 % är EF uttalat nedsatt [30-31]. Flertalet tillstånd kan påverka EF, däribland hjärtinfarkt, behandling med cytostatika och undersökningsförhållanden. Hjärtinfarkt kan innebära allvarliga konsekvenser med försvagad pumpförmåga, sämre cirkulation, lägre blodtryck samt efterföljande vänsterkammarsvikt på grund av nekrotiserade myokardceller. EF kan därför snabbt påvisas lägre än tidigare med varierad sänkning beroende på infarktens utbredning [4, 32]. Vissa cytostatika är också känt, att vid behandling av cancersjukdomar, förorsaka försämrade hjärttillstånd med degenererad systolisk funktion och följaktligen även försämrad EF [3, 33]. En större kroppsvolym vid UKG är enligt Lang et al (2015) en bidragande faktor till förändrad EDV och ESV vilket således även influerar EF [34]. Med UKG kan vänsterkammarens ejektionsfraktion (Left Ventricular Ejection Fraction (LVEF)) uppskattas genom antingen en subjektiv visuell bedömning av vänster kammare, eller vid användning av den vanligaste metoden idag: Simpsons biplanmetod (Figur 3 & 4). Metoden bygger på en volymsberäkning av LV i både 2C och 4C genom en utlinjering av endokardiets konturer i EDV och ESV. Dagens ultraljudsutrustning har automatiska mätprogram som utför beräkning av LVEF utifrån flertalet principer, där mjukvaran, via Simpsons biplanmetod, delar in kammarvolymen i skivor/cylindrar. Skivornas volymer summeras varvid EF kan beräknas via ovanstående ekvation [1, 3-4, 13, 36-37].
7
För att få ut ett värde på den systoliska vänsterkammarfunktionen vid MPI används rutinmässigt s.k. EKG-triggning eller ”gating” [2, 19]. Med detta hjälpmedel kan bilder från de olika delarna av hjärtcykeln erhållas och med en automatisk utlinjering av konturerna på hjärtats endokardium kommer vänsterkammarvolymen över hjärtcykeln fås ut (Figur 5). Därigenom möjliggörs beräkning av EDV, ESV och EF [2, 8, 19, 36].
Figur 5. EF-bestämning vid MPI. Quantitative gated SPECT (QGS 2012) [38]. Figur 3 & 4. Utlinjering av endokardiet vid slutdiastolisk- och
8
Syfte
Studiens syfte är att jämföra om det föreligger en signifikant skillnad i EF-bestämning för patienter som genomfört en MPI och UKG i vila under en tvåmånadersperiod på Länssjukhuset Ryhov i Jönköping.
Nollhypotes (H0): EF skiljer sig inte åt mellan MPI och UKG.
9
Material och metod
Denna studie är retrospektiv och av kvantitativ ansats vars frågeställning har uppkommit vid Klinisk fysiologi på Länssjukhuset Ryhov i Jönköping. Artiklar har inhämtats från Pubmed och via databasen PRIMO från Jönköping University med hjälp av sökorden “myocardial perfusion imaging”, “ejection fraction”, “echocardiography”, “SPECT”, “gated SPECT”, “myocardial scintigraphy”, “aging and cardiovascular disease”, “BMI” och “single photon emission computed tomography”.
Urval
Populationen bestod av 527 patienter där alla under år 2016 utfört en MPI i vila på Länssjukhuset Ryhov i Jönköping. För att bli inkluderad krävdes det att patienten även genomgått en UKG-undersökning med som mest två månader mellan de två undersökningarna, vilket begränsade antalet till 94 stycken. Tvåmånadersperioden valdes för att inkludera ett tillräckligt stort antal patienter, men som förhoppningsvis inte hunnit genomgå behandling mellan undersökningarna som kan komma att påverka EF. Perioden valdes även för att minska risken att patientens hälsotillstånd reducerats avsevärt. Författarna till denna studie hade inte möjlighet att exkludera patienter som under tvåmånadersperioden fått ett avsevärt försämrat eller förbättrat EF, på grund av att patienternas journaler inte fanns tillgängliga. Däremot exkluderades ytterligare tre patienter vars MPI-undersökning inte var gated, varvid EF inte kunde bestämmas. Studien har inte orsakat extra kostnader eller ytterligare belastning för såväl patienter som personal då undersökningarna genomfördes enligt schema på kliniken av medicinska skäl.
Insamling av data
Insamling av data pågick under vecka 14 och 18, år 2017. En sammanställning av patienter som alla utfört MPI och UKG under föregående år, 2016, utlämnades tillsammans med tillhörande ålder, kön, undersökningsdatum och EF för UKG. Eftersom att EF från UKG redan fanns tillgängligt var tillvägagångssättet för insamling av måttet (automatisk eller manuell) okänt, men EF från MPI beräknades med den automatiska programvaran Quantitative Gated SPECT (QGS 2012, Cedars-Sinai Medical Center, Los Angeles CA, USA). Samtidigt erhölls information om vilken gammakamera som använts och vilket företag som står bakom produkten (Philips eller Siemens). Undersökningsdatum för de två metoderna var presenterade varav tid mellan undersökningarna kunde kontrolleras. Patienternas kroppsvikt hämtades under v. 18 med hjälp av det patientadministrativa systemet(PAF).
10
Ekokardiografi
Siemens Acuson SC2000 och tillhörande hjärtprob 4C1C användes på alla patienter för visualisering av de ekokardiografiska snitten under TTE-undersökningarna, och tre EKG-elektroder uppkopplades på samtliga. Patienten i sidoläge är att föredra för att underlätta åskådliggörande av hjärtat och ingår i metodbeskrivningen, dock är läget av patienten inget som kan säkerställas i denna studie. Programmet eSie Left Heart användes för automatiska beräkningar av EDV och ESV i 4C och 2C, vilket senare kunde korrigeras av utövaren vid behov, och lagring till digitala bilder skedde via systemet Syngo Dynamics (Siemens Medical Solutions, USA) [39]. Det fanns inte dokumenterat om den automatiskt beräknade EF via Simpsons biplanmetod var manuellt korrigerad eller inte.
Myokardscintigrafi
Två tvåhövdade gammakameror Philips Brightview (Philips Healthcare, The Netherlands) och Siemens ECAM+ (Siemens Medical Solutions USA) användes för tomografisk insamling av bilder (SPECT). Bildtagning i vila påbörjades ca 45 minuter efter intravenös injektion av 5,7 MBq av 99mTc-Tetrofosmin/kg kroppsvikt och inför bildtagning placerades patienten liggande med armarna ovanför huvudet, uppkopplad till EKG. Kollimatorer som användes var av lågenergi-högupplösande parallellhåltyp. Energifönstret sattes på 140 keV med ett acceptansfönster på 20 % för Philips och 19 % för Siemens med en asymmetri på 2 %. Tillhörande detektorer ställdes in till 90° (L-mode) för insamling av bilder. Detta skedde med åtta bilder per hjärtcykel på en zoom av 1,45 (Siemens) och 1,46 (Philips) vid rotation på 180° på detektorerna från höger snett framifrån 45° till vänster snett bakifrån 45°. Bilder togs i 32 vinklar under 30 sekunder per vinkel. Bildmatrisen som användes vid registrering var 64 x 64 pixel. Projektionerna som erhölls vid undersökning rekonstruerades sedan genom iterativ rekonstruktion (10 iterationer, 8 subsets) med postfiltrering Butterworth filter (order 10, cutoff 0,45) i programvaran Hybrid Recon (Hermes Medical Solutions, Stockholm, Sweden). Beräkning av global EF från det insamlade materialet gjordes i QGS (Cedars-Sinai Medical Center, Los Angeles, CA, USA) [2, 19, 21, 26].
Statistiska beräkningar
Vid de statistiska beräkningarna användes IBM Statistical Package for Social Science (SPSS) Statistics 21 (SPSS, Chicago, IL) med tillhörande T-test för parvisa observationer med beroende variabler. Urvalet ansågs normalfördelat på grund av ett antal >30 individer och vidare användes en signifikansnivå på 0,05 (α=0,05). Beräkningarna utfördes utifrån hela urvalet med
11
efterföljande indelningar av kön samt vikt- och åldersgrupper. Detta för att besvara om det fanns en statistisk signifikant skillnad mellan de två undersökningsmetoderna, och senare vilka indelningar som händelsevis påverkat utfallet. Vid beräkning av kön, vikt- och åldersgrupper användes Split file för att möjliggöra analysering av flera undergrupper. Minimum och maximum för ålder och dagar mellan undersökningstillfällena beräknades enligt One Way ANOVA och SPSS användes även för att sammanställa ett spridningsdiagram, med regressionslinje och konfidensintervall, utifrån skillnad i EF hos varje individ mellan de två undersökningsmetoderna.
Etiska överväganden
En etisk egengranskning har gjorts enligt School of Health and Welfare/Hälsohögskolans anvisningar (Bilaga 1). Inhämtning av personuppgifter godkändes av verksamhetschefen vid Klinisk fysiologi på Länssjukhuset Ryhov (Bilaga 2). Ett informerat samtycke ansågs inte väsentligt då data som låg till underlag för studien inhämtades från föregående år (2016) och författarna hade ingen personlig kontakt med de patienter som genomgått undersökningarna. Enskilda medicinska skäl låg till grund för att utredningarna genomfördes, varav ytterligare belastning och kostnad för patient som såväl personal besparades. All data avidentifierades vid statistiska beräkningar för att omintetgöra spårning av individerna som ligger till grund för studien.
12
Resultat
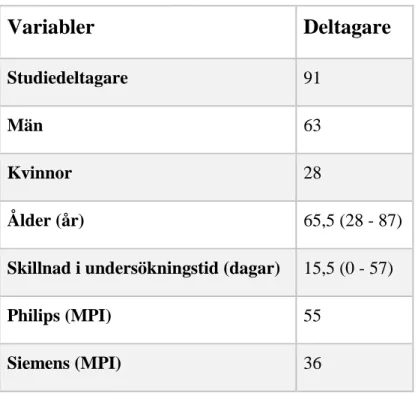
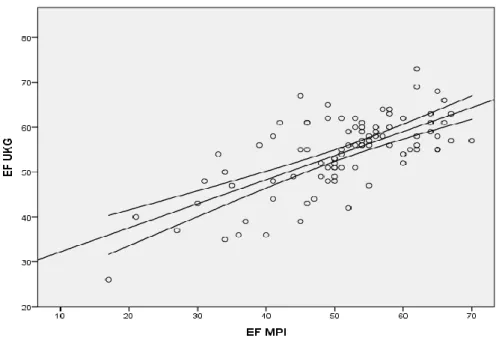
Av de 91 patienter som inkluderades var 63 män och 28 kvinnor med en ålder mellan 28 – 87 år. Alla patienter utförde undersökningarna inom tidsperioden på två månader (se Tabell 2 för fullständig demografi). En överskådlig visualisering av varje individs EF, erhållna från respektive undersökning, visar med hjälp av regressionslinjen ett linjärt samband mellan de två undersökningsmetoderna. Ett konfidensintervall på 95 % (0,95) användes, där en statistisk signifikant skillnad föreligger hos individer utanför intervallet (Figur 6). Ålder och vikt delades ytterligare upp i tre grupper med en spridning på 21 år respektive 21 kg inom varje grupp (Tabell 3 & 4).
Variabler
Deltagare
Studiedeltagare 91 Män 63 Kvinnor 28 Ålder (år) 65,5 (28 - 87)Skillnad i undersökningstid (dagar) 15,5 (0 - 57)
Philips (MPI) 55
Siemens (MPI) 36
Tabell 2. Studiedeltagare, män och kvinnor samt gammakameramärke presenteras i antal (st) medan ålder och dagar anges som medelvärde. Inom parentes återges spridningen (min-max).
13
Åldersgrupp (år) Antal Viktgrupp (kg) Antal Kvinnor Män 25-45 4 55-75 32 13 19
46-66 44 76-96 38 12 26
67-87 43 97-117 21 3 18
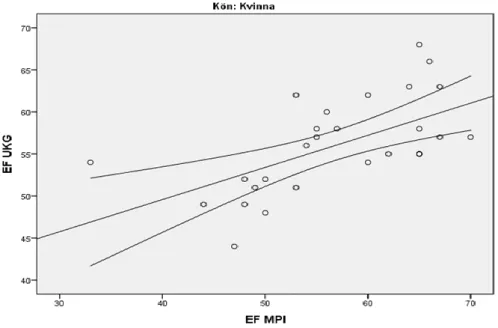
T-test för parvisa observationer visade en statistisk signifikant skillnad mellan EF som erhölls från UKG och MPI då p<0,05 och enligt resultatet var EF något lägre för MPI än för UKG. Män och kvinnor jämfördes vidare för sig via ett identiskt T-test där kvinnor inte visade sig ha en skillnad i EF mellan de två undersökningarna (p=n.s) (Figur 7). Män däremot, med ett p-värde <0,05 har en stark statistisk signifikant skillnad mellan de två undersökningarna (Tabell 5). Kvinnorna hade som mest en skillnad i EF på 21 procentenheter mellan de två undersökningstillfällena och männen en skillnad på 22 procentenheter, som minst förelåg det ingen skillnad i EF för varken män som kvinnor.
Tabell 4. Studiedeltagarnas vikt med ett intervall på 21 kg. Kvinnor och män anges i antal.
Tabell 3. Studiedeltagarnas ålder med ett intervall på 21 år.
Figur 6. Visualisering över spridningen av EF mellan undersökningarna. Varje prick motsvarar en individ. Linjär regression (y=26,88+0,54*x) med 95 % konfidensintervall.
14
Tabell 5. EF är presenterat i medelvärden ± standardavvikelsen (SD). Det exakta p-värdet är angivet.
Kön EF UKG EF MPI P-värde Total 54,3±8,4 51,3±10,7 0,000341
Män 53,6±9,3 48,8±10,5 0,000005
Kvinnor 56,0±5,6 56,9±8,8 0,524
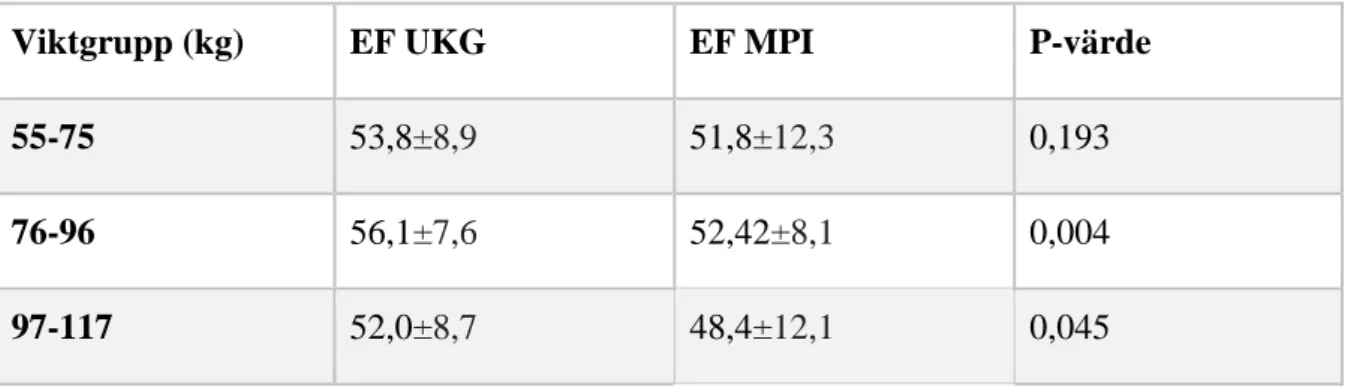
De två äldre åldersgrupperna visades ha en signifikant skillnad i EF mellan de två undersökningsmetoderna där den äldsta gruppen uppvisade ett p-värde i närhet med signifikansnivån 0,05. Den yngre åldersgruppen (25-45 år) visade på ett omvänt resultat vilket emellertid bör iakttas med försiktighet på grund av dess ringa innehåll med enbart fyra individer (Tabell 6). Även viktgrupperna gav varierande resultat. Den lättare viktgruppen (55-75 kg) visade ingen statistisk signifikant skillnad mellan de två undersökningarna (p>0,05) (Figur 8). För den mellersta och övre viktgruppen kunde däremot en skillnad påträffas (Tabell 7).
Figur 7. Visualisering över spridningen av EF mellan undersökningarna för kvinnor. Varje prick motsvarar en individ. Linjär regression (y=34,29+0,38*x) med 95 % konfidensintervall.
15
Tabell 6. EF är presenterat i medelvärden ± SD. Det exakta p-värdet är angivet.
Åldersgrupp (år) EF UKG EF MPI P-värde 25-45 51,3±10,4 45,8±11,1 0,383
46-66 54,9±7,9 51,9±9,6 0,005
67-87 54,1±8,8 51,6±11,7 0,046
Tabell 7. EF är presenterat i medelvärden ± SD. Det exakta p-värdet är angivet.
Viktgrupp (kg) EF UKG EF MPI P-värde 55-75 53,8±8,9 51,8±12,3 0,193
76-96 56,1±7,6 52,42±8,1 0,004
97-117 52,0±8,7 48,4±12,1 0,045 Figur 8. Visualisering över spridningen av EF mellan undersökningarna för viktgruppen 55-75 kg. Varje prick motsvarar en individ. Linjär regression (y=27,51+0,51*x) med 95 % konfidensintervall.
16
Diskussion
Metoddiskussion
Personuppgifter och relaterad information har kontrollerats av författarna och handledaren vilket kan garantera att uppgifter och mätdata använts korrekt samt att resultatet är pålitligt och relevant för arbetet. Syftet var att se om en signifikant skillnad i EF-bestämning fanns mellan de båda undersökningsmetoderna, vilket med hjälp av det insamlade materialet, kunde undersökas och senare bekräftas. Artiklar har sökts genom att använda utvalda sökord som finns specificerade under “Material och metod”. Dessa var något begränsade då mängder av artiklar med, men även utan, relevans för arbetet uppdagades vid artikelsök. Dessa hade ett publiceringsdatum från bland annat samma år (2017) men även sedan 1980-talet, men ett begränsat tidsintervall på artiklar uteslöts då äldre artiklar alltjämt kan innehålla den nyaste informationen inom området. De äldre artiklarna, valda att användas i detta arbete, har använts i nyare studier och innehöll samma eller liknande information som andra studier som inkluderats i detta arbete. Innehållet har enligt de båda författarna därför fortfarande en hög relevans för det som undersökts. Alla tidskrifter, där artiklarna i detta arbete publicerades, granskades efter Impact Factor (IF) där dessa hade som mest en IF på ca 17 och som lägst på ca 0,3. Artiklar uteslöts som var publicerade i tidskrifter utan IF och i kommande studier kan validiteten stärkas ytterligare om artiklar med låg IF utesluts. Användning av respektive mätinstrument (gammakamera och ultraljudsmaskin) har inte författarna av arbetet haft större insyn över, utan metodbeskrivningar har legat till grund för tillvägagångssättet för undersökningarna. Eftersom att metoderna är ackrediterade enligt SS-EN17025 [40] ställer det krav på att metodbeskrivningar används korrekt och att kompetens finns för att utföra undersökningarna. Validiteten för de båda undersökningarna är höga då de kan appliceras på individer av olika kroppsbyggnad och åldersspann, dock kan det vid UKG uppstå vissa svårigheter med visualisering vid högt BMI. Insamlad data, så som vikt, ålder och kön, har kontrollerats flertalet gånger vid överföring till SPSS utav de två författarna för att konstatera att resultatet grundar sig på de exakta värdena. Ytterligare har även handledaren granskat mätdata och resultat, för att stärka arbetets validitet och metoden har beskrivits för att enkelt kunna upprepas. Kriterievaliditeten kan i fortsatta studier stärkas genom att jämföra mätmetoderna med golden standard, CMR. Dock har det formulerade syftet ingen relation med vilken undersökning som korrelerar bäst med CMR. Reliabiliteten vill utredas för de två undersökningarna i detta arbete där om syftet ger ett lika resultat av EF, är reliabiliteten hög för de två metoderna. Här har skillnader dock kunnat urskiljas mellan mätmetoderna, men även att
17
de stämmer överens i enskilda fall. Det har dock inte kontrollerats hur många olika undersökare som har varit aktiva i insamlingen vid UKG, vilket skulle kunna orsaka en felaktig variation i EF-bestämning på grund av så kallade slumpmässiga eller systematiska fel hos de olika användarna. Däremot ska undersökningen följa gällande metodbeskrivning vilket borde resultera i att EF-bestämningen inte skiljer avsevärt mellan undersökarna, däremot kan felkällor uppkomma vid manuella justeringar. Kvalitetskontroller görs dagligen av gammakameror för att kontrollera att eventuella fel inte påverkar resultatet och att fel borde kunna uteslutas. Däremot var arbetet tidsbegränsat vilket medförde att det inte fanns möjlighet att vidare utreda om de olika kamerorna (Philips & Siemens) som var av olika årgång, haft en större inverkan på slutresultatet.
Resultatdiskussion
Resultatet av denna studie visar att en statistisk signifikant skillnad av EF mellan de två undersökningsmetoderna föreligger för det totala urvalet i vila. Nollhypotesen är således förkastad. EF visade sig vara lägre för MPI än för UKG vilket även har noterats i tidigare studier där dock denna skillnad inte anses ha en vedertagen förklaring [16]. En möjlig förklaring till detta kan enligt Henneman et al. (2006) vara att utflödestrakten i LV är mer framträdande vid UKG och att området därför blir underskattat vid MPI [12]. Ytterligare uppdelning av data utfördes för att vidare se var skillnaden förelåg och vilka parametrar som kan vara av relevans för denna skillnad. Utfallet visade att det inte förelåg någon statistisk signifikant skillnad bland kvinnor varvid intresse fanns att undersöka om ålders- och viktgrupper hade ytterligare påverkan på resultatet.
Vid hög ålder föreligger en ökad risk, samt en ökad förekomst av flertalet hjärtsjukdomar som orsakar efterföljande försämring av den systoliska- och diastoliska hjärtfunktionen. Hjärtats åldrande medför utöver flertalet riskfaktorer även naturliga ombildningar som därmed förändrar den systoliska- och diastoliska funktionen. Däribland försämrad diastolisk relaxation, minskad tidig diastolisk fyllnad, ökad sen diastolisk fyllnad men även tilltagande arytmier. Det naturliga åldrandet samt risker som detta medför försämrar alltså EF i olika utsträckning [41-43] beroende på individens hälsotillstånd. Det finns därför en risk hos individer med hög ålder att EF försämras inom studiens tvåmånadersperiod utan att de två undersökningarna skiljer sig åt, på grund av nytillkomna hjärtsjukdomar som exempelvis hjärtinfarkt [44]. Troligen är tidsintervallet i denna studie tillräckligt snävt för att utesluta en försämring av EF hos individer med snabb degenererande hjärtsjukdom. Emellertid är detta inget som kan säkerställas i detta
18
arbete. Vad gäller hjärtarytmier, är det känt att dessa ökar i frekvens och i intensitet med stigande ålder där de framträder oftare i vila och under träning hos en äldre individ [41-42]. En GSPECT vid MPI har begränsningar där arytmier kan orsaka sämre precision för EF-beräkningen. På grund av denna minskade precision rekommenderas inte användning av EKG för arytmipatienter med exempelvis förmaksflimmer eller med frekventa tidiga ektopiska extraslag [44]. Följaktligen blev det relevant att granska mer ingående vilka åldersgrupper studiedeltagarna tillhörde för att spekulera kring om åldrandets fysiologi och dess medföljande risker för hjärtsjukdomar kan ha haft en inverkan på slutresultatet. Individerna som deltog i denna studie hade en medelålder på 65,5 år vilket resulterade i att den yngre åldersgruppen (<45 år) presenterades med endast fyra individer, varvid resultatet inte anses vara helt tillförlitligt. Den äldre åldersgruppen med ett större antal individer visade på ett p-värde i närhet, men mindre än signifikansnivån (p<0,05), vilket ändock styrker att det finns en skillnad i EF mellan de två metoderna. Åldrarna 46-66 år med 44 individer inom gruppen kan med säkerhet fastställa en stark statistisk signifikant skillnad av EF mellan de två undersökningsmetoderna varvid slutsatsen är en skillnad i EF-bestämning oberoende av ålder.
Flertalet studier har framhävt att fetma och övervikt är riskfaktorer för utveckling av hjärtsjukdomar som påverkar EF [45-46]. Patienter med fetma men även de med andra tillstånd som kronisk obstruktiv lungsjukdom (KOL) och begränsat utrymme mellan revbenen kommer oftare ha en sämre bildkvalitet än övriga individer under avbildning av de ekokardiografiska snitten vid UKG [9, 44]. Enligt Foley et al. (2012) kan inte EF bestämmas med Simpsons biplanmetod på ca en tredjedel av patienterna på grund av oduglig bildkvalitet. Ifall mätningar ändå utförs, trots sämre bildkvalitet, kan beräkningarna bli felaktiga på grund av att endokardiets konturer inte kan visualiseras och mätas korrekt [44]. Visualisering av endokardiets konturer är en huvudsaklig faktor till att EF kan bestämmas mer exakt [5, 34, 47]. Body mass index (BMI) hade varit fördelaktigt att använda istället för kroppsvikt då måttet mer explicit beskriver om individen är överviktig eller inte och BMI tar ytterligare hänsyn till en persons längd där en tyngre individ inte nödvändigtvis behöver vara över normalvikt [48]. Brist på tillgång till journaler och tid för inhämtning av godkännande från individer som berördes, medförde att en kompromiss med kroppsvikt användes. Utifrån tidigare studier konstateras det därför att övervikt och fetma har en negativ påverkan på EF, främst vid UKG, som följaktligen kan komma att påverka utfallet i detta arbete. Vidare granskning av kroppsvikt av de 91 studiedeltagarna visade att de övre grupperna (>76 kg) skiljde sig åt i EF mellan de två metoderna. Detta understryker att kroppsvikt har en betydelse för bestämning av EF eftersom
19
att individer >76kg ligger till grund för att män fick en signifikant skillnad i EF, där tyngre individer (>76 kg) får ett mer varierat resultat än lättare (<76 kg). Kvinnorna var som mest representerade i den lättare viktgruppen varvid slutsatser kan dras: kroppsvikt (>76 kg) är en bidragande faktor till att män, i denna studie, har en skillnad i EF mellan de två undersökningarna.
I denna studie kunde inte information om patienterna som kan påverka EF hämtas på grund av brist på tillgång till journaler, och inhämtning av deltagarnas godkännande var inte möjlig inom avsatt tid. Det enda exklusionskriteriet som kunde användas förekom hos individer som inte genomgått en GSPECT varvid EF inte kunde beräknas. Brist på exklusionskriterier (exempelvis patienter med pågående cytostatikabehandling eller nyligen genomgången hjärtinfarkt mellan de två undersökningstillfällena) utesluter inte risken att resultatet blivit avvikande. Cytostatikabehandling och hjärtinfarkt kan nämligen medföra att EF ändras markant [3, 33, 41] utan att MPI eller UKG har begränsningar i programvaran eller i genomförandet. Ifall exklusionskriterier varit möjligt att använda skulle det innebära att eventuella försämrade hälsotillstånd, som för närvarande inte kan fullt säkerställas, skulle haft en mindre inverkan på resultatet av studiens datamaterial. Av denna anledning valdes den begränsande tvåmånadersperioden för att minska risken för ett försämrat hälsotillstånd hos den enskilda individen som kan komma att påverka EF mellan de två undersökningarna.
Patienten i sidoläge är den standardiserade metoden för att åskådliggöra hjärtat i 4C och 2C vid UKG [39]. Rätt positionering optimerar avbildning av de ekokardiografiska snitten med en minskad risk att utövaren skär dessa snett. Synliga konturer av endokardiet är, som tidigare nämnt, en grundläggande faktor till att EF beräknas korrekt och när mindre än 80 % av konturerna är visualiserade bör kontrast användas för bästa bildkvalitet [34, 47]. Oförmåga till sidoläge kan exempelvis uppstå vid patientsmärta varvid rekommendationer för positionering inte kan användas. Patienter som inte låg i sidoläge kan inte exkluderas i denna studie på grund av avsaknad av dokumentation, vilket medför att patientläget kan vara en anledning till missvisande EF. Missvisande EF kan likaså uppstå vid snedskurna snitt när patienten trots allt, är placerad enligt standardiserade metoder [1]. Utövarens skicklighet att precisera de ekokardiografiska snitten för att avbilda en korrekt hjärtvy är avgörande i beräkningen av EF [34, 47]. Placeras ultraljudsgivaren för högt upp på bröstkorgen kan hjärtapex missas och EF felbedömas enligt Simpsons biplanmetod på grund av en förminskning av EDV och ESV i LV [1, 49]. Därför bör biplanmätningarna göras i både 4C och 2C för mer pålitliga resultat [1].
20
Utövarens skicklighet ligger även i den mänskliga förmågan att detektera endokardiets konturer till skillnad från den automatiska bedömningen. Felkällor kan uppkomma ifall manuella korrigeringar inte utförs vid missbedömda automatiska beräkningar, och EDV och ESV är således beroende av den subjektiva bedömningen för rätt bestämning av EF och ett tillförlitligt resultat [45]. Flera sjukdomstillstånd kan även orsaka att avbildningen vid UKG blir av sämre kvalitet än förväntat. Emfysem försvårar exempelvis lungornas förmåga att tömma sig på luft vilket orsakar hinder för ultraljudsvågorna att nå målorganet. Luft reflekterar nämligen alla utsända ultraljudsvågor med en följd av att skuggor uppstår under det luftfyllda organet som skymmer alla strukturer i det utsatta området [50]. Endokardiets konturer kan således även i detta fall bli svårvisualiserade. Exkludering av felaktigt patientläge, sjukdomstillstånd med påverkan på EF och nyutbildade utövare vid UKG kan eventuellt ge i kommande studier ett mer tillförlitligt resultat.
Vid MPI ligger patienten, vid Länssjukhuset Ryhov [21], alltid på rygg (supine position) och beräkningarna utförs automatiskt vilket minskar risken för felkällor som mer frekvent uppkommer vid UKG [2]. Felkällor kan ändock uppstå, vid MPI, på grund av skillnader i programvarans algoritmer som används för att detektera konturer i LV. En liten LV, trots normal hjärtfunktion, kan medföra att ESV underskattas [12, 44] och enligt Toba et al. (2000) har det visats att små hjärtan ger spridda EF-bestämningar vid användning av programvaran QGS från Cedars-Sinai än hos andra automatiska programvaror [11]. Kvinnor har oftare mindre LV än män vilket innebär att EF vanligen överskattas, på grund av en felbedömd ESV, hos dessa individer vid en MPI. Detta förmodas bero på en sämre bildupplösning som gör endokardiet i LV suddig i jämförelse med väggtjockleken i LV. Pulstätheten från hjärtat ökar även i samband med en hjärtkontraktion vilket anses ligga till grund för den missbedömda ESV vid små volymer i LV [44]. Allmänt är ändock 2DE vid UKG mer benägen att variera i EF-bestämning än MPI på grund av geometriska antaganden varav tredimensionell ekokardiografi (3DE) är en ny framtagen, men inte än fulländad, metod inom ekokardiografi för att minska dessa antaganden [6, 16, 44].Det är viktigt att de rätta volymerna för EDV och ESV beräknas och används för att undvika felaktig EF. Om dessa inte beräknas kommer EF att värderas för lågt vid underskattad EDV och överskattad ESV.Mätningen av volymerna vid MPI är beroende av en tillräckligt lång insamling av volymer i LV (undersökningstid) för att finna den största och minsta kammarvolymen. Kortare undersökningstid kan medföra en missvisande EDV och ESV och enanvändning av åtta bilder per hjärtcykel, istället för 16 bilder, har visats orsaka en systematiskt minskad EF på 2-6 % [16, 19]. Vid insamling av bilder i detta arbete användes åtta
21
bilder per hjärtcykel vilket kan ha influerat EF-bestämningen till det sämre. En överskattning av EF vid små hjärtan, men en underskattning EF vid åtta bilder/cykel, kan vara en anledning till att kvinnor inte uppvisade en signifikant skillnad i EF mellan de två metoderna. Män däremot som mer sällan uppvisar små volymer i LV kan ha fått ett underskattat EF vid MPI på grund av att åtta istället för 16 bilder användes per hjärtcykel. En kroppsvikt >76 kg behöver, som tidigare diskuterat, därför inte vara en anledning till att män uppvisade en signifikant skillnad i EF-bestämning utan snarare att vid en lättare kroppsvikt (där majoriteten i detta arbete var kvinnor) överskattas EF felaktigt.
Vid bearbetning av de insamlade bilderna finns en möjlighet, vid utlinjering, att en bit av hjärtat har kapats av eller att bukupptag har inkluderats felaktigt. Detta skulle innebära att en del av volymen försvinner och skapar en falsk för hög eller låg EF beroende på hur hjärtat blir skuret. Att hjärtat kapats kan därför bero på högt radioaktivt upptag i lever och tarmar som stör bedömningen [22, 44]. Detektering av myokardiets konturer kan även vara begränsade vid MPI i anslutning till den automatiska beräkningen hos individer med perfusionsdefekter (exempelvis efter en hjärtinfarkt). Är perfusionsdefekterna tillräckligt svåra med följd av att LV-konturerna inte kan fastläggas riktigt kan EF följaktligen beräknas felaktigt. De automatiska programmen som används idag har dock en hög precision, och påverkan på EF kan således bli minimal trots svåra perfusionsdefekter [44]. Inga uppgifter har inhämtats om deltagarna haft perfusionsdefekter eller inte.
Framtida studier kan för ett mer tillförlitligt resultat utesluta patienter vars EF kan komma att ändras markant mellan de två undersökningarna och även kontrollera om en skillnad kan urskiljas mellan olika gammakameramärken. Detta innefattar exkludering av hjärtsjukdom med känd påverkan på EF, patienter med svårbedömda konturer av endokardiet på grund av oduglig bildkvalitet och patienter på hjärttoxisk behandling (cytostatika). Vidare kan en inkludering av BMI istället för kroppsvikt i framtida studier övervägas, eftersom att tidigare studier visade att en högre kroppsvikt, men främst övervikt (högt BMI), haft en påverkan på EF. Urvalet på 91 individer är dock tillräckligt stort för att generaliseras på en större population för att slutsatser ska kunna framföras adekvat. Resultatet kräver vidare utredning för att analysera vilken undersökning av MPI och UKG som korrelerar bäst med golden standard, CMR, och som därför ger ett mer sanningsenligt mått på EF.
22
Slutsatser
Nollhypotesen förkastas vilket innebär att EF-bestämningen skiljer sig åt mellan de två undersökningarna, MPI och UKG, i vila där ålder inte har en påverkan på EF-bestämningen. Patienter med en lättare kroppsvikt (majoriteten kvinnor) kan vara en anledning till att resultatet skiljer sig åt för män då kvinnor oftare uppvisar en mindre hjärtvolym som, vid MPI, ger en överskattad EF-bestämning. Detta tillsammans med att åtta bilder/hjärtcykel användes, som istället ger en underskattning av EF, kan vara en förklaring till att kvinnornas EF inte skiljde sig åt mellan de två metoderna medan män uppvisade en statistisk signifikant skillnad.
23
Omnämnanden
Tack till handledare och sjukhusfysiker Sven-Åke Starck för all hjälp med insamling av data och utformning av examensarbetet. Ytterligare tack till personal på avdelningen för Klinisk fysiologi på Länssjukhuset Ryhov för hjälp och tillgång till utrustning samt till det insamlade datamaterialet.
24
Referenser
1. Olsson A. Ekokardiografi. Stockholm: Ultraview Tryckspecialisten AB; 2014.
2. Hietala SO, Åhlström Riklund K, redaktörer. Nuklearmedicin. Lund: Studentlitteratur AB; 2013.
3. Maret E, Brudin L, Lindstrom L, Nylander E, Ohlsson JL, Engvall JE. Computer-assisted determination of left ventricular endocardial borders reduces variability in the echocardiographic assessment of ejection fraction. Cardiovascular Ultrasound. 2008;6(55). doi: 10.1186/1476-7120-6-55.
4. Garg N, Dresser T, Aggarwal K, Gupta V, Mittal MK, Alpert MA. Comparison of left ventricular ejection fraction values obtained using 2D echocardiography, and gated single-photon emission computed tomography. SAGE Open Medicine. 2016;4:1–7. doi: 10.1177/2050312116655940.
5. Yu EH, Sloggett CE, Iwanochko RM, Rakowski H, Siu SC. Feasibility and Accuracy of Left Ventricular Volumes and Ejection Fraction Determination by Fundamental, Tissue Harmonic, and Intravenous Contrast Imaging in Difficult-to-Image Patients. Journal of the American Society of Echocardiography. 2000;13(3):216-224. doi: 10.1067/mje.2000.103597.
6. Chahal NS, Lim TK, Jain P, Chambers JC, Kooner JS, Senior R. Population-Based Reference Values for 3D Echocardiographic LV Volumes and Ejection Fraction. J Am Coll Cardiol Img. 2012;5(12):1191-1197. doi: 10.1016/j.jcmg.2012.07.014.
7. Ande F, Buss S, Celik C, Abdel-Atyl H, Fernanda Braggion Santos M, Katus HA, et al. Discrepancies in ejection fraction measurements between echocardiography and cardiovascular magnetic resonance lead to different clinical classifications. Journal of Cardiovascular Magnetic Resonance. 2013;15(Suppl 1):O11. doi: 10.1186/1532-429X-15-S1-O11.
8. Danesh-Sani SH, Zakavi SR, Oskoueian L, Kakhki VR. Comparison between 99mTc-sestamibi gated myocardial perfusion SPECT and echocardiography in assessment of left ventricular volumes and ejection fraction - effect of perfusion defect and small heart. Nucl Med Rev. 2014;17(2):70-74. doi: 10.5603/NMR.2014.0020.
9. Hatipoğlu F, Burak Z, Ömür Ö. Comparison of gated myocardial perfusion SPECT, echocardiography and equilibrium radionuclide ventriculography in the evaluation of left ventricle contractility. Arch Turk Soc Cardiol. 2014;42(4):349-357. doi: 10.5543/tkda.2014.74150.
25
10. Kracskó B, Barna S, Sántha O, Kiss A, Varga J, Forgács A, et al. Effect of patient positioning on the evaluation of myocardial perfusion SPECT. J. Nucl. Cardiol. 2017. doi: 10.1007/s12350-017-0865-4.
11. Toba M, Kumita SI, Cho K, Mizumara S, Kijuma T, Nakajo H, et al. Comparison of emory and cedars-sinai methods for assessment of left ventricular function from gated myocardial perfusion SPECT in patients with a small heart. Ann Nucl Med. 2000;14(6):421-426. doi: 10.1007/BF02988287.
12. Henneman MM, Bax JJ, Schuijf JD, Jukema W, Holman ER, Stokkel MPM, et al. Global and regional left ventricular function: a comparison between gated SPECT, 2D echocardiography and multi-slice computed tomography. European Journal of Nuclear Medicine and Molecular Imaging. 2006;33(12):1452-1460. doi: 10.1007/s00259-006-0158-7.
13. Jonson B, Wollmer P, redaktörer. Klinisk fysiologi med nuklearmedicin och klinisk neurofysiologi. Stockholm: Liber AB; 2011.
14. Stanford University. Apikal 5 chamber view [Bild]. Stanford University: 2009
[Uppdaterad 2009-06-23, citerad 2017-04-30] Hämtad från:
http://web.stanford.edu/group/ccm_echocardio/cgi-bin/mediawiki/index.php/Apical_5_chamber_view
15. Stanford University. Apikal 2 chamber view [Bild]. Stanford University: 2009
[Uppdaterad 2009-06-23, citerad 2017-04-30] Hämtad från:
https://web.stanford.edu/group/ccm_echocardio/cgi-bin/mediawiki/index.php/Apical_2_chamber_view.
16. Yalçin H, Maza S, Yalçin F. Single photon emission computed tomography: An alternative imaging modality in left ventricular evaluation. Vasc Health Risk Manag. 2008;4(5):1069-1072. doi: 10.2147/VHRM.S3152.
17. Berglund E, Jönsson BA, redaktörer. Medicinsk fysik. Lund: Studentlitteratur AB; 2007.
18. Carlsson S, Svensson SE. Nuklearmedicin. Version 1.0. 2007-10-31. Tillgänglig: http://www.sfnm.se/wp/wp-content/uploads/2013/08/Nuklearmedicin_SC_SES.pdf 19. Biersack HJ, Freeman LM, editors. Clinical Nuclear Medicine. Tyskland;
Springer-Verlag Berlin Heidelberg; 2007.
20. Hesse B, Tägil K, Cuocolo A, Anagnostopoulos C, Bardiés M, Bax J, et al. EANM/ESC procedural guidelines for myocardial perfusion imaging in nuclear cardiology. Eur J Nucl Med Mol Imaging. 2005;32(7):855-897. doi: 10.1007/s00259-005-1779-y.
26
21. Metodbeskrivning, Myokardscintigrafi (930, 934, 938, 939). Medicinsk diagnostik, Klinisk fysiologi. Version 1.0. Gäller från 2017-04-04.
22. Strauss WH, Douglas Miller D, Wittry MD, Cerqueira MD, Garcia EV, Iskandian AS, et al. Procedure Guideline for Myocardial Perfusion Imaging 3.3*. Journal of Nuclear Technology. 2008;36(3):155-161. doi: 10.2967/jnmt.108.056465.
23. SPC, Summary of Product Characteristics - produktresume (läkemedelsbeskrivning). 24. Fathala A. Myocardial Perfusion Scintigraphy: Techniques, Interpretation, Indications
and Reporting. Annals of Saudi Medicine. 2011;31(6):625–634. doi: 10.4103/0256-4947.87101.
25. Jorfeldt L, Pahlm O, redaktörer. Kliniska arbetsprov - metoder för diagnos och prognos. Lund: Studentlitteratur AB; 2013.
26. Verberne HJ, Acampa W, Anagnostopoulos C, Ballinger J, Bengel F, De Bondt P, et al. EANM procedural guidelines for radionuclide myocardial perfusion imaging with SPECT and SPECT/CT: 2015 revision. Eur J Nucl Med Mol Imaging. 2015;42(12):1929-1940. doi: 10.1007/s00259-015-3139-x.
27. Lännergren J, Westerblad H, Ulfendahl M, Lundeberg T, redaktörer. Fysiologi. Lund: Studentlitteratur AB; 2007.
28. Haug E, Bjålie JG, Sand O, Sjaastad OV. Människokroppen. Stockholm: Liber AB; 2007.
29. Sahlen A, Winter R. How should we measure global and regional left ventricular systolic function? Journal of Echocardiography. 2011;9(2):41-50. doi: 10.1007/s12574-011-0085-x.
30. Vård vid hjärtsvikt, Beskrivning av åtgärderna, Region Jönköpings län. (2014). Hämtad från http://plus.rjl.se/infopage.jsf?nodeId=35546&childId=8593, 2017-05-16.
31. Joffe SW, Ferrara J, Chalian A, Tighe DA, Aurigemma GP, Goldberg RJ. Are ejection fraction measurements by echocardiography and left ventriculography equivalent? American Heart Journal. 2009;158:496-502. doi: 10.1016/j.ahj.2009.06.012.
32. Ericson E, Ericson T, redaktörer. Medicinska sjukdomar. Lund: Studentlitteratur AB; 2012.
33. Feenstra J, Grobbee DE, Remme WJ, Stricker BH. Drug-induced heart failure. Journal of the American College of Cardiology. 1999;33(5):1152-1162. doi: 10.1016/S0735-1097(99)00006-6.
34. Lang RM, Badano LP, Mor-Avi V, Afilalo J, Armstrong A, Ernande L, et al. Recommendations for Cardiac Chamber Quantification by Echocardiography in Adults:
27
An Update from the American Society of Echocardiography and the European Association of Cardiovascular Imaging. Journal of the American Society of Echocardiography. 2015;28(1):1-39. doi: 10.1016/j.echo.2014.10.003.
35. Stanford University. Echocardiography in ICU: Left ventricular systolic function [Bild]. Stanford University: 2009 [Uppdaterad 2009-07-15, citerad 2017-05-02] Hämtad från:
https://web.stanford.edu/group/ccm_echocardio/cgi-bin/mediawiki/index.php/Left_ventricle_systolic_function.
36. Wood PW, Choy JB, Nanda NC, Becher H. Left Ventricular Ejection Fraction and Volumes: It Depends on the Imaging Method. Echocardiography. 2014;31(1):87-100. doi: 10.1111/echo.12331.
37. Negishi K, Negishi T, Haluska BA, Hare JL, Plana JC, Marwick TH. Use of speckle strain to assess left ventricular responses to cardiotoxic chemotherapy and cardioprotection. Eur Heart J Cardiovasc Imaging. 2014;15(3):324–331. doi: 10.1093/ehjci/jet159.
38. Erhållen från Klinisk fysiologi, Länssjukhuset Ryhov i Jönköping.
39. Metodbeskrivning, Ultraljud hjärta. Medicinsk diagnostik, Klinisk fysiologi. Version 8.0. Gäller från 2016-02-22.
40. Swedish Standards Institute [Internet]. Allmänna kompetenskrav för provnings- och kalibreringslaboratorier (ISO/IEC 17025:2005). Tillgänglig från: http://www.sis.se/sociologi-service-f%C3%B6retagsorganisation-och-ledning-och-
administration/kvalitet/produkt-och-f%C3%B6retagscertifiering-f%C3%B6rs%C3%A4kran-om-%C3%B6verenskommelse/ss-en-iso-iec-170252005. Hämtad 2017-05-24.
41. Merrill GF. Our aging bodies. Rutgers University Press; 2015.
42. Saxon SV, Etten MJ, Perkins EA. Physical change and aging - A Guide for Helping Professions. New York; Springer Publishing Company; 2014.
43. Velásquez-Rodríguez J, Diez-Delhoyo F, Valero-Masa MJ, Vicent L, Devesa C, Sousa-Casasnovas I, et al. Prognostic Impact of Age and Hemoglobin in Acute ST-Segment Elevation Myocardial Infarction Treated With Reperfusion Therapy. The American Journal of Cardiology. 2017;S0002-9149(17):30341-30347. doi: 10.1016/j.amjcard.2017.03.018.
44. Foley TA, Mankad S, Anavekar N, Bonnichsen CR, Morris MF, Miller TD, et al. Measuring Left Ventricular Ejection Fraction – Techniques and Potential Pitfalls. European Cardiology. 2012;8(2):108–114. doi: 10.15420/ecr.2012.8.2.108.
28
45. Bening C, Weiler H, Vahl CF. Effects of gender, ejection fraction and weight on cardiac force development in patients undergoing cardiac surgery - an experimental examination. Cardiothorac Surg. 2013;8:214. doi: 10.1186/1749-8090-8-214.
46. Seo JS, Jin HY, Jang JS, Yang TY, Kim DK, Kim DS, et al. The Relationships between Body Mass Index and Left Ventricular Diastolic Function in a Structurally Normal Heart with Normal Ejection Fraction. J Cardiovasc Ultrasound. 2017;25(1):5-11. doi: 10.4250/jcu.2017.25.1.5.
47. Evangelista A, Flachskampf F, Lancellotti P, Badano L, Aguilar R, Monaghan M, et al. European Association of Echocardiography recommendations for standardization of performance, digital storage and reporting of echocardiographic studies. Eur J Echocardiogr. 2008;9(4):438-448. doi: 10.1093/ejechocard/jen174.
48. World Health Organization [Internet]. Global database on body mass index. BMI
classification. Tillgänglig från:
http://apps.who.int/bmi/index.jsp?introPage=intro_3.html. Hämtad 2017-05-15.
49. Edelman SK, Rowe DW, Pechacek LW, Garcia E. Left ventricular volumes and ejection fraction derived from apical two-dimensional echocardiography. Cardiovasc Dis. 1981;(3):344-354.
50. Allisy-Roberts P, Williams J. Farr’s physics for Medical Imaging. W B Saunders Co Ldt; 2007.
![Figur 1. Apikal fyrkammarvy [14]. Figur 2. Apikal tvåkammarvy [15].](https://thumb-eu.123doks.com/thumbv2/5dokorg/4616243.119037/7.892.131.764.730.960/figur-apikal-fyrkammarvy-figur-apikal-tvåkammarvy.webp)
![Figur 5. EF-bestämning vid MPI. Quantitative gated SPECT (QGS 2012) [38].](https://thumb-eu.123doks.com/thumbv2/5dokorg/4616243.119037/11.892.209.684.107.330/figur-ef-bestämning-mpi-quantitative-gated-spect-qgs.webp)