Kommersiella kit för
detektion av
makrolidresistens hos
Mycoplasma genitalium
HUVUDOMRÅDE: Biomedicinsk laboratorievetenskap FÖRFATTARE: Katarina Carlsson, Josefin Gustafsson HANDLEDARE: Sandra Karlsson
EXAMINATOR: Emma Carlsson JÖNKÖPING Maj 2020
En litteratursammanställning som underlag för
implementering i rutinverksamhet på Länssjukhuset
Ryhov i Jönköping
1
Sammanfattning
Mycoplasma genitalium är en sexuellt överförbar bakterie som traditionellt behandlas med makroliden
azitromycin. Bakterien har utvecklat makrolidresistens som främst orsakas av mutationer i positionerna A2058 och A2059 i genen 23s rRNA. För detektion av dessa mutationer används PCR-baserade metoder. På Laboratoriemedicin på Länssjukhuset Ryhov, Jönköping, detekteras M. genitalium med PCR och de ämnar sätta upp en metod för att även testa makrolidresistens. Denna studie ska ge ett teoretiskt underlag för att välja ett tillförlitligt kommersiellt kit för ändamålet. Syftet var att genom en litteraturstudie kartlägga och jämföra kommersiella kit som påvisar M. genitalium och makrolidresistens eller enbart makrolidresistens.
Sökningar med för syftet relevanta sökord gjordes i databaserna PubMed och ResearchGate och resulterade efter urval och kvalitetsgranskning i 15 publikationer. Fem kommersiella kit för detektion av M. genitalium och makrolidresistens, samt ett kit för enbart detektion av makrolidresistens, identifierades. Endast ResistancePlus® MG (SpeeDx, Australien) som detekterar både M. genitalium
och makrolidresistens utvärderades i tillräckligt många publikationer för att resultera i en slutsats. Sammanfattande värden, för ResistancePlus MG, för sensitivitet, specificitet och konkordans var alla >95% vilket tyder på att metoden är tillförlitlig. Utvärderingarna av övriga metoder visar höga värden, men fler studier behövs för att säkerställa dess prestanda.
2
Summary
Commercial kits for detection of macrolide resistance in
Mycoplasma genitalium
- A literature compilation as a base of choice before implementation at the hospital Ryhov in Jönköping
Mycoplasma genitalium (MG) is a sexually transmitted bacteria, traditionally treated with the
macrolide azithromycin. Macrolide resistance has developed and is mainly caused by mutations in the
23s rRNA gene (position A2058/A2059). These mutations can be detected by PCR based methods..
Laboratory medicine at the hospital Ryhov, Jönköping, detects MG with PCR and wants to implement a method for detection of macrolide resistance. This study presents a theoretical base for their choice of a commercial kit. The purpose was to identify and compare commercial kits for detection of MG and macrolide resistance, or macrolide resistance solely.
Searches with keywords, relevant to the purpose, were made in PubMed and ResearchGate and resulted in 15 publications, after selection and quality examination. Five commercial kits for detection of MG and macrolide resistance, and one kit for detection of macrolide resistance, were identified. ResistancePlus®
MG (SpeeDx, Australia), which detect MG and macrolide resistance, was the only kit evaluated in enough number of studies to present a credible result. Total sensitivity, specificity and concordance of ResistancePlus MG were all >95%, which demonstrate reliable performance for this method. The evaluations of the other methods indicated well performing methods, but more studies are needed to ensure their performance.
3
Innehållsförteckning
Inledning ... 4
Bakgrund... 4
Mycoplasma genitalium och dess komplikationer ... 4
Behandling ... 4 Makrolidresistens ... 5 Metoder för detektion ... 5 Detektion av M. genitalium ... 5 Detektion av makrolidresistens ... 5
Syfte... 6
Frågeställningar ... 6Metod ... 6
Datainsamling ... 6Databassökning och urval ... 6
Inklusions-/exklusionskriterier ... 6
Kvalitetsgranskning ... 7
Databearbetning ... 7
Etiska överväganden ... 9
Resultat ... 9
AllplexTM MG & AziR Assay (Seegene) ... 10
LightMix® Modular M. genitalium + Macrolide (TIB Molbiol) ... 10
Macrolide-R/MG ELITe MGB® Kit (ELITechGroup) ... 10
RealAccurate® TVMGRES (Pathofinder) ... 10
ResistancePlus® MG (SpeeDx) ... 11
ResistancePlus® MG FleXible (SpeeDx) ... 12
S-DiaMGResTM (Diagenode) ... 12
Diskussion ... 12
Resultatdiskussion ... 13
Sensitivitet och specificitet ... 13
AllplexTM MG & AziR (Seegene) ... 13
LightMix® Modular M. genitalium + Macrolide (TIB Molbiol) ... 13
Macrolide-R/MG ELITe MGB® Kit (ELITechGroup) ... 14
RealAccurate® TVMGRES (Pathofinder) ... 14
ResistancePlus® MG (SpeeDx) ... 14 S-DiaMGResTM (Diagenode) ... 14 Metoddiskussion ... 14
Slutsats ... 15
Referenser ... 16
Bilagor ... 18
4
Inledning
Mycoplasma genitalium är en mycket liten, sexuellt överförbar, bakterie som bland annat kan orsaka
uretrit (1, 2). Endast ett fåtal antibiotika har effekt mot M. genitalium däribland tetracycliner, makrolider och fluorokinoloner. Makroliden azitromycin har tidigare varit ett effektivt behandlingsalternativ, men ökning av makrolidresistens har orsakat problem med botande behandling (2). Hadad et al. har i en svensk studie från 2018 beskrivit att resistensökningen förhoppningsvis kan dämpas genom att rutinmässigt testa alla positiva M. genitalium för makrolidresistens och därigenom minska det selektiva trycket genom minskad användning av azitromycin (3). Även läkemedelverkets behandlingsrekommendation säger att det är av största vikt att behandla med rätt antibiotikum, för att nå full behandlingseffekt och undvika fortsatt resistensutveckling (4).
Laboratoriemedicin på Länssjukhuset Ryhov i Jönköping har sedan oktober 2019 skickat alla positiva
M. genitalium prover till Örebro Universitetssjukhus för att testa för makrolidresistens. I dagsläget
handlar det om ungefär 100 prover per år, men laboratoriemedicin räknar med en ökning. Med tanke på förväntad ökning av antal prover, resursåtgången för att skicka prover samt möjligheten till förkortade svarstider avser nu Laboratoriemedicin på Ryhov sätta upp en egen metod för detektion av makrolidresistens hos M. genitalium. För att ge ett teoretiskt underlag för metodval kommer tillgängliga kommersiella kit för ändamålet sammanställas och jämföras i denna litteraturstudie.
Bakgrund
Mycoplasma genitalium och dess komplikationer
M. genitalium är orsak till en sexuellt överförbar smitta som kan ge uretrit hos både män och kvinnor
(5). Hos kvinnor kan infektionen också orsaka cervicit, bäckeninflammation (pelvic inflammatory disease), prematur födelse, spontan abort eller infertilitet (6). Studier har också visat att en infektion med M. genitalium kan öka risken för HIV-infektion (2). Inflammationen i det urogenitala området orsakad av att M. genitalium fäster till epitelcellerna och framkallar en signal om akut inflammation via receptorer för det medfödda immunförsvaret. De flesta infektioner med M. genitalium är dock asymtomatiska och infektionen går över utan att komplikationer uppstår. I en litteraturstudie av Gnanadurai och Fifer (7) föreslås att det inte finns anledning till screening på asymtomatiska patienter. Munson (8) däremot som granskat flera andra studier menar att M. genitalium bör ingå i screening för sexuellt överförbara sjukdomar, för att öka patienters välbefinnande och för att förbättra klinisk verkan, inkluderat att identifiera resistenta stammar.
Behandling
Avsaknaden av cellvägg gör Mycoplasma spp naturligt resistenta mot cellväggsantibiotika, som penicillin, cefalosporin och vankomycin (1). Endast antibiotika som inhiberar nukleinsyrareplikation och proteinsyntes har effekt (9), och traditionellt har tetracycliner, makrolider och fluorokinoloner varit effektiva behandlingsalternativ (2). Tetracycliner är bredspektrumantibiotika som inhiberar proteinsyntes genom att binda till 30S ribosomer och blockerar bindningsstället för tRNA (1), men behandlingseffektiviteten är inte optimal och botar endast 22-45% (9). Fluorokinoloner är en utvecklad typ av kinoloner som inhiberar DNA syntes (1). Makrolider binder till bakteriers 23S rRNA i ribosomala subenheten 50S (1) och påverkar translationen och förändrar eller stoppar syntes av vissa proteiner (10). I Sverige, och även i övriga Europa, är makroliden azitromycin förstahandsalternativ vid behandling av
M. genitalium eftersom den hittills visat sig vara mest effektiv (2, 4).
Resistens mot makrolider har ökat snabbt och har föreslagits bero på behandling med engångsdos med ett gram azitromycin, som är vanlig vid utbredd infektion av Chlamydia trachomatis (3), men som även används för behandling av M. genitalium (11). Den nyare rekommendationen med utökad femdagarsbehandling vid M. genitalium-infektion kan också öka selektion för resistens, men det beskrivs som mer sällsynt (3). Läkemedelsverket skriver i sin behandlingsrekommendation att behandling med ett gram azitromycin peroralt som engångsdos bör undvikas (4).
Vid makrolidresistens rekommenderas, i Sverige, behandling med fluorokinolonen moxifloxacin, men även mot detta har vissa stammar utvecklat resistens (3, 4). I dessa fall saknas tillgängliga
5
patienter som haft behandlingssvikt med både azitromycin och moxifloxacin (2). Pristinamycin är en streptogramin som blockerar translation genom bindning till bakteriers 50S ribosomala subenhet och som genom synergieffekt av att den består av två typer av kemiska substanser får en baktericid effekt (12). Detta licenspreparat har endast förskrivits i enstaka fall på specialistkliniker (4).
Makrolidresistens
Makrolidresistens orsakas främst av mutationer i region V i genen för 23S rRNA hos M. genitalium, liksom hos flera andra bakterier (5, 13). Mutationerna består i utbyte av enskilda nukleotider, single-nucleotide polymorphisms (SNP) i positionerna A2058 och A2059, vilka har visat sig spela en viktig roll som bindningsställe för makrolider (13). Mutationerna har främst visats orsaka resistens mot makroliden azitromycin (5, 9), vilket betyder att begreppet makrolidresistens i sammanhanget egentligen betyder azitromycinresistens. Eftersom det är den makroliden som används vid behandling kommer begreppet fortsatt att användas. De fem främsta resistensassocierade mutationerna är A2058G, A2058C, A2058T, A2059C och A2059G, se Tabell 1. När vildtypsallelen A i position A2058 eller A2059 byts ut till en annan bas, blir bakterien resistent mot makrolider (14).
Tabell 1. De fem främsta mutationerna associerade med makrolidresistens hos M. genitalium
presenterade med vilken nukleotid som blir utbytt i position A2058 eller A2059 (14).
A2058 A2059 Prevalens vildtyp A A
A2058G G A Mest frekvent
A2059G A G Frekvent
A2058T T A Relativt frekvent
A2058C C A Sällsynt
A2059C A C Sällsynt
Metoder för detektion
Detektion av M. genitaliumMycoplasma spp kan odlas, men det görs sällan då de kräver mycket tillsatser i odlingsmedia och växer
väldigt långsamt med små kolonier som är svårdetekterade. De känsligaste diagnostiska testen för
Mycoplasma spp är amplifiering av artspecifika målgener med polymerase chain reaction (PCR) (1).
Exempel på målgener för M. genitalium är gener i MgPa operonet, inklusive genen för MgPa adhesin som har en viktig funktion för bakteriens virulens genom bindning och möjlighet att tränga in i epitelceller, och 16S rRNA (15). Exempel på provmaterial för extraktion till PCR är swab från vagina och livmoderhals, urin och endometriala biopsiprover. Från män kan även sperma och prostatautsöndringar användas (16).
Detektion av makrolidresistens
Eftersom M. genitalium inte odlas för diagnostisering kan inte heller traditionell resistensbestämning göras. Liksom för detektion av M. genitalium används PCR-baserade metoder för detektion av makrolidresistens (7). De första detektionerna av makrolidassocierade SNP i 23S rRNA gjordes genom sekvensering av amplifierade fragment över den aktuella regionen. Den första studien som presenterade mutationer i 23S rRNA kopplade till makrolidresistens i M. genitalium publicerades 2008 (5). Eftersom sekvensering är tidskrävande har andra snabbare metoder utvecklats, med sekvensering som referensmetod. Ett exempel är fluorescensmärkta hydrolysprober i kvantitativ PCR (qPCR) där en specifik region amplifieras och där proverna genom fluorescensen kan genotypas som vildtyp eller mutant (17). Även smältpunktsanalys (high resolution melt, HRM) har presenterats som möjligt alternativ för detektion av makrolidresistens. HRM innebär att hastigheten för denaturering från dubbelsträngat DNA till enkelsträngat DNA mäts och kommer skilja beroende på nukleinsyrainnehåll. Endast en avvikande bas ger olika hastighet och genom inkorporering av fluorescensmärkning som endast binder dubbelsträngat DNA kan denatureringen/smältpunkten detekteras i realtid (18).
Flera metoder har utvecklats till kommersiella kit för att detektera makrolidresistens, i vissa fall i kombination med samtidig detektion av M. genitalium. Dessa kit presenteras som resultat av denna litteraturstudie.
6
Syfte
Syftet var att genom en litteraturstudie kartlägga och jämföra kommersiella kit som påvisar M.
genitalium och makrolidresistens eller enbart makrolidresistens.
Frågeställningar
• Vilka kommersiella kit finns tillgängliga för detektion av makrolidresistens hos M. genitalium? • Vad har de olika kiten för sensitivitet och specificitet?
• Vilket kit har sammantaget den högsta sensitiviteten och specificiteten?
Metod
På grund av rådande Coronautbrott under våren 2020 kunde inte en laborativ datainsamling utföras och det ursprungliga syftet att laborativt testa och jämföra tre kommersiella kit åt Laboratoriemedicin på Ryhov fick modifieras. Studien utfördes istället som en litteraturstudie där kommersiella kit för detektion av makrolidresistens hos M. genitalium, i flera fall i kombination med detektion av M.
genitalium, sammanställdes och jämfördes.
Eftersom det fanns ett begränsat antal studier inom området gjordes en allmän litteraturstudie. Dock utfördes studien på ett systematiskt sätt och följde Forsberg och Wengströms beskrivning av systematisk litteraturstudie (19).
Datainsamling
Datainsamlingen genomfördes genom sökningar efter publikationer som beskriver och utvärderar kommersiella kit för detektion av makrolidresistens hos M. genitalium. När kommersiella kit hade identifierats utifrån dessa artiklar gjordes sökningar efter metodbeskrivningar på respektive företags hemsida eller google.se, för att få en mer detaljerad beskrivning av respektive kit/metod.
Databassökning och urval
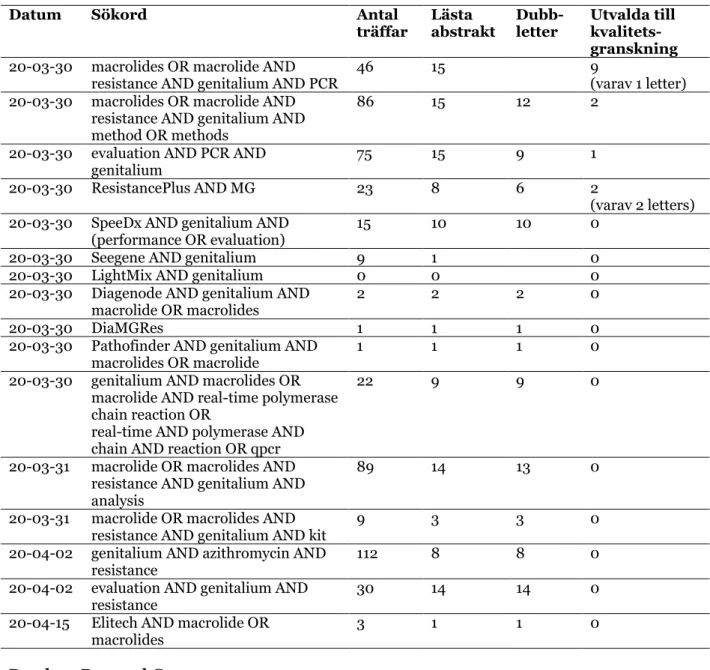
Sökningar gjordes i PubMed med för syftet relevanta sökord, inklusive MeSH-termer, enskilt eller i kombination, se Tabell 2. Vid sökning kom nya relevanta sökord upp och ytterligare sökningar gjordes. Sökningar med metodnamn som sökord gjordes även i ResearchGate. När nya sökord eller kombinationer inte resulterade i några unika träffar av relevanta publikationer (endast dubbletter) ansågs den totala sökningen vara fullständig.
Samtliga titlar lästes och där titel tydde på att publikationen kunde handla om någon metod för detektion av makrolidresistens lästes publikationens abstract. Publikationer med relevanta abstract lästes i sin helhet och de vars syfte var relevant för examensarbetets syfte kvalitetsgranskades. Totalt lästes 29 abstract varav 15 publikationer valdes ut för kvalitetsgranskning. Figur 1 visar urvalsprocessen från databassökning till kvalitetsgranskning.
Inklusions-/exklusionskriterier
Eftersom studien behandlar relativt nya metoder, sattes en gräns att endast publikationer publicerade de senaste tio åren skulle inkluderas i studien. Endast kvantitativa originalstudier på engelska inkluderades. På grund av begränsning i antal publikationer, inkluderades även en vetenskaplig poster och tre letters1 i studien.
7
Figur 1. Flödesschema över urvalsprocessen från databassökning till utvalda publikationer
för kvalitetsgranskning. Publikationer äldre än tio år filtrerades bort i sökningen. Övriga inklusionskriterier (kvantitativ originalstudie på engelska) användes vid urval vid abstractgranskning.
Kvalitetsgranskning
Utvalda publikationer kvalitetsgranskades enligt protokoll i Bilaga 1, där svar förknippade med hög kvalitet gav poäng. Protokollet bestod av frågor som formulerats för att ge en allmän kvalitetsbedömning samt en anpassad kvalitetsbedömning utifrån litteraturstudiens syfte. Protokoll från andra examensarbeten användes för att välja lämpliga frågor. En publikation kunde maximalt få 13 poäng och gränsen för hög kvalitet sattes till 11 poäng. Även publikationer med lägre poäng, ner till 10 poäng användes. Publikationerna granskades av två personer, oberoende av varandra, och medelpoäng användes för utvärdering.
Databearbetning
Resultat i de kvalitetsgranskade publikationerna, som svarade till syftet i denna studie, grupperades beroende på vilken metod de berörde (sex grupper). Publikationerna sammanställdes i en tabell innehållande publikationsinformation med kvalitetspoäng från kvalitetsgranskningen, namn på kommersiell metod som utvärderats, vilken typ av metod det var, samt resultatet i form av sensitivitet och specificitet, se Bilaga 2.
Från alla studier har metodernas sensitivitet (andel sant positiva) och specificitet (andel sant negativa) sammanställts. Hur väl överens alla resultat från kit stämmer med referensmetoden (konkordans) är en samlad bedömning av sensitivitet och specificitet. Konkordans har beräknats både för detektion av M.
genitalium (positiva och negativa), för detektion av makrolidresistens (resistenta och känsliga), samt en
total konkordans för både detektion av M. genitalium och makrolidresistens. För den totala konkordansen har det totala antalet testade prover använts, vilket innebär att de prover som analyserats för makrolidresistens redan har testats som positivt för M. genitalium och finns således med som två testade prover med två resultat. Den totala konkordansen blir därmed det totala antalet korrekta resultat delat med det totala antalet test som utförts.
Databassökning
(16 sökningar i PubMed, 7 sökningar i ResearchGate)
↓
Titelgranskning (562)
↓
Abstractgranskning (29)
(inklusive 3 letter och 1 poster)
↓
Kvalitets-granskning
8
Tabell 2. Sökhistorik från sökning i PubMed och ResearchGate. Sökning utförd med
relevanta sökord, vilka resulterade i utvalda publikationer till kvalitetsgranskning.
Databas: PubMed
Datum Sökord Antal
träffar Lästa abstrakt Dubb- letter Utvalda till kvalitets- granskning
20-03-30 macrolides OR macrolide AND
resistance AND genitalium AND PCR 46 15 9 (varav 1 letter) 20-03-30 macrolides OR macrolide AND
resistance AND genitalium AND method OR methods
86 15 12 2
20-03-30 evaluation AND PCR AND
genitalium 75 15 9 1
20-03-30 ResistancePlus AND MG 23 8 6 2
(varav 2 letters) 20-03-30 SpeeDx AND genitalium AND
(performance OR evaluation) 15 10 10 0
20-03-30 Seegene AND genitalium 9 1 0
20-03-30 LightMix AND genitalium 0 0 0
20-03-30 Diagenode AND genitalium AND
macrolide OR macrolides 2 2 2 0
20-03-30 DiaMGRes 1 1 1 0
20-03-30 Pathofinder AND genitalium AND
macrolides OR macrolide 1 1 1 0
20-03-30 genitalium AND macrolides OR macrolide AND real-time polymerase chain reaction OR
real-time AND polymerase AND chain AND reaction OR qpcr
22 9 9 0
20-03-31 macrolide OR macrolides AND resistance AND genitalium AND analysis
89 14 13 0
20-03-31 macrolide OR macrolides AND
resistance AND genitalium AND kit 9 3 3 0
20-04-02 genitalium AND azithromycin AND
resistance 112 8 8 0
20-04-02 evaluation AND genitalium AND
resistance 30 14 14 0
20-04-15 Elitech AND macrolide OR
macrolides 3 1 1 0
Databas: ResearchGate
Datum Sökord Antal
träffar Lästa abstrakt Dubb- letter Utvalda till kvalitets-granskning
20-04-02 Seegene AND Allplex AND genitalium
3 2 1 1 (poster)
20-04-02 macrolide AND resistance AND
genitalium AND evaluation 11 8 8 0
20-04-15 SpeeDx AND ResistancePlus AND
genitalium 20 5 5 0
20-04-15 MolBiol AND LightMix AND
genitalium 0 0 0
20-04-15 Diagenode AND DiaMGREs 1 1 1 0
20-04-15 Pathofinder AND genitalium 2 1 1 0
20-04-15 Elitech AND macrolide 2 1 1 0
9
Etiska överväganden
En litteraturstudie behöver inget etiskt tillstånd, dock har etiska reflektioner gjorts vid urval av publikationer. De publikationer som redovisat att de tagit hänsyn till etiska aspekter har fått kvalitetspoäng i kvalitetsgranskningen. Övriga publikationer har inkluderats i studien eftersom de behandlar anonymiserade prover som samlats in utan att det påverkat enskilda individer då studierna varit retrospektiva. De publikationer som inte angett etiska överväganden, två letters, en poster och två artiklar, har markerats i resultattabellen i Bilaga 2.
För att undvika ett skevt resultat har alla resultat som berör litteraturstudiens syfte presenterats i resultatet. Inga resultat som skulle kunna ändra litteraturstudiens resultat har undanhållits.
Resultat
Resultatet av litteraturstudien består av 15 publikationer, varav tre letters och en poster. Studierna som analyserats har utvärderat en eller flera kommersiella kit för detektion av M. genitalium och makrolidresistens eller enbart makrolidresistens. Tio publikationer har utvärderat ResistancePlus® MG
(SpeeDx, Australien), varav en har testat prestandan när prover tagits i annan buffert än den rekommenderade och en har testats för att mäta bakteriebörda. Två studier har utvärderat det kit av samma typ som ovan, som anpassats för GeneXpert® (Cepheid, CA, USA); ResistancePlus® MG FleXible
(SpeeDx, Australien). Vardera en publikation har utvärderat AllplexTM MG & AziR (Seegene, Korea),
Macrolide-R/MG ELITe MGB® (ELITechGroup, WA, USA), RealAccurate® TVMGRES (Pathofinder,
Nederländerna) och en föregångare till kitet LightMix® Modular M. genitalium + Macrolide (TIB
Molbiol, Tyskland). S-DiaMGResTM (Diagenode, Belgien) har utvärderats i två studier, varav en
utvärderade en prototyp för kitet. Samtliga publikationer är sammanställda i en tabell i Bilaga 2, presenterade med huvudsakligt resultat och kvalitetspoäng.
Sensitivitet, specificitet och konkordans för varje kit finns presenterad i Tabell 3. Där det finns flera studier, som utvärderat samma kit, har en sammanställning gjorts där antal testade prover och resultat har sammanvägts från studierna. För värden från enskilda studier se Bilaga 2. En beskrivning av respektive kit samt aspekter kring dess sensitivitet, specificitet och konkordans följer.
Tabell 3. Resultatsummering. Sensitivitet, specificitet och konkordans för detektion av M. genitalium (MG) och makrolidresistens för respektive kit sammantaget från alla
publicerade studier om metoderna.
Antal
studier Sensitivitet (MG) Specificitet (MG) Konkordans (MG) Sensitivitet (resistens) Specificitet (resistens) Konkordans (resistens) Total konkordans (MG+resistens)
AllplexTM MG & AziR (Seegene)
1 100%* 100%* 94,6%* 76,9% 100% 90% 92,3%
LightMix® Modular M. genitalium + Macrolide (TIB Molbiol)
1 97,8 Inga negativa prover testade 98,8% 96,3% 97,8% 97,0% (föregångare till kit)
Macrolide-R/MG ELITe MGB® (ELITechGroup)
1 85,6% 100% 89,3% 100% 99,4% 99,5% 93,3%
RealAccurate® TVMGres (Pathofinder)
1 96,4% Inga negativa prover testade 95% 97,3% 96,1% 96,1%
ResistancePlus® MG (SpeeDx)
8
97,7% (6 studier) 99,8% (5 studier) 99,4% (5 studier) 95,5% 97,6% 96,7% 98,5%
S-DiaMGResTM (Diagenode) 1 2 (inkl. prototyp) 94,8% 94,8% - - - - 100% 98,2% 97,3% 97,6% 98,7 97,9% - - *ResistancePlus MG som referensmetod
10
Allplex
TMMG & AziR Assay (Seegene)
Allplex MG & AziR (Allplex) är en multiplex qPCR som ger simultan detektion av M. genitalium och sex mutationer i positionerna A2058 och A2059, vilka är associerade med makrolidresistens (20).
I en studie av Barratt et al. (21) har Allplex jämförts mot ResistancePlus MG (n=93, varav 63 negativa enligt båda metoderna). I jämförelsen mot ResistancePlus MG hade Allplex en sensitivitet och specificitet på 100%, och konkordansen var 94,6%. Fem prover som ResistancePlus MG bedömde som negativa blev positiva med Allplex. Fyra av dessa extraherades om och testades på nytt, men för det femte fanns inte tillräckligt med provmaterial kvar. Denna gång gav Allplex tre positiva jämfört mot två som detekterades av ResistancePlus MG. Detektion av resistens, i 30 prover positiva för M. genitalium, jämfördes mot sekvensering och kunde därmed jämföras mot andra metoder. Av de 13 prover som hade resistensmutation detekterades tio av Allplex.
LightMix
®Modular M. genitalium + Macrolide (TIB Molbiol)
LightMix Modular M. genitalium + Macrolide (LightMix) är en qPCR kombinerad med smältkurvsanalys för detektion av M. genitalium och mutationer i positionerna A2058 och A2059. Ett 73 bp långt fragment av en målgen för M. genitalium amplifieras och detekteras med en märkt hydrolysprobe. Samtidigt amplifieras ett 115 bp långt fragment av genen för 23S rRNA som detekteras av en märkt probe och definieras som muterad eller vildtyp genom smältpunktsanalys (22).
Gossé et al (23) har testat en föregående metod till detta kit och resultaten har jämförts mot DNA-sekvensering. Utvärderingen av metoden gjordes på 139 M. genitalium-positiva prover, varav 85 hade resistensmutation. Metoden bedömde 136 prover som positiva för M. genitalium. Eftersom inga negativa prover inkluderades kunde metodens specificitet för detektion av M. genitalium inte utvärderas. Smältkurvsanalysen differentierade korrekt mellan vildtyp och mutant, men kunde inte identifiera olika mutationstyper.
Macrolide-R/MG ELITe MGB
®Kit (ELITechGroup)
Macrolide-R/MG ELITe MGB (Macrolide-R/MG) är en realtidsamplifiering som en del i systemet ELITe InGenius, vilket är ett automatiserat system för extraktion, amplifiering, detektion och resultattolkning. Amplifieringen görs av 23S rRNA-genen i M. genitalium och två specifika prober används för detektion. En probe identifierar de huvudsakliga mutationerna för makrolidresistens, i positionerna A2058 och A2059 genom smältpunktsanalys. Proberna är utvecklade av ELITechGroup och har specifika funktioner som ger ökad sensitivitet och specificitet (24).
Endast en studie, av Braam et al. (25), har testat detta kit och jämfört mot sekvenserade prover efter standard qPCR eller reverse transcriptase nested (RTN) qPCR. Totalt testades 318 prover och av dessa var 236 positiva för M. genitalium. En rutinmetod för detektion av M. genitalium (qPCR mot MgPa) detekterade 196 av dessa (83,1%). Macrolide-R/MG detekterade 202 (85,6%). 51 prover hade enligt sekvensering makrolidresistensassocierade mutationer, samtliga detekterades av kitet.
RealAccurate
®TVMG
RES(Pathofinder)
RealAccurate TVMGRES (RealAccurate) är en multiplex qPCR som detekterar infektion av Trichomonas
vaginalis och M. genitalium samt mutationer i A2058/A2059 i 23S rRNA i M. genitalium. Detektion
av resistensmutationer sker med ”Molecular beacon”-prober. En beacon-probe är anpassad för detektion av SNPs genom att ha signifikant högre specificitet än traditionella hybridiseringsprober (26). Kitet har i en studie av Le Roy et al. (27) jämförts mot två andra kommersiella kit; ResistancePlus MG och S-DiaMGRes, samt referensmetoder. För detektion av M. genitalium användes qPCR mot MgPa som referensmetod och för resistensdetektion användes amplifiering och sekvensering av 23S rRNA genen. 195 prover positiva för M. genitalium testades, varav 188 detekterades av RealAccurate. Då inga negativa M. genitalium var inkluderade, kunde inget värde på specificiteten för detektion av M.
11
ResistancePlus
®MG (SpeeDx)
ResistancePlus MG är en multiplex qPCR. Metoden detekterar M. genitalium och de fem mutationerna i 23S rRNA genen som är associerade med makrolidresistens (position A2058 och A2059) (28). Metoden bygger på principen PlexPCR®, som är utvecklat av SpeeDx. Metoden ger ökad specificitet och
sensitivitet tack vare specialdesignade primers och oligos (29, 30).
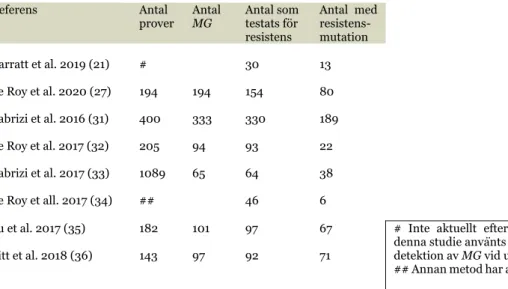
Åtta studier som har utvärderat ResistancePlus MG har jämfört resultat från kitet mot en referensmetod (21, 27, 31-36). I två av dessa (21, 34) har endast detektion av resistens utvärderats. I studien av Le Roy et al. (34) har en annan metod använts för detektion av M. genitalium och i studien av Barratt et al. (21) är ResistancePlus MG referensmetod för utvärdering av en annan metod vid detektion av M. genitalium. I en annan studie av Le Roy et al. (27) har endast känt positiva M. genitalium testats, vilket innebär att denna studie inte ger något värde på metodens specificitet med avseende på detektion av M. genitalium. Samtliga studiers resultat har sammanställts för att få sammanfattande värden för sensitivitet, specificitet och konkordans, som alla är >95% och kan jämföras mot andra metoders värden i Tabell 3. Hur många prover som testats i respektive studie finns presenterat i Tabell 4
Tabell 4. Antal prover vid utvärdering av ResistancePlus® MG (SpeeDx). Enskilda värden av hur många prover som testats i de studier som utvärderat ResistancePlus MG. (MG = M. genitalium)
Referens Antal
prover Antal MG Antal som testats för resistens Antal med resistens-mutation Barratt et al. 2019 (21) # 30 13 Le Roy et al. 2020 (27) 194 194 154 80 Tabrizi et al. 2016 (31) 400 333 330 189 Le Roy et al. 2017 (32) 205 94 93 22 Tabrizi et al. 2017 (33) 1089 65 64 38 Le Roy et all. 2017 (34) ## 46 6
Su et al. 2017 (35) 182 101 97 67 # Inte aktuellt eftersom ResistancePlus MG i denna studie använts som referensmetod för Pitt et al. 2018 (36) 143 97 92 71 detektion av MG vid utvärdering av ett annat kit.
## Annan metod har använts för detektion av MG
Murray et al. (37) har utvärderat kompabilitet mellan kitet och en annan typ av buffert vid provtagning. Det gällde provtagning som görs med Hologic Aptima för testning för Chlamydia trachomatis och
Neisseria gonorrhoeae. Konkordansen vid detektion av M. genitalium med Aptimabuffertprover
jämfört med standardbuffertprover är 97,9% och vid detektion av makrolidresistens 98,9%. Studien antyder också att prover tagna i Aptimabuffert eventuellt kan ge bättre resultat. I studien bedöms fyra prover tagna i Aptimabuffert ha resistensmutation, men samma prover tagna i standardbuffert bedöms som vildtyp. Sekvensering av dessa prover resulterade i tre mutanter och en vildtyp. Resultatet för prover tagna i Aptimabuffert var korrekt i tre av fyra fall (75%), medan resultat för prover tagna i standardbuffert endast var korrekt i ett av fyra fall (25%).
Det finns också en studie presenterad av Murray et al. (38) som visar på ytterligare ett användningsområde för kitet. Eftersom bakteriebörda ofta korrelerar med symtom och behandlingseffektivitet, föreslås att kitet kan användas för att mäta bakteriebörda hos en patient. Hög börda har exempelvis associerats med behandlingssvikt med azitromycin. I denna studie har också metoden upprepats två gånger med samma prover (n=39), vilket visade stark korrelation (r=0,858 mellan test ett och två, samt r=0,892 mellan test ett och tre). I studien har inte resultatet jämförts mot referensmetod och presenterar därmed inga värden för sensitivitet och specificitet.
12
ResistancePlus® MG FleXible (SpeeDx)
Två studier (39, 40) har utvärderat prestandan för den version av ResistancePlus MG som utvecklats för GeneXpert, ResistancePlus® MG FleXible (FleXible). Anledningen till att detta kit har utvecklats är
fördelen med mer patientnära tester, vilket är möjligt med GeneXpert. GeneXpert är en snabb metod som i ett instrument renar ett prov, amplifierar och detekterar med qPCR samt rapporterar resultat (40). I studien av Sweeney et al. (39) har resultatet jämförts mot standardutförande med ResistancePlus MG (n=179, varav 63 positiva för M. genitalium). Sensitiviteten och specificiteten för detektion av M.
genitalium var 96,8% respektive 100%. Konkordansen var 98,9%. När det gäller detektion av
makrolidresistens stämde alla resultat överens med referensmetoden (n=43). Det testades även flera spädningar med känt positiva M. genitalium-prover, där FleXible kunde detektera tillförlitligt i ytterligare en tiospädning jämfört med standardmetoden.
Den andra studien, av Drud et al. (40), har jämfört resultatet från FleXible med TaqMan qPCR mot
MgPa och sekvensering av 23S rRNA. I GeneXpert finns olika matriser som kan användas beroende på
provmaterial. För urinprover (urinmatris) stämde resultatet från FleXible överens med referensmetoderna till 97,5% för detektion av M. genitalium och till 100% för detektion av makrolidresistens (n=40, varav tio positiva för M. genitalium med resistensmutation och tio vildtyp). När swabprover testades (swabmatris) var konkordansen 97,5% för detektion av M. genitalium och 92,7% för detektion av makrolidresistens (n=120, varav 55 positiva för M. genitalium (29 mutanter och 26 vildtyp)). Om samtliga testade prover läggs ihop blev konkordansen 98% för detektion av M.
genitalium och 94,6% för detektion av makrolidresistens.
S-DiaMGRes
TM(Diagenode)
S-DiaMGRes är en qPCR som är designad för detektion och identifiering av de fem vanligaste makrolidresistensmutationerna, efter detektion av M. genitalium med annan metod, företaget föreslår S-DiaMGTVTM (Diagenode). I amplifieringen används primers som passar för både vildtyp och
mutanter, medan prober ger detektionsspecificitet (41).
Le Roy et al. (27) har jämfört kitet mot två andra kit och referensmetod; ResistancePlus MG, RealAccurate TVMGRES och amplifiering och sekvensering av 23S rRNA genen. Verifiering av förekomst
av M. genitalium (n=195) har gjorts genom qPCR mot MgPa. Det amplikon som S-DiaMGRes använder för detektion av mutationer kan även användas för detektion av M. genitalium, där 94,8% av de kända proverna identifieras som M. genitalium. Eftersom inga negativa prover har testats går det inte att säga något om metodens specificitet gällande detektion av M. genitalium. Sensitivitet, specificitet och konkordans för detektion av makrolidresistens (n=154, 80 mutanter och 74 vildtyp) var hög, >97%. I en studie av Thellin et al. (42) har en prototyp för S-DiaMGRes utvärderats, där 43 M. genitalium-positiva prover bedömts med pyrosekvensering som referens. I studien har M. genitalium detekterats med primers och prober från S-DiaMGTVTM kitet (Diagenode, Belgien) med en sensitivitet på 95%.
Eftersom det är kitet som används för detektion av makrolidresistens (S-DiaMGRes) som utvärderas i denna litteraturstudie är det utvärderingen av detektion av makrolidresistens som studerats. I Tabell 3 presenteras en sammanlagd, tillsammans med studien av Le Roy et al. (27), sensitivitet, specificitet och konkordans för makrolidresistens.
Diskussion
Syftet med studien var att genom en litteraturstudie kartlägga och jämföra kommersiella kit som påvisar
M. genitalium och makrolidresistens eller enbart makrolidresistens. Detta gjordes för att ge
Laboratoriemedicin på Ryhov ett underlag för att välja metod för detektion av makrolidresistens vid implementering i rutindiagnostiken. Som poängteras i flera studier (3, 23, 27, 31, 33, 36) och i europeiska riktlinjer från 2016 (2) är det viktigt att upptäcka eventuell makrolidresistens för att kunna ge behandling som mer sannolikt är effektiv, samt att minska utvecklingen av makrolidresistens. Att det finns enkla och snabba metoder för detektion av både M. genitalium och makrolidresistens, som också är pålitliga, är därför avgörande.
Samtliga värden för sensitivitet, specificitet och konkordans tyder på att alla identifierade kommersiella kit har bra prestanda. På grund av begränsningen av antal publikationer kan dock resultatet från denna studie endast ligga till grund för huruvida ResistancePlus MG är ett bra metodval eller inte.
13
Resultatdiskussion
Sensitivitet och specificitetAlla utvärderade kommersiella kit har godkänd prestanda, där sensitivitet för detektion av M.
genitalium ligger mellan 85,6–100% och specificiteten är 100% i de fall där den testats (99,8% i samlat
värde för ResistancePlus MG). Den lägre sensitiviteten (85,6%) ses för Macrolide-R/MG och beror sannolikt på att resultatet från kitet har jämförts mot extra effektiv amplifiering i form av RTN qPCR, där DNA mängden i ett prov först ökats genom att skapa cDNA av rRNA vilket följts av nested qPCR som ökat mängden DNA ytterligare. Som beskrivs i resultatet detekterade Macrolide-R/MG fler positiva prover än den rutinmetod (qPCR mot MgPa) som användes, 85,6 % jämfört mot 83,1%.
När det gäller detektion av makrolidresistens ligger kitens sensitivitet mellan 76,9%-100% och specificiteten mellan 96,3%-100%. Den lägre sensitiviteten (76,9%) ses för Allplex och kan bero på att det här endast testats 13 mutanter varav Allplex detekterade tio. I samma studie detekterade ResistancePlus MG elva mutanter (84,6%) vilket inte heller är ett högt värde, i jämförelse med det sammanlagda sensitivitetsvärdet för ResistancePlus MG som ligger på 95,5%. För en tydligare utvärdering av Allplex skulle därmed fler prover behöva testas.
I två studier (23, 27) har endast positiva M. genitalium testats vilket innebär att det i de studierna inte går att säga något om metodernas specificitet för detektion av M. genitalium. Specificitet är en viktig aspekt vid val av metod och att testa detta är därför nödvändigt. Nya och flera tester som inkluderar negativa prover skulle behövas. Det är också skillnad på negativa prover, där olika studier har använt olika typer av negativa prover. De flesta studierna har använt kliniska prover som inte är positiva för M.
genitalium, och okänt om de är positiva för andra patogener eller inte. Andra studier (36, 40) har valt
ut prover som är positiva för specifika patogener som kan finnas i ett urin- eller swabprov, men negativa för M. genitalium. Styrkan på värdet för specificitet är högre i de studier där andra patogener använts som negativa, men samtidigt är kliniska prover mer likt verkligheten. I studien av Tabrizi et al. (33) testades 1024 negativa prover som samtliga gav negativt resultat. Det stora antalet som testats ger en hög styrka på det höga specificitetsvärdet för metoden (ResistancePlus MG).
När det gäller sensitivitet har den testats genom att bedöma hur stor andel positiva eller muterade som detekteras. I de fall där makrolidresistensen inte detekteras kommer patienter sannolikt behandlas med azitromycin utan effekt, därför är ett så högt sensitivitetsvärde som möjligt önskvärt. Hur svaga prover som kan detekteras har testats i några av studierna, men där ges inga entydiga resultat och därför skulle nya studier behövas för att säkerställa detektionsgränser. Flera studier tar upp i diskussion att de prover som inte gett resultat i de allra flesta fall har varit väldigt svaga och legat nära detektionsgräns även för referensmetoderna.
AllplexTM MG & AziR (Seegene)
Allplex har endast utvärderats i en publicerad studie (21), vilket betyder att det inte går att dra några slutsatser om dess prestanda. Eftersom ResistancePlus MG användes som referensmetod för detektion av M. genitalium är inte heller detektionen av M. genitalium jämförbar mot andra studiers resultat som har haft qPCR mot målgener i M. genitalium som referensmetod.
I studien detekterar Allplex fler M. genitalium än ResistancePlus MG, vilket tyder på att Allplex kan vara en mer känslig metod. För att styrka detta behövs dock flera studier där resultatet även jämförs mot annan referensmetod, exempelvis qPCR mot någon målgen i M. genitalium, samt inkluderar svaga prover i studien.
LightMix® Modular M. genitalium + Macrolide (TIB Molbiol)
För LightMix finns endast en studie som beskriver en föregångare till kitet (23). Det finns därmed inga studier som kan användas för att utvärdera det egentliga kitet. Resultatet från föregångaren visar dock på att metodprincipen har hög sensitivitet och specificitet.
I metoden används smältkurvsanalys för att bedöma förekomst av resistensassocierade mutationer. Denna metod kan inte alltid bestämma vilken mutation som finns. Om en studie ska genomföras för att bedöma förekomst av de olika mutationstyperna är därmed inte detta kit att rekommendera, men för detektion av resistens så räcker det om resultatet bli resistent eller känslig.
14
Macrolide-R/MG ELITe MGB® Kit (ELITechGroup)
Enligt metodbeskrivningen (24) ska kitet Macrolide-R/MG användas i det automatiserade systemet ELITe InGenius®. Detta gjordes inte i studien av Braam et al. som utvärderat metoden (25), vilket
betyder att det kommersiella kit som finns tillgängligt nu är en nyare version. Om metodens prestanda har förbättrats kan inte avgöras eftersom det inte finns några studier publicerade. En aspekt som bör tas i beaktande är just det att detta kit är del i ett automatiserat system, vilket innebär att en större del av proceduren måste anpassas till en ny metod vid implementering.
Liksom LightMix använder Macrolide-R/MG smältkurvsanalys för att bedöma förekomst av resistensassocierade mutationer och har därmed samma begränsning i att bestämma mutationstyp.
RealAccurate® TVMGRES (Pathofinder)
Eftersom kitet endast utvärderas i en studie (27) så kan inga slutsatser dras om kitets prestanda, dock visar resultatet i studien på en relativt hög konkordans. RealAccurate skiljer sig mot de andra kiten genom att den endast detekterar fyra mutationer (26). Det detekterar inte mutationen A2059C, vilket är en ovanlig mutation, men det kan ändå innebära att resistens missas.
ResistancePlus® MG (SpeeDx)
Sammanställningen av resultaten från de studier som utvärderat ResistancePlus ger höga värden (>95%) för sensitivitet, specificitet och konkordans för både detektion av M. genitalium och detektion av makrolidresistens. Den totala konkordansen, när samtliga prover som testats i de olika studierna lades ihop, både för detektion av M. genitalium och makrolidresistens, blev 98,5%. Totalt hade 2925 test utförts i dessa studier, vilket ger en styrka i värdet med 98,5% konkordans. Detta resultat tyder på att ResistancePlus MG är ett bra val.
Att kitet verkar fungera bra när annan typ av provtagningsbuffert används (Aptima) är bra. Det innebär att prover som tagits för testning av C. trachomatis och N. gonorrhoeae även kan testas för M.
genitalium. Studien visar också på bra hållbarhet i Aptimabuffert.
Versionen FleXible, som utvecklats för GeneXpert, visar på väl överensstämmande resultat jämfört både mot ResistancePlus MG (39) och mot annan referensmetod (40). Dessutom visar båda studierna att denna metod har lägre detektionsgräns än standardmetoden. Det är en snabb metod som inkluderar alla moment från prov till resultat. Detta är ett bra alternativ, men kräver ett nytt instrument och sannolikt blir varje test dyrare än det traditionella kitet.
S-DiaMGResTM (Diagenode)
S-DiaMGResär endast framställd för detektion av mutationer associerade med makrolidresistens. Detta innebär att det krävs två olika kit, ett för detektion av M. genitalium och S-DiaMGRes för detektionen av resistensen. Detta påverkar både kostnadseffektiviteten och tidsförbrukningen vid arbetet med diagnostisering. Sensitiviteten och specificiteten för kitet är hög, men det finns endast en studie där det färdiga kitet har använts vilket gör värdena mindre pålitliga.
Metoddiskussion
Vid omställning till litteraturstudie fick syftet modifieras från att laborativt testa tre kommersiella kit till att genom en litteraturstudie kartlägga och jämföra kommersiella kit som påvisar M. genitalium och makrolidresistens eller enbart makrolidresistens. Vid artikelsökningen användes två olika databaser vilket stärker resultatet då det resulterade i ett större utbud av publikationer. Förhoppningen var att det skulle finnas många publicerade studier, men eftersom det är relativt nya kit så var utbudet väldigt begränsat. Den äldsta publikationen i resultatet är från 2016, vilket betyder att resultatet är aktuellt i forskningssammanhanget. Begränsningen i antal publicerade och refereegranskade artiklar innebar att kriterierna för inkludering fick sänkas. Trots detta beslutades att studien skulle fortgå då den ansågs kunna bidra med relevant information för metodval och för framtida studier. För att få ihop flera studier inkluderades tre letters och en vetenskaplig poster. Detta ger inte litteraturstudiens resultat en stark vetenskaplig grund, men det kan ändå ge indikationer på vilka kit som är bra och hur nya utvärderingar kan göras.
Att flera av kiten inte berörs i mer än en publikation, varav ett kit endast har en föregångares resultat att luta sig mot, ger inte litteraturstudien styrka i just jämförelse mellan metoder. ResistancePlus MG har utvärderats i flera studier och därmed kan resultat för denna metod användas för att dra slutsatser om dess prestanda. I övrigt har litteraturstudien främst inneburit en sammanställning av de olika kommersiella kiten och förslag på viktiga aspekter att tänka på vid utvärdering av denna typ av metoder.
15
Det går att få en uppskattning om hur bra de andra kiten presterar, men för att kunna göra en jämförelse mellan kiten behövs fler studier. Med de resultat som finns får ResistancePlus MG bra värden och är definitivt ett bra val, men dessvärre ges inte övriga kit någon chans på grund av bristande information. Den laborativa utvärdering som var tänkt att utföras kan med fördel planeras för att få ett mer utbrett underlag för att välja metod.
Studiens validitet styrks genom att medelvärdet på kvalitetspoäng för publikationerna är 11,3 (86,9%), varav elva publikationer har hög kvalitet (11–13 poäng) och fyra ligger på gränsen till hög kvalitet (10– 10,5 poäng), se Bilaga 2. Bristen på flera studier som utvärderar de olika kiten innebär att de resultaten inte kan få en evidensgrad. Där det finns flera studier, för ResistancePlus MG, anses evidensgraden vara hög eftersom studierna med högt bevisvärde visar på liknande resultat.
Det är svårt att jämföra värden mellan metoderna eftersom de inte har testats på samma prover och framför allt eftersom det inte gjorts flera studier. En studie kan ha haft många mycket svagare prover, det vill säga liten mängd DNA, och därför har detektion inte kunnat göras och värdet för sensitivitet har blivit lägre än om det hade testats endast på starka prover. Metoderna kan också utföras på olika provmaterial vilket eventuellt kan påverka hur resultatet blir. Detta har inte tagits hänsyn till i denna studie eftersom de flesta studier som har granskats inte har gjort skillnad på resultat från olika provmaterial. För att utvärdera hur olika provmaterial påverkar resultatet behöver nya studier göras. För utvärdering av dessa typer av metoder bör kiten jämföras mot samma referensmetod. Det är en fördel om flera kit kan utvärderas samtidigt med samma prover och det är viktigt att även svaga prover inkluderas i studierna, samt både positiva och negativa prover.
I en studie av Le Roy et al. (34) där ResistancePlus MG har utvärderats fanns endast sex mutanter, vilket är väldigt få och ger svag styrka för resultatet. Detta beror på att fokus i studien var detektion av M.
genitalium med annan metod. När detta resultat sammanställs med övriga studier på ResistancePlus
MG blir svagheten dock försumbar, vilket visar på betydelsen av flera studier.
Slutsats
I denna litteraturstudie, har fem kommersiella kit för detektion av M. genitalium och makrolidresistens, samt ett kit för enbart detektion av makrolidresistens hos M. genitalium, identifierats. En vetenskaplig jämförelse har inte kunnat göras mellan metoderna eftersom det inte finns tillräckligt med publicerade studier. Den metod som har utvärderats i flera studier, ResistancePlus MG, har den högsta totala konkordansen som omfattar både detektion av M. genitalium och makrolidresistens, och är enligt litteraturstudiens sammanställning ett tillförlitligt kit.
ResistancePlus MG är ett beprövat kit och baserat på litteraturstudien är ResistancePlus MG ett bra metodval för implementering på Laboratoriemedicin på Ryhov. Dock skulle en laborativ jämförelse med Allplex MG & AziR kunna vara av intresse, då Allplex indikerades ha högre sensitivitet för detektion av
M. genitalium. LightMix Modular M. genitalium + Macrolide har inte testats tillräckligt och skulle också
kunna inkluderas i jämförelsen, eftersom företaget bakom LightMix, TIB Molbiol, redan levererar andra analyser till Laboratoriemedicin.
16
Referenser
Artiklar med * ingår i resultatet.
1. Murray PR, Rosenthal KS, Pfaller MA. Medical microbiology. Philadelphia, PA: Elsevier; 2016. 2. Jensen JS, Cusini M, Gomberg M, Moi H. 2016 European guideline on Mycoplasma genitalium
infections. J Eur Acad Dermatol Venereol. 2016;30(10):1650-6.
3. Hadad R, Golparian D, Lagos AC, Ljungberg J, Nilsson P, Jensen JS, et al. Macrolide and fluoroquinolone resistance in Mycoplasma genitalium in two Swedish counties, 2011-2015. Apmis. 2018;126(2):123-7.
4. Läkemedelsverket. Sexuellt överförbara bakteriella infektioner – behandlingsrekommendation 2015 [2020-02-28] Hämtad från: http://www.lakemedelsverket.se/globalassets/dokument/ behandling-och-forskrivning/behandlingsrekommendationer/behandlingsrekommendation/ behandlingsrekommendation-sexuellt-overforbara-bakteriella-infektioner.pdf.
5. Jensen JS, Bradshaw CS, Tabrizi SN, Fairley CK, Hamasuna R. Azithromycin treatment failure in Mycoplasma genitalium-positive patients with nongonococcal urethritis is associated with induced macrolide resistance. Clin Infect Dis. 2008;47(12):1546-53.
6. Lis R, Rowhani-Rahbar A, Manhart LE. Mycoplasma genitalium infection and female reproductive tract disease: a meta-analysis. Clin Infect Dis. 2015;61(3):418-26.
7. Gnanadurai R, Fifer H. Mycoplasma genitalium: A Review. Microbiology. 2020;166(1):21-9. 8. Munson E. Molecular Diagnostics Update for the Emerging (If Not Already Widespread) Sexually
Transmitted Infection Agent Mycoplasma genitalium: Just About Ready for Prime Time. J Clin Microbiol. 2017;55(10):2894-902.
9. Bradshaw CS, Jensen JS, Waites KB. New Horizons in Mycoplasma genitalium Treatment. J Infect Dis. 2017;216(suppl_2):S412-s9.
10. Vazquez-Laslop N, Mankin AS. How Macrolide Antibiotics Work. Trends Biochem Sci. 2018;43(9):668-84.
11. Bissessor M, Tabrizi SN, Twin J, Abdo H, Fairley CK, Chen MY, et al. Macrolide resistance and azithromycin failure in a Mycoplasma genitalium-infected cohort and response of azithromycin failures to alternative antibiotic regimens. Clin Infect Dis. 2015;60(8):1228-36.
12. Mast Y, Wohlleben W. Streptogramins - two are better than one! International journal of medical microbiology : IJMM. 2014;304(1):44-50.
13. Pfister P, Jenni S, Poehlsgaard J, Thomas A, Douthwaite S, Ban N, et al. The structural basis of macrolide-ribosome binding assessed using mutagenesis of 23S rRNA positions 2058 and 2059. J Mol Biol. 2004;342(5):1569-81.
14. Jensen JS. Protocol for the detection of Mycoplasma genitalium by PCR from clinical specimens and subsequent detection of macrolide resistance-mediating mutations in region V of the 23S rRNA gene. Methods Mol Biol. 2012;903:129-39.
15. Waites KB, Xiao L, Paralanov V, Viscardi RM, Glass JI. Molecular methods for the detection of Mycoplasma and ureaplasma infections in humans: a paper from the 2011 William Beaumont Hospital Symposium on molecular pathology. J Mol Diagn. 2012;14(5):437-50.
16. Heavey E. Mycoplasma genitalium. Nursing2020. 2017;47(7).
17. Kristiansen GQ, Lisby JG, Schonning K. A 5' Nuclease Genotyping Assay for Identification of Macrolide-Resistant Mycoplasma genitalium in Clinical Specimens. J Clin Microbiol. 2016;54(6):1593-7.
18. Twin J, Jensen JS, Bradshaw CS, Garland SM, Fairley CK, Min LY, et al. Transmission and selection of macrolide resistant Mycoplasma genitalium infections detected by rapid high resolution melt analysis. PLoS One. 2012;7(4):e35593.
19. Forsberg C, Wengström Y. Att göra systematiska litteraturstudier : värdering, analys och presentation av omvårdnadsforskning. Stockholm: Natur & kultur; 2016.
20. Seegene Inc. Allplex™ MG & AziR Assay [2020-05-04].
Hämtad från: http://www.seegene.com/assays/allplex_mg_n_azir_assay.
21. * Barratt A, Gifford L, Jones S, Spiller O, Moore C. The use of Seegene's Allplex™ MG & AziR assay for the detection of Mycoplasma genitalium and macrolide resistance in Wales. STI & HIV 2019 World Congress, Vancouver. 2019.
22. TIB Molbiol. Instructions for use: LightMix ® Modular M. genitalium + Macrolide V190123. Berlin:
Roche (www.lifescience.roche.com); 2019.
23. * Gossé M, Lysvand H, Pukstad B, Nordbø SA. A Novel SimpleProbe PCR Assay for Detection of Mutations in the 23S rRNA Gene Associated with Macrolide Resistance in Mycoplasma genitalium in Clinical Samples. Journal of clinical microbiology. 2016;54(10):2563-7.
17
24. ELITechGroup. Macrolide-R/MG ELITe MGB® Kit 2019 [2020-04-28]. Hämtad från: https://www.elitechgroup.com/wp-content/uploads/sites/16/2020/01/SCH-mRTS401ING-48_en_00.pdf.
25. * Braam JF, van Marm S, Severs TT, Belousov Y, Mahoney W, Kusters JG. Sensitive and specific assay for the simultaneous detection of Mycoplasma genitalium and macrolide resistance-associated mutations. Eur J Clin Microbiol Infect Dis. 2018;37(11):2137-44.
26. PathoFinder. RealAccurate® TVMGRES PCR Kit -Instructions for use v.1.0 2018 [2020-05-04 ]. Hämtad från: https://kaldur.landspitali.is/focal/gaedahandbaekur/gnhsykla.nsf/5e27f2e5a88c89 8e00256500003c98c2/85a82540dbc0dc4d0025846d003249df/$FILE/Pathofinder%20instructi ons%20for%20use.pdf.
27. * Le Roy C, Bébéar C, Pereyre S. Clinical Evaluation of Three Commercial PCR Assays for the Detection of Macrolide Resistance in Mycoplasma genitalium. Journal Of Clinical Microbiology. 2020;58(2).
28. Tabrizi SN, Tan LY, Walker S, Twin J, Poljak M, Bradshaw CS, et al. Multiplex Assay for Simultaneous Detection of Mycoplasma genitalium and Macrolide Resistance Using PlexZyme and PlexPrime Technology. PLoS One. 2016;11(6):e0156740.
29. SpeeDx. PlexPrime ® 2019 [2020-03-27].
Hämtad från: https://plexpcr.com/technology/plexprime. 30. SpeeDx. PlexZyme® 2019 [2020-03-27].
Hämtad från: https://plexpcr.com/technology/plexzyme.
31. * Tabrizi SN, Tan LY, Walker S, Twin J, Poljak M, Bradshaw CS, et al. Multiplex Assay for Simultaneous Detection of Mycoplasma genitalium and Macrolide Resistance Using PlexZyme and PlexPrime Technology. PLoS One. 2016;11(6):e0156740.
32. * Le Roy C, Hénin N, Bébéar C, Pereyre S. Evaluation of a Commercial Multiplex Quantitative PCR (qPCR) Assay for Simultaneous Detection of Mycoplasma genitalium and Macrolide Resistance-Associated Mutations in Clinical Specimens. Journal of clinical microbiology. 2017;55(3):978-9. 33. * Tabrizi SN, Su J, Bradshaw CS, Fairley CK, Walker S, Tan LY, et al. Prospective Evaluation of
ResistancePlus MG, a New Multiplex Quantitative PCR Assay for Detection of Mycoplasma genitalium and Macrolide Resistance. J Clin Microbiol. 2017;55(6):1915-9.
34. * Le Roy C, Pereyre S, Hénin N, Bébéar C. French Prospective Clinical Evaluation of the Aptima Mycoplasma genitalium CE-IVD Assay and Macrolide Resistance Detection Using Three Distinct Assays. Journal of clinical microbiology. 2017;55(11):3194-200.
35. * Su JP, Tan LY, Garland SM, Tabrizi SN, Mokany E, Walker S, et al. Evaluation of the SpeeDx ResistancePlus MG Diagnostic Test for Mycoplasma genitalium on the Applied Biosystems 7500 Fast Quantitative PCR Platform. Journal of clinical microbiology. 2017;56(1).
36. * Pitt R, Cole MJ, Fifer H, Woodford N. Evaluation of the Mycoplasma genitalium Resistance Plus kit for the detection of M. genitalium and mutations associated with macrolide resistance. Sexually transmitted infections. 2018;94(8):565-7.
37. * Murray GL, Danielewski J, Bradshaw CS, Williamson DA, Birnie J, Su JP, et al. Performance of the ResistancePlus MG diagnostic test for Mycoplasma genitalium using samples collected with Hologic Aptima Specimen Collection kits. Journal of medical microbiology. 2020;69(2):244-8. 38. * Murray GL, Danielewski J, Bodiyabadu K, Machalek DA, Bradshaw CS, Costa A-M, et al. Analysis
of Infection Loads in Mycoplasma genitalium Clinical Specimens by Use of a Commercial Diagnostic Test. Journal of clinical microbiology. 2019;57(9).
39. * Sweeney EL, Mhango LP, Ebeyan S, Tan LY, Bletchly C, Nimmo GR, et al. Evaluation of the ResistancePlus MG FleXible Cartridge for Near-Point-of-Care Testing of Mycoplasma genitalium and Associated Macrolide Resistance Mutations. Journal of clinical microbiology. 2020;58(3). 40. * Drud ST, Njuguna P, Ebeyan S, Erskine S, Holm M, Johansson SC, et al. Evaluation of the
ResistancePlus MG FleXible Assay for Detection of Wild-Type and 23S rRNA-Mutated Mycoplasma genitalium Strains. Journal of clinical microbiology. 2020;58(3).
41. Diagnostics D. Mycoplasma genitalium and Macrolide Resistance, S-DiaMGRes™ 2017 [2020-05-04]. Hämtad från: https://www.diagenodediagnostics.com/products/s-diamgres.
42. * Thellin O, Elmoualij B, Zorzi W, Jensen JS, Close R, Deregowski V, et al. Four-color multiplex real-time PCR assay prototype targeting azithromycin resistance mutations in Mycoplasma genitalium. BMC infectious diseases. 2019;19(1):827.
18
Bilagor
Bilaga 1. Protokoll för kvalitetsbedömning av utvalda publikationer Bilaga 2. Sammanfattning/översikt av publikationer
19
Bilaga 1. Protokoll för kvalitetsbedömning av utvalda publikationer
Titel: __________________________________________________________________ Författare: ______________________________________________________________ Årtal: _________ Tidskrift: _________________________________________________
För att publikationen ska inkluderas i fortsatt granskning ska dess syfte vara relevant för examensarbetet. Utvärderas en eller flera metod/er som är relevanta för examenarbetet? □ Ja (fortsätt granskning) □ Nej (exkludera)
1. Är hypoteser, syfte och eventuella frågeställningar klart beskrivna? □ Ja (1 p) □ Nej (0 p)
2. Har urvalet redovisats? □ Ja (1 p) □ Nej (0 p)
3. Var urvalet lämpligt med tanke på syftet? □ Ja (1 p) □ Nej (0 p)
4. Har etiska aspekter redovisats? □ Ja (1 p) □ Nej (0 p)
5. Är metoden tydligt beskriven? □ Ja (1 p) □ Nej (0 p)
6. Har lämplig referensmetod använts? □ Ja (1 p) □ Nej (0 p)
7. Är statistisk metod adekvat? □ Ja (1 p) □ Nej (0 p)
8. Är de viktigaste resultaten av studien tydligt beskrivna? □ Ja (1 p) □ Nej (0 p)
9. Svarar resultatet mot syftet? □ Ja (1 p) □ Nej (0 p)
10. Har man tagit hänsyn till eventuellt bortfall i resultatet? □ Ja (1 p) □ Nej (0 p)
11. Finns det risk att finansiella intressen eller andra bindningar kan ha påverkat resultatet? □ Ja (0 p) □ Nej (1 p)
12. Om ”ja” på fråga 11: Har författarna deklarerat att finansiella intressen eller andra bindningar inte har påverkat resultatet?
□ Ja (0,5 p) □ Nej (0 p) Sammanfattande bedömning
□ Bra (2 p) □ Medel (1 p) □ Dålig (0 p) Kommentar: ______________________________ Är resultatet relevant för examensarbetets syfte? □ Ja □ Nej (exkludera)
Om nej, kort motivering varför: ________________________________________________ Poäng: _______ Granskad av: ________________________________________________
20
Bilaga 2. Sammanfattning/översikt av publikationer sorterade efter tidskrift.
Kv.p = kvalitetspoäng, * = har inte angivit etiska överväganden
MG = detektion av M. genitalium
resistens = detektion av makrolidresistens Namn på
publikation
(typ av publikation)
Författare Å
r Kv.p Utvärderat Kit Metodtyp i kit Sensi-tivitet
MG resp. resistens Speci- ficitet MG resp. resistens Konkor- dans MG resp. resistens BMC Infect Dis Four-color multiplex real-time PCR assay prototype targeting azithromycin resistance mutations in Mycoplasma genitalium (42) (artikel) Thellin O, Elmoualij B, Zorzi W, Jensen JS, Close R, Deregowski V, Le Guern Fellous M, Quatresooz P 2 0 1 9 10,5 S-DiaMGRes (prototyp) (Diagenode) Multiplex qPCR 95% resp. 93,8% 100% resp. 100% 97,0% resp. 95%
Eur J Clin Microbiol Infect Dis
Sensitive and specific assay for the simultaneous detection of Mycoplasma genitalium and macrolide resistance-associated mutations (25) (artikel) Braam JF, van Marm S, Severs TT, Belousov Y, Mahoney W, Kusters JG 2 0 1 8 12,5 Macrolide-R/MG ELITe MGB® (Elitech) qPCR och smältkurvs-analys 85,6% resp. 100% 100% resp. 99,4% 89,3% resp. 99,5% J Clin Microbiol A Novel SimpleProbe PCR Assay for Detection of Mutations in the 23S rRNA Gene Associated with Macrolide Resistance in Mycoplasma genitalium in Clinical Samples (23) (artikel) Gossé M, Lysvand H, Pukstad B, Nordbø SA 2 0 1 6 13 Föregångare till LightMix® Modular M. genitalium + Macrolide (TIB Molbiol) qPCR och smältkurvs-analys 97,8% resp. 98,8% 85% resp. 96,3% 96,2% resp. 97,8% Evaluation of a Commercial Multiplex Quantitative PCR (qPCR) Assay for Simultaneous Detection of Mycoplasma genitalium and Macrolide Resistance-Associated Mutations in Clinical Specimens (32) (letter) Le Roy C, Hénin N, Bébéar C, Pereyre S 2 0 1 7 11,5 * ResistancePlus®
MG (SpeeDx) Multiplex qPCR 100% resp. 95,5% 99,1% resp. 95,8% 99,5 % resp. 95,7%
21 Namn på publikation (typ av publikation) Författare Å
r Kv.p Utvärderat Kit Metodtyp i kit Sensi-tivitet
MG resp. resistens Speci-ficitet MG resp. resistens Konkor- dans MG resp. resistens J Clin Microbiol Prospective Evaluation of ResistancePlus MG, a New Multiplex Quantitative PCR Assay for Detection of Mycoplasma genitalium and Macrolide Resistance (33) (artikel) Tabrizi SN, Su J, Bradshaw CS, Fairley CK, Walker S, Tan LY, Mokany E, Garland SM 2 0 1 7 11 ResistancePlus®
MG (SpeeDx) Multiplex qPCR 98,5% resp. 100% 100% resp. 96,2% 99,9% resp. 98,4% French Prospective Clinical Evaluation of the Aptima Mycoplasma genitalium
CE-IVD Assay and Macrolide Resistance Detection Using Three Distinct Assays (34) (artikel) Le Roy C, Pereyre S, Hénin N, Bébéar C 2 0 1 7 10 * ResistancePlus®
MG (SpeeDx) Multiplex qPCR Endast resistens: 66,7% Endast resistens: 95,2% Endast resistens: 95,7% Evaluation of the SpeeDx ResistancePlus MG Diagnostic Test for Mycoplasma genitalium on the Applied Biosystems 7500 Fast Quantitative PCR Platform (35) (letter) Su JP, Tan LY, Garland SM, Tabrizi SN, Mokany E, Walker S, Bradshaw CS, Read T, Murray GL 2 0 1 8 12 ResistancePlus®
MG (SpeeDx) Multiplex qPCR 98,0% resp. 92,5% 100% resp. 100% 98,9% resp. 94,8% Analysis of Infection Loads in Mycoplasma genitalium Clinical Specimens by Use of a Commercial Diagnostic Test (38) (artikel) Murray GL, Danielewski J, Bodiyabadu K, Machalek DA, Bradshaw CS, Costa AM, Birnie J, Garland SM 2 0 1 9 11,5 ResistancePlus®
MG (SpeeDx) Multiplex qPCR Har inte jämfört utförande mot referensmetod. Har testat om metoden kan användas för att mäta
bakteriebörda (load). Har testat reproducerbarhet med resultatet ”robust reproducerbarhet”.
Evaluation of the ResistancePlus® MG FleXible cartridge for near point-of-care testing of Mycoplasma Genitalium and associated macrolide resistance mutations (39) (letter) Sweeney EL, Mhango LP, Ebeyan S, Tan LY, Bletchly C, Nimmo GR, Whiley DM 2 0 2 0 10 ResistancePlus® MG FleXible (SpeeDx) Multiplex PCR på GeneXpert Jämförd mot Resistance Plus® MG (SpeeDx). 96,8% resp. 100% Jämförd mot Resistance Plus® MG (SpeeDx). 100% resp. 100% Jämförd mot Resistance Plus® MG (SpeeDx). 98,9% resp. 100%
22 Namn på publikation (typ av publikation) Författare Å
r Kv.p Utvärderat Kit Metodtyp i kit Sensi-tivitet
MG resp. resistens Speci-ficitet MG resp. resistens Konkor- dans MG resp. resistens J Clin Microbiol Clinical Evaluation of Three Commercial PCR Assays for the Detection of Macrolide Resistance in Mycoplasma genitalium (27) (artikel) Le Roy C, Bébéar C, Pereyre S 2 0 2 0 11 * ResistancePlus® MG (SpeeDx), S-DiaMGResTM (Diagenode) RealAccurate® TVMGres (Pathofinder) 3x Multiplex qPCR ResPlus: 95,4% resp 100% S-DiaMG: 94,8% resp 100% RealAccur: 96,4% resp 95% Inga MG-negativa → ingen specificitet för MG- detektion. Resistens: ResPlus: 94,6% S-DiaMG: 97,3% RealAccu: 97,3% Beräknas inte för detektion av MG. Resistens: ResPlus: 97,4% S-DiaMG: 98,7% RealAccu: 96,1% Evaluation of the ResistancePlus MG FleXible Assay for Detection of Wild-Type and 23S rRNA-Mutated Mycoplasma genitalium Strains (40) (artikel) Drud ST, Njuguna P, Ebeyan S, Erskine S, Holm M, Johansson SC, Tan LY, Jensen JS 2 0 2 0 11,5 ResistancePlus® MG FleXible (SpeeDx) Multiplex PCR på GeneXpert 96,1% resp. 92,1% 99,2% resp. 97,2% 98,0% resp. 94,6% J Med Microbiol Performance of the ResistancePlus MG diagnostic test for Mycoplasma genitalium using samples collected with Hologic Aptima Specimen Collection kits (37) (artikel) Murray GL, Danielewski J, Bradshaw CS, Williamson DA, Birnie J, Su JP, De Petra V, Tan LY, Wee R, Machalek DA, Read TRH, Garland SM 2 0 2 0 12 ResistancePlus®
MG (SpeeDx) Multiplex qPCR Annan buffert (Aptima) än rekom-menderad, jämförd mot standard-utförande. 92,9% resp. 100% Annan buffert än rekom-menderad, jämförd mot standard-utförande. 100% resp. 96,3% Annan buffert än rekom-menderad, jämförd mot standard-utförande. 97,9% resp. 98,9% PLoS ONE Multiplex Assay for Simultaneous Detection of Mycoplasma genitalium and Macrolide Resistance Using PlexZyme and PlexPrime Technology (31) (artikel) Tabrizi SN, Tan LY, Walker S, Twin J, Poljak M, Bradshaw CS, Fairley CK, Bissessor M, Mokany E, Todd AV, Garland SM 2 0 1 6 11,5 ResistancePlus®
MG (SpeeDx) Multiplex qPCR 99,1% resp. 97,4% 98,5% resp. 100% 99% resp. 98,5%
Sex Transm Infect
Evaluation of the
Mycoplasma genitalium
Resistance Plus kit for the detection of M. genitalium and mutations associated with macrolide resistance (36) (artikel) Pitt R, Cole MJ, Fifer H, Woodford N 2 0 1 8 10,5 * ResistancePlus®
MG (SpeeDx) Multiplex qPCR 94,9% resp. 90,1% 100% resp. 100% 96,5% resp. 92,4%