Postoperativt illamående och kräkning
bland patienter i dagkirurgi
En studie om följsamhet till rutin vid ett medelstort regionsjukhus i Sverige
Julia
Halatchev
Viktor Triumf
Specialistsjuksköterska, Anestesisjukvård 2017
Luleå tekniska universitet Institutionen för hälsovetenskap
Institutionen för hälsovetenskap Avdelningen för omvårdnad
Postoperativt illamående och kräkning bland patienter i
dagkirurgi
En studie om följsamhet till rutin vid ett medelstort regionsjukhus i Sverige
Postoperative nausea and vomiting among patients in
ambulatory surgery
A study in guideline adherence at a medium sized county hospital in Sweden
Julia Halatchev Viktor Triumf
Kurs: O7067H, Examensarbete 15hp Vårterminen 2017
Specialistsjuksköterskeprogrammet inriktning anestesisjukvård Handledare: Ulrica Strömbäck
2
Postoperativt illamående och kräkning bland patienter i
dagkirurgi
En studie om följsamhet till rutin vid ett medelstort regionsjukhus i Sverige
Julia Halatchev Viktor Triumf
Institutionen för hälsovetenskap
Luleå tekniska universitet
Abstrakt
Postoperativt illamående och kräkning är fortfarande ett vanligt förekommande problem i samband med anestesi. Förutom obehaget med detta finns även medicinska risker som aspiration av maginnehåll eller sårruptur. PONV går att förebygga till viss del med hjälp av läkemedel, pre-operativ riskskattning samt genom anpassad anestesimetod. Genom att göra en riskskattning kan personal uppskatta vilka patienter som ligger i riskzonen för PONV och därigenom anpassa behandlingen. Syftet med denna studie var att undersöka hur riktlinjerna för att riskbedöma och förebygga PONV följs vid en dagkirurgisk avdelning. Studien genomfördes som en prospektiv observationsstudie med en kvantitativ ansats. Sammanlagt deltog 49 patienter i studien. De fick svara på om de kände av illamående och/eller kräkningar 2 samt 4 timmar postoperativt. Datan analyserades sedan i Package for Social Science (SPSS). Resultatet visade att rutinen följdes i 63% av fallen och att förekomsten av PONV var på 16%. Slutsatser som kan dras ifrån detta är att rutinen för PONV följs i samma utsträckning som många andra rutiner inom hälso- och sjukvård och att förekomsten av PONV är som förväntat utifrån tidigare studier. Rutinen borde dock kunna följas i fler än 63% av fallen. Vidare forskning kring huruvida ökad följsamhet skulle kunna sänka förekomsten av PONV behövs.
Nyckelord: postoperativt illamående och kräkningar, postoperativ omvårdnad, kvantitativ, profylax, följsamhet till rutin.
Keywords: postoperative nausea and vomiting, postoperative caring, quantitative, prophylaxis, adherence to guideline
3
Innehållsförteckning
BAKGRUND ...4 Rational ... 8 SYFTE ...8 METODBESKRIVNING ...9 Design ... 9 Deltagare ... 9 Genomförande ... 9 Datainsamling ... 10 Dataanalys ... 10 Etiska överväganden ... 10 RESULTAT ...12 DISKUSSION ...14 Resultatdiskussion ... 14 Metoddiskussion ... 17 KONKLUSION ...19 REFERENSER ...20BILAGA 1: INFORMATIONSBREV TILL PATIENTEN SAMT BLANKETT FÖR SAMTYCKE ... 28
BILAGA 2: PROTOKOLL FÖR DATAINSAMLING ... 31
4
Bakgrund
Under 2015 genomfördes ca 820 000 operationer i Sverige vilket är en ökning med ca 20% sedan 2005 (Socialstyrelsen, 2015). Med varje operation finns det flera risker för patienten relaterat till både anestesin och kirurgin och Brenner och Kautz (2015) har identifierat åtta olika risker som kan uppstå vid eller efter en operation. Dessa risker inkluderar, skada från felaktigt utfört ingrepp eller felaktigt preparathantering, oavsiktlig nedkylning/uppvärmning, rubbningar i elektrolyt- och vätskebalansen till följd av perioperativa infusioner, tryck eller skada till följd av felaktig
positionering, desaturation och respiratoriska problem, postoperativa infektioner, smärta från operationen och postoperativt illamående/kräkning. I engelsk litteratur används begreppet postoperative naseau and vomiting (PONV) varför vi framledes i denna studie kommer att använda förkortningen PONV. Enligt Golembiewski och O’Brien (2002) är PONV den vanligaste postoperativa komplikationen. Hur vanligt förekommande det är varierar men ett flertal källor uppskattar att ca 30% av alla opererade patienter drabbas av detta om det inte förebyggs (Apfel et al., 1999; Blackburn & Spencer, 2009; Dienemann et al., 2012;
Golembiewski & O’Brien, 2002; Smith & Ruth-Sahd, 2016; Spencer, 2015). Enligt Dienemann et al. (2012) drabbas ca 70-80% av högriskpatienterna av PONV.
Definition av PONV
Enligt Smith och Ruth-Sahd (2016) definieras PONV som ett oönskat upplevt fysiologiskt svar på den kirurgiska processen i form av illamående, kräkning eller känsla av att behöva kräkas eller ulka. Blackburn och Spencer (2015) delar upp begreppet i två delar nausea (illamående) och vomiting (kräkning). Där definieras illamående som en känsla eller upplevelse av att behöva kräkas som kan inkludera aktivering av centrala, sympatiska och parasympatiska mekanismer. Kräkning definieras som en ofrivillig uppkastning av maginnehåll som sker genom autonom gastrointestinal och respiratorisk aktivitet. Kräkning kan delas upp i två delar, pre-ejektionsfasen och ejektionsfasen. Under pre-ejektionsfasen sker en aktivering av sympatiska nervsystemet som medför takypné, takykardi, hypertension, svettning och blekhet. Vid ejektionsfasen stänger sig epiglottis och kraftiga kontraktioner i diafragma, bukmuskulatur och esophagus hjälper till att kasta upp innehåll från magsäcken och övre delen av duodenum.
5
Enligt Odom-Forren (2011) kan PONV delas in i olika delar, PONV, sen PONV, försenad PONV och PDNV (Post Discharge Nausea and Vomiting). Det råder en konsensus om att PONV sker inom de första 2 timmarna efter operationen. Illamående och kräkning som uppkommer 2-6 timmar efter operationen är sen PONV och illamående och kräkning som uppkommer senare än 6 timmar kallas försenad PONV. I tidigare studier finns ingen enhetlig tidsaspekt för PDNV utan allt illamående och kräkning som uppkommer efter att patienten blivit utskriven från sjukhuset definieras som PDNV oavsett hur lång tid som gått från operationen. Förekomsten PDNV är enligt Stewart (2013) högre än för PONV men de som drabbas av PDNV har i högre grad besvär av illamående än kräkning.
Risker vid PONV
PONV är ett stort obehag för patienten och vissa patienter är mer oroliga för att må illa och kräkas än för postoperativ smärta (Blackburn & Spencer, 2015; Lipp & Kaliappan, 2007). Förutom obehaget finns även allvarliga risker i form av aspiration, uttorkning, rubbningar i elektrolytbalansen, sårrupturer, ökat tryck i ögat och torax och esofagusruptur (Blackburn & Bhakta et al., 2016; Spencer, 2015). Enligt Berg (2010) kunde hälften av de dagkirurgiska patienterna inte återuppta normala dagliga sysslor på grund av PONV dagen efter operation.
Riskbedömning av PONV
Det finns idag väl utarbetade och validerade instrument för att i förväg upptäcka patienter som ligger i riskzonen för PONV. Ett vedertaget och vanligt förekommande instrument är Apfel-skalan. Apfel et al. (1999) identifierade fyra riskfaktorer för PONV; kvinnligt kön, icke-rökare, postoperativ administrering av opioider och tidigare episod av PONV och/eller åksjuka.
Enligt Mayeur et al. (2012) och Thomas, Jones och Strike (2002) är den förenklade Apfel-skalan ett enkelt och bra instrument för att upptäcka PONV. Med hjälp av denna är det möjligt att med PONV-profylax sänka incidensen även hos högriskpatienter (Apfel>2). Den förenklade Apfel-skalan ger ett poäng för varje förekommande riskfaktor som sedan summeras och ger ett värde mellan noll och fyra. Incidensen för PONV beroende på hur många riskfaktorer som finns är: 0 (10%), 1 (21%), 2 (39%), 3 (61%) och 4 (79%) (Apfel et al., 1999). Vissa sjukhus väljer att använda en annan variant av Apfel-skalan där ålder räknas in och post-operativt opioidbehov
6
exkluderas. Enligt Murphy et al. (2006) är låg ålder en associerad faktor med PONV men den är ändå inte lika bra på att förutse PONV som post-operativt opioid behov.
Fysiologi och behandling av PONV
Enligt Börjesson, Arweström, Baker och Berterö (2010) faller behandlingen av PONV ofta på sjuksköterskan och det är viktigt att sjuksköterskan har god kunskap om etiologin och
behandlingen kring PONV för att på bästa sätt kunna använda sina kunskaper för att anpassa behandlingen samt informera och stötta patienten. PONV är ett komplicerat problem då
illamående kan bero på en mängd olika orsaker och troligen finns det fler orsaker som ännu inte är helt kartlagda (Blackburn & Spencer, 2015). Det finns två områden i hjärnan som är centrala för illamående och kräkning, dessa är kräkcentrum och kemotriggerzonen. Kräkcentrum tar emot impulser från kranialnerver i innerörat, baroreceptorer i karotiskärlen, tryck- och sträckreceptorer i magtarmkanalen samt baroreceptorer i aortabågen. Det tar även emot signalen från andra
områden i hjärnan som behandlar smärta, rädsla, syn, förväntan, minne men även direkta smärtsignaler från perifera nerver. Kräkcentrum samordnar de muskler och nervimpulser som ingår vid en kräkning. Detta är muskler i mag-tarmkanalen, ansikte, hals, svalg och diafragma samt sympatiska och parasympatiska signaler via nervus vagus och nervus fascialis som bland annat styr salivering och tårsekretion (Blackburn & Spencer, 2015). Kemotriggerzonen är en del som ligger utanför blodhjärnbarriären och därför är extra känslig för läkemedel och substanser som finns i blodet. I kemotriggerzonen finns många receptorer för serotonin (5-HT), dopamin och opioider. Stimuleras dessa uppstår illamående och kräkning. Genom att farmakologiskt påverka receptorer eller singalsubstanser som verkar i kemotriggerzonen eller kräkcentrum så kan man minska förekomsten av PONV (Pleuvry, 2015), se figur 1. Farmakologisk behandling av PONV har dock risker, främst i form av extrapyramidala biverkningar men även arytmier. Därför är det viktigt med bra screening för att upptäcka de patienter som finns i riskzonen, annars riskerar patienterna att utsätts för onödiga risker i form av överbehandling (Blackburn & Spencer, 2015; Pleuvry, 2015; Nelson, 2002). Det finns även icke-farmakologisk behandling av PONV. Att trycka på P6-punkten som ligger belägen mellan flexor carpi radialis och palmaris longus ca 5 cm från handleden har en viss effekt på förekomsten av postoperativt illamående (Stott, 2016). Pre-operativ ångest har även visat sig ge en liten ökning av risken för PONV (Blackburn & Spencer, 2015; Nelson, 2002). Orsaken till detta tros bero på att ångest leder till
7
ökad mängd katekolaminer och även att personer med ångest tenderar att svälja mer luft vilket ökar risken för PONV (Nelson, 2002). Lukt påverkar även vår känsla av illamående men vissa dofter som till exempel pepparmint, lavendel och ingefära men även lukten av isopropylalkohol (återfinns vanligen i handdesinfektionsmedel) har visat sig kunna ge en viss minskning av PONV (Collins, 2011).
Fig 1. Uppkomstmekanismer vid PONV och receptorer av betydelse för dess
profylax/behandling (Oddby Muhrbeck, 2002)
PONV och dagkirurgi
Berg (2010) uppskattar att ungefär hälften av all kirurgi i Sverige idag är dagkirurgisk, vilket innebär att patienten aldrig blir inskriven på en vårdavdelning utan åker hem samma dag som operationen utförs. Enligt Mitchell (2015) har andelen dagkirurgi ökat och förväntas fortsätta öka som följd av den utveckling som sker kring laparoskopisk kirurgi och anestesimetoder. Idag är det på vissa sjukhus möjligt att göra längre och större planerade operationer som
cholecystektomi och höftledsplastik i dagkirurgi (Berger et al., 2009; Mitchell, 2015). En av fördelarna med dagkirurgi är en hög andel nöjda patienter och bättre utnyttjande av sjukvårdens resurser, men det ställer även högre krav på den perioperativa vården och patienten och dess närstående (Berger et al., 2009). Enligt Çaparlar et al. (2017) och Berger et al. (2009)
8
vid dagkirurgiska operationer. Således blir behandling och förebyggande av PONV centralt för både patientens hälsa samt för att på ett optimalt sätt utnyttja sjukvårdens resurser.
Rational
Trots att mycket forskning gjorts på förekomsten av PONV och försök att minimera riskerna för PONV är det fortfarande en av de vanligaste komplikationerna efter en operation (Golembiewski & O’Brien, 2002). Varför PONV uppstår och varför vissa drabbas värre än andra är komplicerat och trots välutvecklade mätinstrument är det ändå svårt att förutse vem som kommer att uppleva illamående och/eller kräkningar (Valeberg, 2013, s. 117). För patienten är PONV en mycket obehaglig och oönskad komplikation och är ett större obehag än smärta (Blackburn och Spencer, 2015). Utöver patientens lidande leder det till ökade kostnader samt förlänger vårdtiden för patienterna vilket i sin tur kan ha negativa effekter för andra patienter som på grund av
påföljande vårdplatsbrist kan bli tvungna att få sina operationer uppskjutna (Parra-Sanchez et al, 2012). Flera förebyggande åtgärder för att minska PONV finns i form av anpassade anestesier, riskbedömning och antiemetikaprofylax (Kranke & Eberhardt, 2011). Genom att anpassa läkemedelsbehandling och anestesimetod utifrån en pre-operativ riskskattning med avseende på PONV kan incidensen av PONV minskas (Pierre, Corno, Benais & Apfel, 2004). På de flesta sjukhus finns rutiner för att förhindra PONV. Vi har valt att undersöka hur dessa rutiner och riktlinjer används i praktiken, främst i form av riskskattning och profylaxbehandling. Detta har betydelse då en god följsamhet till rutiner är en viktig del i att minska morbiditet och mortalitet bland patienterna (de Vries et al., 2010).
Syfte
Syftet med studien var att undersöka hur riktlinjerna för att riskbedöma och förebygga PONV följs vid en dagkirurgisk avdelning. Frågeställningar:
● Hur stor andel drabbas av PONV?
● Hur stor andel har administrerats profylaxbehandling enligt rutinen? ● Hur stor andel har ordinerats profylaxbehandling enligt rutinen?
9
Metodbeskrivning
DesignStudien genomfördes som en prospektiv observationsstudie med en deskriptiv kvantitativ ansats. Detta valdes då deltagarna inte utsattes för någon intervention utan enbart mätning av ett
fenomen. Då syftet med studien var att undersöka förekomsten av PONV och följsamheten kring profylaxrutinen som finns är det gynnsamt att använda en kvantitativ ansats (jfr. Polit & Beck, 2016, s. 206). För att kunna se en förändring över tid och kunna mäta illamåendet upprepade gånger hos samma deltagare valdes ett prospektivt tillvägagångssätt. Enligt Billhult och Gunnarsson (2012, s. 117-120) anses prospektiva studier generellt visa på ett mer tillförlitligt resultat än retroprospektiva studier då det alltid finns en viss osäkerhet kring hur och var data insamlats.
Deltagare
Studiens urval omfattade patienter som skulle genomgå elektiv kirurgi på en dagkirurgisk avdelning vid ett medelstort regionsjukhus i norra Sverige. De deltagare som valdes ut uppfyllde studiens inklusionskriterier: aktuell för narkos med eller utan samtidig blockad (regional eller central), kvinnor och män ≥18 år. Exklusionskriterier var de patienter som inte var förmögna att svara på frågor. Åldern på deltagarna varierade mellan 19-88 år och fördelningen mellan könen var 53% kvinnor och 45% män. Initialt inkluderades 50 personer men en person exkluderades då man frångick den planerade anestesin och personen erhöll endast regional anestesi.
Genomförande
Då denna magisteruppsats är en del av en större studie som genomförs vid det aktuella sjukhuset var verksamhetschefer och personal redan informerade och delaktiga i studiens tillvägagångssätt. Därmed fanns det redan ett samtycke från dem att genomföra studien i deras verksamhet samt att personal var informerad om studiens syfte och vad det innebar för dem. Innan denna studie påbörjades skickades ett informationsbrev (bilaga 1) hem till patienterna i samband med kallelsen för operation. Ett formulär för skriftligt samtycke gavs till deltagarna samma dag de
10
opererades. Författarna valde att själv genomföra datainsamlingen vilket enligt Polit och Beck (2016, s. 196) är ett sätt att säkerställa att studien genomförts på rätt sätt.
Datainsamling
Datainsamlingen skedde i flera steg. Insamlandet började på själva operationsdagen då patienten fick svara på frågor preoperativt och postoperativt. De postoperativa frågorna ställdes 2 timmar samt 4 timmar efter operationsslut. Vid varje observationspunkt gällde frågan hur det varit sedan föregående observationspunkt. PONV utvärderades med hjälp av ett formulär med
standardiserade frågor (bilaga 2) som ställdes muntligt av författarna. Frågorna skrevs med hjälp av validerade instrument för att utvärdera PONV (Myles & Wengritzky, 2012). Alla formulär fick en specifik kod som kunde länkas till en specifik kodnyckel för att man skulle kunna gå tillbaka och spåra uppgifter. Övrig data som behövdes till studien hämtades in från deltagarnas anestesijournal för att få fram information om premedicinering, preoperativt ordinerade
antiemetikaprofylax, perioperativt givna antiemetikaprofylax, anestesimetod samt operationstid. Samtliga deltagare i studien erhöll generell anestesi. Med inhalationsanestesi menas i detta fall inhalationsgas (Sevorane) och anestesimetoden TIVA innebär total intravenös anestesi.
Dataanalys
Den insamlade data analyserades med hjälp av Statistical Package for Social Science (SPSS, Version 22.0.0.0). Deskriptiv statistik användes för att sammanfatta och beskriva den data som samlats in (jfr. Billhult & Gunnarsson, 2012, s. 306-309; Polit & Beck, 2016, s. 356). Resultatet presenterades därefter i löpande text samt i tabellform.
Etiska överväganden
Alla deltagare i studien fick i förväg information om syftet med studien samt hur den skulle gå tillväga. De blev informerade om att deltagandet i studien var frivilligt samt att de kunde avbryta sitt deltagande när som helst under studiens gång utan att behöva ange en orsak. Dem blev även informerade om att oavsett deltagande i studien eller inte skulle detta inte påverka den vård och omvårdnad de fick. Informerat samtycke är ett sätt att skydda deltagarnas autonomi och på så sätt
11
säkerställer man att de självmant väljer att delta (Kjellström, 2012, s. 82). För att en deltagare ska kunna avgöra om denne vill delta i studien måste dem ha fått all information som kan tänkas påverka beslutet om sitt deltagande. De ska ha förstått vad ett deltagande innebär och eventuella konsekvenser (Kjellström, 2012, s. 72; Olsson & Sörensen, 2011, s. 84-85).
Deltagarna informerades om att personuppgifter och data avidentifierades för att kunna garantera konfidentialitet och anonymitet för dem. Data som samlades in sparades i ett låst arkivskåp och var oåtkomlig för obehöriga. När studien avslutats och publicerats kommer all data att
makuleras. Då studien är en del av en större studie som pågår fanns det redan en godkänd etikansökan, vilket innebär att etiskt godkännande redan fanns för att genomföra studien enligt syfte och metod i denna studie.
Etiska principer inom forskning finns till för att se till att människors rättigheter och värde upprätthålls för att undvika att de som deltar blir skadade eller felaktigt utnyttjade. Principen att forskningen ska göra gott innebär att det är forskarens ansvar och skyldighet att inte orsaka skada samt att väga vinsterna med forskningen mot riskerna. En annan viktig etisk princip är forskarens respekt för autonomi, att alla har rätt att själv bestämma över sitt eget liv (Kjellström, 2012, s. 70-73). Eftersom detta är en observationsstudie gjordes bedömningen att deltagarna inte utsattes för någon risk att skadas av studien. Studiens resultat kommer även kunna vara till nytta för framtida patienter då det kommer bidra med en ökad kunskap om följsamheten till rutiner vilket är en viktig del i patientsäkerhetsarbetet.
12
Resultat
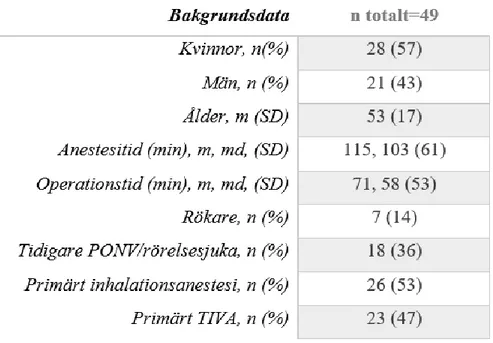
49 personer deltog i studien, 28 (57%) var kvinnor och 21 (43%) var män. Medelåldern på deltagarna var 53 år, se tabell 1.
Tabell 1. Bakgrundsdata
Fördelningen av patienternas modifierade Apfel-score visas i tabell 2. Poäng bestämdes efter de kriterier som omfattas av den modifierade Apfel-score som användes på det sjukhus där
undersökningen genomfördes, se bilaga 3.
13
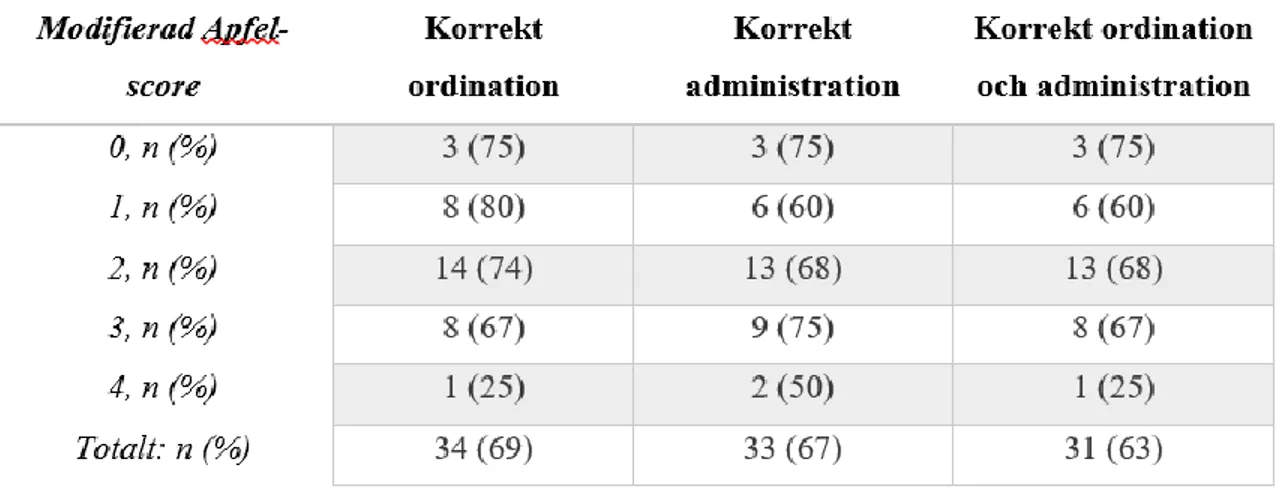
Följsamhet till PONV-rutin presenteras utifrån om korrekt ordination och/eller korrekt administration har följts. Med korrekt ordination menas i detta fall att rutinen har följts och patienten fick rätt profylax ordinerat utifrån dennes M-Apfel score och med korrekt
administration menas att rutinen har följts och patienten har fått rätt profylax administrerat utifrån M-Apfel score, även i de fall där det saknats eller funnits en felaktig ordination i den pre-operativa bedömningen. Av de 49 deltagarna fick31 (63%)korrekt ordinerad och administrerad PONV-profylax utifrån sin modifierade Apfel-score (M-Apfel) (tabell 3). Av de 16 personer som hade M-Apfel 3 och 4 sövdes 7 (44%) med inhalationsanestesi. Högst andel avvikelser från rutinen begicks i gruppen M-Apfel 4, där rutinen endast följdes i 25% av fallen. 50% sövdes med inhalationsanestesi.
Tabell 3. Följsamhet enligt PONV-rutin
3 av de 5 personer som hade M-Apfel-score 0-1 och som hade fått PONV-profylax trots att det inte var indicerat utifrån deras riskbedömning fick Betapred (betametason). Av de 35 personer i M-Apfel score 2-4 grupperna så var endast 19 Betapred men 25 fick läkemedlet. Av de totalt 49 deltagarna så fick 28 Betapred (17 som monoterapi och 11 i kombination med något annat preparat). 7 av de 49 personerna fick Dridol (droperidol) och 10 av 49 fick Postafen (meklozin).
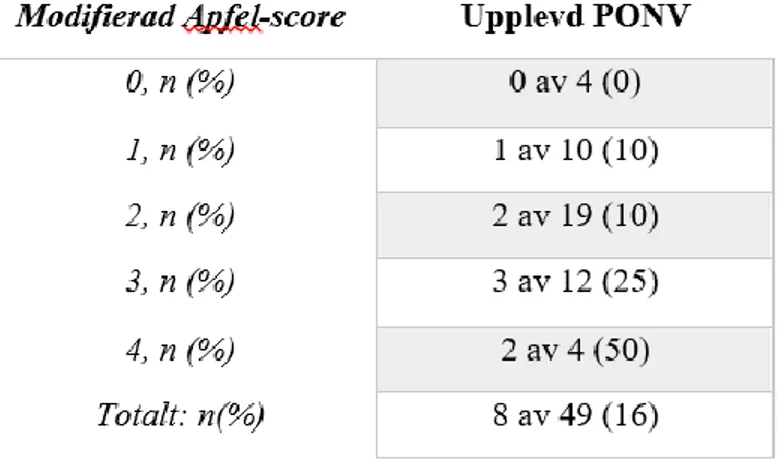
Av studiens 49 deltagare drabbades 8 av PONV (tabell 4), varav samtliga var kvinnor.
Medelåldern bland dessa personer var 45 år. 7 av 8 hade fått korrekt ordinerad PONV-profylax och 6 av 8 hade fått korrekt administrerad PONV-profylax. I förhållande till respektive grupps
14
storlek (grupperade efter M-Apfel-score) upplevde flest personer PONV i M-Apfel score 4 (50%) och M-Apfel score 3 (25%). 1 av de 2 personer med M-Apfel score 3 som inte fått korrekt administrerad PONV-profylax hade fått mer läkemedel än vad rutinen säger att hon bör få utifrån sin M-Apfel-score. Hos 2 av de 8 deltagarna fanns det enligt rutinen utrymme att ge mer
läkemedel utifrån deras M-Apfel-score. 2 av de 8 deltagarna sövdes med inhalationsanestesi, dessa två personer hade båda M-Apfel score >2.
Tabell 4. Antal drabbade av PONV
Diskussion
ResultatdiskussionSyftet med studien var att undersöka hur riktlinjerna för att riskbedöma och förebygga PONV följs vid en dagkirurgisk avdelning. Vi fann att ca 16% av patienterna upplevde PONV vilket är liknande resultat som Pierre, Corno, Benais och Apfel (2004) kom fram till då riskskattning av PONV och anpassning av medicinering och anestesimetod gjordes. Samtliga som drabbades av PONV var kvinnor, vilka löper nästan tre gånger större risk för PONV jämfört med män
(Murphy et al., 2006). Författarna till denna studie anser att det ändå är anmärkningsvärt att inga av männen i denna studie drabbades av PONV.
Resultatet i denna studie visade att följsamheten till rutinen var 63%. I vissa fall fick patienterna mer PONV-profylax än vad som var rekommenderat utifrån M-Apfel score och blev alltså
15
överbehandlade vilket kan medföra en risk för oönskade biverkningar från en behandling som sannolikt inte gagnar patienten. Enligt flera studier kring följsamhet till riktlinjer/rutiner inom sjukvården är följsamheten mellan 58% och 82%, där de högsta värdena framkom vid
självskattning (Freeland et al., 2015; Helder et al., 2010; Ng, Chung, Toderika, & Cheng-Lai, 2016; Nilsson et al., 2014; Nilsson, Brulin, C., Grankvist & Juthberg, 2017; Webster et al., 2015). Att rutinen för att förebygga PONV frångås i nästan 37% av alla de dagkirurgiska anestesier kan ses som att personalen inte följer de evidensbaserade riktlinjerna som är uppsatta av verksamheten. Detta resultat samstämmer väl med Webster et al. (2015) som visar att
följsamheten till rutiner generellt bland anestesisjuksköterskor ligger på 66%. Att avsteg från rutin görs skulle kunna förklaras av den s.k. Efficiency-Thoroughness Trade-Off-principen (ETTO-principen) som innebär att ett visst avkall på säkerheten görs av personal, för att öka effektiviteten i arbetet, men att dessa avsteg endast görs i den mån att personen fortfarande bedömer sitt handlande som säkert (Ödegård, 2013, s. 289). Även Johansson och Wallin (2013, s. 109) menar att erfarna sjuksköterskor oftare grundar sina beslut på erfarenhet jämfört med sjuksköterskor med mindre yrkeserfarenhet som i större utsträckning grundar sina beslut på regler och riktlinjer.
Följsamhet och patientsäkerhet
Även om denna studies resultat visar att följsamheten till rutiner var relativt god och att 63% av de dagkirurgiska patienterna fick sina PONV-förebyggande åtgärder korrekt ordinerade och administrerade utifrån de rutiner som fanns, är det dock viktigt enligt författarna till denna studie att reflektera över de 37% där avsteg gjordes från rutinen. I Hälso- och sjukvårdslagen (HSL, SFS 1982:763) framgår det tydligt att sjukvården ska upprätthålla en trygg och säker vård för patienten. En säker vård är en vård som baseras på evidensbaserad kunskap och det är därför viktigt att rutiner finns och efterföljs för att kunna upprätthålla patientsäkerheten. Sjukhuset i studien använder sig av en modifierad Apfel-score som väljer att lägga vikt vid ålder istället för postoperativt opioidbehov. Medelåldern för de som upplevde PONV i denna studie var 45 år, det vill säga ovanför den brytpunkt som finns i rutinen. Enligt Murphy et al. (2006) är låg ålder en beroende faktor som är associerad med PONV men den fungerar inte som en faktor för att förutse vem som kommer drabbas. Murphy et al. (2006) menar att postoperativt opioidbehov är en oberoende riskfaktor som bättre kan förutse PONV än ålder. Det finns även andra faktorer, till
16
exempel ångest, som är associerade med PONV men som inte är bra på att förutse vem som kommer drabbas Nackdelen med att bedöma post-operativt opioidbehov är att det ibland kan vara svårt att förutse på grund av individuella skillnader i smärtkänslighet och därför blir åldern en enklare variabel att mäta. Utifrån detta anser författarna till denna studie att en ändring av rutinen bör övervägas så att hänsyn istället tas till de riskfaktorer som finns i den ursprungliga förenklade Apfel-score.
I resultatet framkom att högst andel avvikelser från rutinen förekom i gruppen M-Apfel 4, där följsamheten endast låg på 25 %. Då syftet har varit att undersöka följsamhet till rutiner, kan inga slutsatser dras om dessa patienter fått felaktig/ingen eller annan behandling. Däremot är det viktigt att reflektera över att kvalitet och säkerhet har en tydlig anknytning till varandra och brister det ena faller även det andra. I Socialstyrelsens föreskrift och allmänna råd om ledningssystem för systematiskt kvalitetsarbete (SOSFS 2011:9) står det att ett bra och omfattande ledningssystem för kvalitet och säkerhet är ett villkor för upprätthållande av en verksamhets patientsäkerhet. Ett sådant ledningssystem innehåller de rutiner och styrande dokument som personalen ska kunna använda som stöd i verksamheten för att kunna ta välgrundade beslut. Dessa rutiner måste dock vara utformade på ett tydligt sätt och vara väl implementerad bland all personal. Författarna till denna studie har inte information om all
personal var medveten om rådande rutiner. Kohn, Corriga och Donaldson (2000, s. 86-87) menar dock att alla händelser som avviker från de normala rutinerna bör rapporteras. Att rapportera avvikelser är allas ansvar och skyldighet. Avvikelsehantering är ett av de viktigaste redskap verksamheten har för att kunna se och förstå de risker som kan uppstå och hjälper till att se samband med processer och rutiner som inte fungerar på ett säkert sätt.
I resultatet framkom att vissa patienter hade fått mer läkemedel än dem skulle ha om rutinen följts, samt att vissa patienter fått mindre läkemedel än rutinen föreskrev. Enligt Ivensky (2017) syftar rutiner till att minska risker för patienten och genom att frångå dem äventyras
patientsäkerheten i viss mån. Regelbundna avsteg från rutiner och riktlinjer innebär ett beteende som ökar risken för att olyckor ska hända varför det är viktigt att upptäcka sådant beteende. För att förändra och förbättra ett sådant beteende är det viktigt med ett system som fokuserar både på ledning, rutiner och individens ansvar och inte skuldbelägger individer utan fokuserar på att lära
17
av misstag. Författarna till denna studie menar således att det är viktigt att ledningen uppmärksammar detta och arbetar för att nå en bättre följsamhet.
Profylaxbehandling
Resultatet i vår studie visar att Betapred var det mest använda PONV-profylaxläkemedlet. Betapred var även det läkemedel som administrerades till flest personer som inte hade det
ordinerat i sin premedicinering. Det var även det läkemedlet som flest gånger hade administrerats till personer som inte skulle ha någon profylax. Detta kan vara ett tecken på att läkemedlet
administreras vanemässigt vid narkosinduktion. Det kan i sin tur medföra en risk att patienten drabbas av biverkningar. Förutom biverkningar som psykiska störningar, ångest och försämrad sårläkning så kan Betapred även interagera med andra läkemedel som antikoagulantia, NSAID-preparat och efedrin (www.fass.se). Denna studie visar även att Betapred administreras i samband med anestesiinduktion. Enligt rutinen är Betapred en del av den PONV-förebyggande pre-medicineringen och skall därför ges innan anestesin börjar. I en studie av Olanders,
Lundgren och Johansson (2014), kunde man se att de patienter som fått Betapred precis i
samband med induktion hade en liten effekt på PONV. De kunde även dra slutsatsen att Betapred har en långsam antiemetisk effekt och läkemedlet därför bör administreras i ett tidigare skede för att få en bättre postoperativ effekt. Denna slutsats stöds även av Aasboe, Raeder och Groegaard (1998) som i sin studie kom fram till att effekten av Betapred inte visades förrän efter 3-4 timmar postoperativt då det gavs i samband med induktion. Med tanke på att mediantiden för en anestesi i vår studie var 1h 43 min minuter betyder det att Betapred borde ha administrerats mycket tidigare för att ha optimal effekt. Att Betapred administrerats trots att det inte var ordinerat som pre-medicinering behöver inte betyda att det gavs utan ordination då det finns en ansvarig narkosläkare vid varje modul som kan ge muntliga ordinationer till narkossjuksköterskan.
Metoddiskussion
En styrka med studien är att vi själva var på plats och genomförde datainsamlingen vilket ledde till att vi kunde undvika ett lågt svarsdeltagande och att formulären inte fylldes i korrekt. Det ledde även till att vi inte fick något bortfall, vilket enligt Trost och Hultåker (2016, s. 147) betyder att vi ej behövde göra en bortfallsanalys.
18
För att uppnå en hög grad av validitet bör ens mätinstrument vara utformat för att mäta det som det avser att mäta (Gunnarsson & Billhult, 2012, s. 152; Polit & Beck, 2016, s. 310). En styrka med studien är att frågorna i formuläret som användes har använts i liknande studier tidigare (jfr. Myles & Wengritzky, 2012) vilket stärker dess validitet. Då frågorna är vedertagna och
beprövade innebär det också att studiens reliabilitet ökar. Att ens studie har hög reliabilitet innebär att man får samma mått vid varje mätning och att man kan överföra resultatet på en större population (Gunnarsson & Billhult, 2012, s. 153). Detta innebär att resultatet troligtvis är överförbart på andra sjukhus av liknande storlek.
En av nackdelarna med självskattningsfrågor med få svarsalternativ är att de kan leda till missförstånd av frågan och att man då inte får ut den information man velat få (Polit & Beck, 2016, s. 270). Detta påtalades av vissa patienter när de skulle uppskatta om de upplevde att de blev rörelsesjuka samt om de klassade sig själva som rökare eller inte.
Självskattning av tidigare PONV/rörelsesjuka
Det finns en viss osäkerhet vid självskattningen av rörelsesjuka/tidigare PONV bland studiens deltagare. Vissa hade haft problem med detta då de var yngre. Enligt Golding et al. (2017) har yngre personer större benägenhet att drabbas av rörelsesjuka och det går att till viss grad träna bort genom tillvänjning. Detta innebär att deltagarna i denna studie kan ha haft rörelsesjuka men vuxit ifrån den eller tränat bort den och har således inte kvar den nu. De flesta som hade
rörelsesjuka var medvetna om detta. I vår studie klassades personer som rörelsesjuka om de upplevde det som ett aktuellt problem, dvs. enstaka händelser som skedde för länge sen
bedömdes inte som aktuellt. Tidigare PONV räknades dock alltid med som en riskfaktor oavsett hur länge sedan operationen skedde.
Självskattning av rökare/icke-rökare
Det finns även en viss osäkerhet vid självskattningen av rökare/icke-rökare bland studiens deltagare. Vissa hade slutat röka inför operationen på inrådan av operatören, vissa andra hade rökt tidigare i livet och vissa personer rökte enstaka cigaretter i samband med fest. Enligt Pomerleau, Pomerleau, Snedecor och Mehringer (2004) kan rökare definieras utifrån om de har ett nikotinberoende klassat enligt DSM-IV sammanvägt med ungefärligt antal cigaretter de rökt
19
under en livstid. Även självdefinierade icke-rökare har i stor utsträckning någon gång använt med cigaretter men sällan rökt mer än 200 cigaretter under sin livstid eller hunnit utveckla ett nikotinberoende (Pomerleau, Pomerleau, Snedecor & Mehringer, 2004). Enligt Golding, Prosyanikova, Flynn och Gresty (2011) kan det vara abstinensen som ger den anti-emetiska effekten och således är det endast de personer som är rökare som har minskad PONV-risk. Om det är abstinensen som har den anti-emetiska effekten skulle snusning också kunna ha effekt på PONV vilket får stöd av Brattwall et al. (2010). I vår studie har definitionen av rökare varit de personer som röker tobak dagligen vilket är en korrekt bedömning utifrån PONV-synpunkt. 14% av deltagarna i studien klassade sig själva som rökare vilket stämmer överens med
Socialstyrelsens rapport om svenska folkets tobaksvanor (Socialstyrelsen, 2009). Dock har studien inte tagit hänsyn till övriga tobaksvanor som till exempel snus då det området behöver mer forskning.
Olika kirurgiska ingrepp
I vår studie har vi inte tagit hänsyn till vilka operationer som personerna genomgått. Detta skulle kunna vara en förklaring till varför vissa patienter fick mer profylaxbehandling än vad deras riskbedömning indikerade. Enligt Bakhta et al. (2016) är vissa kirurgiska ingrepp mer
associerade med PONV. Gynekologiska laparoskopier är en sådan grupp och då dessa patienter är dagkirurgiska patienter kan de förhöjda förekomsten av PONV leda till förlängda vårdtider. Enligt Aleksandar, Velimir, Sava och Duško (2012) har de patienter som genomgår
laparoskopiska, i synnerhet gynekologiska, uppemot 70% ökad risk för PONV.
Konklusion
I denna studie framkom att följsamheten till rutinen för att förebygga PONV var 63% vilket stämmer överens med tidigare studier kring följsamhet. Frekvensen av PONV var 16% vilket också stämmer överens med tidigare studier. Utifrån detta resultat finns utrymme att förbättra följsamheten men det är dock osäkert om detta kommer minska frekvensen av PONV. I resultatet framkommer att avsteg görs från rutinen. Det hade därför varit av värde att göra en studie som undersöker varför dessa avsteg görs. Att även undersöka andra rutiner kring
20
anestesisjuksköterskans arbetsuppgifter hade kunnat ge svar på om den följsamhet som uppmättes i denna studie är hög eller låg i förhållande till andra rutiner inom kliniken.
Vidare forskning inom detta område pågår ständigt och är välbehövligt då PONV fortfarande är ett stort postoperativt problem som skapar obehag för patienten och kan medföra risker. PONV har dock visat sig vara svårt att bli av med och att studera eventuella biverkningar från
antiemetika hade kunnat visa om det är ett problem för patienterna. Att undersöka om snusning påverkar PONV i samma utsträckning som rökning är också ett område som behöver undersökas närmare.
21
Referenser
Aleksandar, Ć., Velimir, C., Sava, R., & Duško, M. (2012). Patient position as a possible risk factor for postoperative nausea and vomiting (PONV) in gynecologic laparoscopy. Acta Medica
Medianae, 51(4), 32-38.
Apfel, C., Laara, E., Koivuranta, M., Greim, C., & Roewer, N. (1999). A simplified risk score for predicting postoperative nausea and vomiting - Conclusions from cross-validations between two centers. Anesthesiology, 91(3), 693-700.
Aasboe, V., Raeder, J. C., & Groegaard, B. (1998). Betamethasone reduces postoperative pain and nausea after ambulatory surgery. Anesthesia and Analgesia, 87(2), 319-323.
Berg, K. (2010). Postoperative recovery in day surgery: evaluation of psychometric properties
and clinical usefulness of a questionnaire in day surgery. Licentiatavhandling (sammanfattning)
Linköping: Linköpings universitet, 2010. Linköping.
Bhakta, P., Ghosh, B. R., Singh, U., Govind, P. S., Gupta, A., Kapoor, K. S., & ... Mukherjee, G. (2016). Incidence of postoperative nausea and vomiting following gynecological laparoscopy: A comparison of standard anesthetic technique and propofol infusion. Acta Anaesthesiologica
Taiwanica, 54, 108-113. doi:10.1016/j.aat.2016.10.002
Billhult, A., & Gunnarsson, R. (2012). Bortfallsanalys och beskrivande statistik. I M. Henricson (Red.). Vetenskaplig teori och metodik: Från idé till examination inom omvårdnad (s. 305-314). Lund: Studentlitteratur.
Billhult, A., & Gunnarsson, R. (2012). Kvantitativ studiedesign och stickprov. I M. Henricson (Red.), Vetenskaplig teori och metodik: Från idé till examination inom omvårdnad (s. 115-126). Lund: Studentlitteratur.
Blackburn, J., & Spencer, R. (2015). Postoperative nausea and vomiting. Anaesthesia and
22
Brattwall, M., Stomberg, M. W., Rawal, N., Segerdahl, M., Houltz, E., & Jakobsson, J. (2010). Postoperative impact of regular tobacco use, smoking or snuffing, a prospective multi-center study. Acta Anaesthesiologica Scandinavica, 54(3), 321-327.
doi:10.1111/j.1399-6576.2009.02140.x
Brenner, P., & Kautz, D. D. (2015). Postoperative care of patients undergoing same-day laparoscopic cholecystectomy 3.0. AORN Journal, 102(1), 15-32.
doi:10.1016/j.aorn.2015.04.021
Börjesson, S., Arweström, C., Baker, A., & Berter, C. (2010). Nurses’ experiences in the relief of postoperative nausea and vomiting. Journal of Clinical Nursing, 19(13/14), 1865-1872.
doi:10.1111/j.1365-2702.2009.03176.x
Çaparlar, C. Ö., Özhan, M. Ö., Süzer, M. A., Yazicioğlu, D., Eşkin, M. B., Şenkal, S., & ... Çekmen, N. (2017). Fast-track anesthesia in patients undergoing outpatient laparoscopic cholecystectomy: comparison of sevoflurane with total intravenous anesthesia. Journal of
Clinical Anesthesia, 37, 25-30. doi:10.1016/j.jclinane.2016.10.036
Collins, A. S. (2011). Postanesthesia Care. Postoperative nausea and vomiting in adults: Implications for critical care postanesthesia. Critical Care Nurse, 31(6), 36-45.
doi:10.4037/ccn2011470
Conway, B. (2009). Prevention and management of postoperative nausea and vomiting in adults.
AORN Journal, 90, 391,396,403-394,400,413. doi:10.1016/j.aorn.2009.06.026
Dienemann, J., Hudgens, A. N., Martin, D., Jones, H., Hunt, R., Blackwell, R., & ... Divine, G. (2012). Risk factors of patients with and without postoperative nausea (PON). Journal of
23
de Vries, E., Prins, H., Crolla, R., den Outer, A., van Andel, G., van Helden, S., & ...
Boermeester, M. (2010). Effect of a comprehensive surgical safety system on patient outcomes.
New England Journal of Medicine, 363(20), 1928-1937.
Freeland, K.N., Cogdill, B.R., Ross, C.A., Sullivan, C.O., Drayton, S.J., Vandenberg, T.A.M., & Garrison, K.L. (2015). Adherence to evidence-based treatment guidelines for bipolar depression in an inpatient setting. American Journal of Health-System Pharmacy, 72, 156-161.
doi:10.2146/sp150023
Golding, J. F., Paillard, A. C., Normand, H., Besnard, S., & Denise, P. (2017). Prevalence, Predictors, and Prevention of Motion Sickness in Zero-G Parabolic flights. Aerospace Medicine
& Human Performance, 88(1), 3-9.
Golding, J. F., Prosyanikova, O., Flynn, M., & Gresty, M. A. (2011). The effect of smoking nicotine tobacco versus smoking deprivation on motion sickness. Autonomic Neuroscience:
Basic and Clinical, 160, 53-58. doi:10.1016/j.autneu.2010.09.009
Golembiewski, J. A., & O'Brien, D. (2002). A systematic approach to the management of postoperative nausea and vomiting. Journal of Perianesthesia Nursing, 17, 364-376. doi:10.1053/jpan.2002.36596
Gunnarsson, R., & Billhult, A. (2012). Mätinstrument och diagnostiska test. I M. Henricson (Red.). Vetenskaplig teori och metodik: Från idé till examination inom omvårdnad (s. 151-160). Lund: Studentlitteratur.
Hafez, M. S., Abdelhamid, M. D., Youssef, M. I., & Abdelrahim, I. H. (2017). Randomized controlled trial of two oral regimens of gabapentin versus placebo in patients for Cesarean section under spinal anesthesia regarding postoperative pain, sedation, nausea and vomiting.
24
Helder, O. K., Brug, J., Looman, C. W., van Goudoever, J. B., & Kornelisse, R. F. (2010). The impact of an education program on hand hygiene compliance and nosocomial infection incidence in an urban Neonatal Intensive Care Unit: An intervention study with before and after
comparison. International Journal of Nursing Studies, 47, 1245-1252. doi:10.1016/j.ijnurstu.2010.03.005
Ivensky, V. (2017). Optimizing Safety. Professional Safety, 62(1), 36-45.
Johansson, E., & Wallin, L. (2013). Evidensbaserad vård. I A. Edberg. (red.). Omvårdnad på
avancerad nivå: kärnkompetenser inom sjuksköterskans specialistområden. (s. 103-145) (1.
uppl.) Lund: Studentlitteratur.
Kjellström, S. (2012). Forskningsetik. I M. Henricson (Red.). Vetenskaplig teori och metodik:
Från idé till examination inom omvårdnad (s. 69-92). Lund: Studentlitteratur.
Kohn, L.T., Corrigan, J., & Donaldson, M.S. (red.) (2000). To err is human [Elektronisk resurs]
building a safer health system. Washington, D.C.: National Academy Press.
Kranke, P., & Eberhart, L. (2011). Possibilities and limitations in the pharmacological management of postoperative nausea and vomiting. European Journal of Anaesthesiology,
28(11), 758-765. doi:10.1097/EJA.0b013e32834a4e1
Lipp, A., & Kaliappan, A. (2007). Focus on quality: Managing pain and PONV in day surgery.
Current Anaesthesia & Critical Care, 18, 200-207. doi:10.1016/j.cacc.2007.07.013
Mayeur, C., Robin, E., Kipnis, E., Vallet, B., Andrieu, G., Fleyfel, M., & ... Lebuffe, G. (2012). Impact of a prophylactic strategy on the incidence of nausea and vomiting after general surgery.
Annales Francaises D'anesthesie et de Reanimation, 31, 53-57.
doi:10.1016/j.annfar.2011.10.016
25
Mitchell, M. (2015). Home recovery following day surgery: a patient perspective. Journal of
Clinical Nursing, 24(3/4), 415-427. doi:10.1111/jocn.12615
Myles, P., & Wengritzky, R. (2012). Simplified postoperative nausea and vomiting impact scale for audit and post-discharge review. British Journal of Anaesthesia, 108(3), 423-429.
doi.org/10.1093/bja/aer505
Murphy, M. J., Hooper, V. D., Sullivan, E., Clifford, T., & Apfel, C. C. (2006). Identification of risk factors for postoperative nausea and vomiting in the perianesthesia adult patient. Journal of
Perianesthesia Nursing, 21, 377-384. doi:10.1016/j.jopan.2006.09.002
Nelson, T. P. (2002). Continuing Education: Postoperative nausea and vomiting: Understanding the enigma. Journal of Perianesthesia Nursing, 17, 178-189. doi:10.1053/jpan.2002.33207
Nilsson, K., Brulin, C., Grankvist, K., & Juthberg, C. (2017). Factors associated with nursing students' adherence to venous blood collection practice guidelines – A cross sectional study.
Nurse Education in Practice, 23, 92-98. doi:10.1016/j.nepr.2017.02.002
Nilsson, K., Grankvist, K., Juthberg, C., Brulin, C., & Söderberg, J. (2014). Deviations from venous blood specimen collection guideline adherence among senior nursing students. Nurse
Education Today, 34, 237-242. doi:10.1016/j.nedt.2013.06.018
Ng, C., Chung, P., Toderika, Y., & Cheng-Lai, A. (2016). Evaluation of adherence to current guidelines for treatment of hyperlipidemia in adults in an outpatient setting. American Journal of
Health-System Pharmacy, 73, 133-140. doi:10.2146/ajhp160050
Oddby Muhrbeck, E. (2002). Postoperative nausea and vomiting in women: an unglamorous
aspect of anaesthesia. (Doktorsavhandling, Karolinska institutet, Stockholm). Hämtad från
26
Odom-Forren, J. (2011). Measurement of postdischarge nausea and vomiting for ambulatory surgery patients: A critical review and analysis. Journal of Perianesthesia Nursing, 26, 372-383. doi:10.1016/j.jopan.2011.09.008
Olanders, K. J., Lundgren, G. A., & Johansson, A. M. (2014). Betamethasone in prevention of postoperative nausea and vomiting following breast surgery. Journal of Clinical Anesthesia, 26, 461-465. doi:10.1016/j.jclinane.2014.02.006
Olsson, H., & Sörensen, S. (2011). Forskningsprocessen. Stockholm: Liber.
Parra-Sanchez, I., Abdallah, R., You, J., Fu, A., Grady, M., Cummings, K., Apfel, C., Sessler, D. (2012). A time-motion economic analysis of postoperative nausea and vomiting in ambulatory surgery. Canadian Journal of Anesthesia-Journal Canadien D Anesthesie, 59(4), 366-375. doi:10.1007/s12630-011-9660-x
Pierre, S., Corno, G., Benais, H., & Apfel, C. (2004). A risk score-dependent antiemetic approach effectively reduces postoperative nausea and vomiting - a continuous quality improvement initiative. Canadian Journal of Anaesthesia-Journal Canadien D Anesthesie,
51(4), 320-325.
Pleuvry, B. J. (2015). Physiology and pharmacology of nausea and vomiting. Anaesthesia &
Intensive Care Medicine, 16, 462-466. doi:10.1016/j.mpaic.2015.06.018
Polit, D. F. & Beck, C. T. (2016). Nursing Research. Generating and Assessing Evidence for
Nursing Practice. (10th eds.). Philadelphia: Wolters Kluwer
Pomerleau, C., Pomerleau, O., Snedecor, S., & Mehringer, A. (2004). Defining a never-smoker: Results from the nonsmokers survey. Addictive Behaviors, 29(6), 1149-1154.
SOSFS 2011:9. Föreskrifter och allmänna råd om ledningssystem för systematiskt
27
SFS 1982:763. Hälso- och sjukvårdslagen. Stockholm: Socialdepartementet
Smith, C. A., & Ruth-Sahd, L. (2016). Reducing the incidence of postoperative nausea and vomiting begins with risk screening: An evaluation of the evidence. Journal of Perianesthesia
Nursing, 31, 158-171. doi:10.1016/j.jopan.2015.03.011
Socialstyrelsen (2009). Folkhälsorapport 2009. Stockholm: Socialstyrelsen.
Socialstyrelsen. (2015). Statistikdatabas för operationer i sluten vård. Hämtad 2017-02-07 från http:// www.socialstyrelsen.se/statistik/statistikdatabas/operationerislutenvard
Stewart, M. W. (2013). Research News: Postdischarge nausea and vomiting. Journal of
Perianesthesia Nursing, 28, 40-42. doi:10.1016/j.jopan.2012.11.003
Stott, A. (2016). Examining the efficacy of stimulating the PC6 wrist acupuncture point for preventing postoperative nausea and vomiting: A Cochrane review summary. International
Journal of Nursing Studies, 64, 139-141. doi:10.1016/j.ijnurstu.2016.07.004
Thomas, R., Jones, N. A., & Strike, P. (2002). The value of risk scores for predicting postoperative nausea and vomiting when used to compare patient groups in a randomised controlled trial. Anaesthesia, 57(11), 1119-1128. doi:10.1046/j.1365-2044.2002.02782_4.x
Trost, J. & Hultåker, O. (2016). Enkätboken. (5., [moderniserade och rev.] uppl.) Lund: Studentlitteratur.
Valeberg. B.T. (2013). Illamående och kräkningar postoperativt. I I. L. Hovind (red.).
28
Webster, C. S., Andersson, E., Edwards, K., Merry, A. F., Torrie, J., & Weller, J. M. (2015). Deviation from accepted drug administration guidelines during anaesthesia in twenty highly realistic simulated cases. Anaesthesia and Intensive Care, 43(6), 698-706.
Wu, Y., Sun, H., Wang, S. & Tseng, C. (2015). Applicability of risk scores for postoperative nausea and vomiting in a Taiwanese population undergoing general anaesthesia. Anaesthesia and
Intensive Care, 43(4), 473-478.
Ödegård, S. (2013) Patientsäkerhet. I J. Leksell & M. Lepp (red.). Sjuksköterskans
29
Bilaga 1 - Informationsbrev till patienten samt blankett för samtycke
Tillfrågan om deltagande i forskningsprojekt
”Illamående och kräkning efter operation”
Bakgrund och SyfteIllamående och kräkning efter operation är något som besvärar många efter operation/narkos och brukar beskrivas som ”det lilla stora problemet”. Många patienter upplever illamående och kräkning som minst lika besvärligt som smärtan efter operation. Det är många faktorer om bidrar till problemet där bl. a. både faktorer hos patienten och de läkemedel som ges för narkos spelar in.
Det finns idag vetenskapligt underlag för att vi utifrån en riskvärdering hos den enskilda patienten ska ge förebyggande behandling mot illamående och kräkning. Patienter med låg risk bör inte få någon förebyggande behandling och patienter med hög risk bör få flera förebyggande läkemedel.
Vi vill nu i en vetenskaplig undersökning ta reda på hur dessa vetenskapligt baserade riktlinjer för att förebygga illamående och kräkning efter operation/narkos fungerar i praktiken. Hur stor andel patienter mår illa efter
operation? Ger vi rätt förebyggande behandling? Kan vi göra det bättre för patienterna? Är illamående och kräkning fortfarande ett problem?
Förfrågan om deltagande
Vi tillfrågar Dig om deltagande i en undersökning där vi observerar hur patienter mår efter operation och då särskilt med avseende på illamående och kräkning.
Hur går studien till?
Efter din operation/narkos kommer du de närmaste timmarna att regelbundet få skatta ditt illamående och förekomst av kräkningar som kan vara relaterade till operation/narkos. När du är på sjukhuset kommer sjukvårdspersonal att ställa frågor till dig.
Vi registrerar all behandling av illamående du får när du är på sjukhuset. För det aktuella behandlingstillfället kommer vi att hämta in uppgifter från de olika journalsystemen för att registrera betydande bakgrundsfaktorer, operations- och narkosförlopp samt omhändertagandet efter operation.
Vilka är riskerna?
Ditt deltagande i studien kommer inte att påverka din vård vid detta tillfälle. Att delta är helt frivilligt och du kan avbryta ditt deltagande när som helst. Att bli tillfrågad om deltagande kan få vissa att känna sig tvingade att delta. Vi vill därför understryka att du gör detta helt frivilligt.
Finns det några fördelar?
Den fördel du kan få av studien är en ökad uppmärksamhet av hur du mår efter operationen. Hantering av data och sekretess
Dina svar och de uppgifter vi registrerar kommer att behandlas så att inte obehöriga kan ta del av dem. Alla insamlade uppgifter kommer att kodas helt och förses med en för dig unik kod i studien. Insamlade uppgifter i forskningsprojektet kommer att behandlas i ett dataregister och uppgifterna om dig identifieras med din unika kod – inte med ditt namn eller personnummer. Endast projektansvarig (se nedan) har tillgång till kodnyckeln med vilken det går att koppla uppgifterna till dig.
30
När studien är slutförd och sammanställd kommer rapporten att publicerasi Digitala Vetenskapliga Arkivet, DiVA. Frivillighet
Om Du deltar har Du rätt att när som helst utträda ur studien utan motivering och utan att det påverkar Ditt fortsatta omhändertagande.
För ytterligare information eller om problem uppstår kan studieansvarig kontaktas. Ansvariga för studien är:
Julia Halatchev, Leg. Sjuksköterska, Anestesisjuksköterskestudent
Luleå Tekniska Universitet julhal-5@student.ltu.se
Viktor Triumf, Leg. Sjuksköterska Anestesisjuksköterskestudent Luleå Tekniska Universitet viktri-7@student.ltu.se
Handledare:
Ulrica Strömbäck, Doktorand Luleå Tekniska Universitet Ulrica.stromback@ltu.se
Handledare:
Åsa Engström, Professor Luleå Tekniska Universitet Asa.engstrom@ltu.se
31 SAMTYCKE
Samtycke till deltagande i studien ”Illamående och kräkning efter operation – är det fortfarande ett problem?” och till behandling av personuppgifter:
Jag har muntligen och skriftligen informerats om den aktuella studien och haft tillfälle att i lugn och ro läsa igenom informationen och att ställa frågor. Jag får också en kopia på den skriftiga informationen och mitt samtycke. Genom min underskrift samtycker jag till:
- att medverka i studien
- att mina personuppgifter behandlas såsom beskrivits -
Jag är medveten om att deltagandet är frivilligt, samt att jag när som helst och utan att ange orsak kan avbryta mitt deltagande utan att det påverkar mitt framtida omhändertagande.
Kvalitetskontroll av data
Jag har också informerats om och samtycker härmed till att oberoende granskare, nationella kontrollmyndigheter och etiska kommittéer vid behov och upp till 15 år efter studieavslut får jämföra de i studien rapporterade uppgifterna med de uppgifter som finns i min patientjournal. Detta får ske under förbehåll av att den information som därvid blir tillgänglig inte förs vidare.
____________________________ ______________________ Forskningspersonens underskrift Plats och datum
_____________________________ Namnförtydligande
Jag har förklarat studiens upplägg, syfte och för ovanstående patient.
_____________________________ ______________________
32
Bilaga 2 - Protokoll för datainsamling
Preoperativt
Studien och insamlandet av data påbörjas operationsdagen. Patienten tillfrågas angående riskfaktorer för PONV enligt:
I samband med tidigare operationer/narkoser – har du då mått illa eller kräkts? Ja / Nej
Brukar du besväras du av rörelsesjuka (åksjuka/sjösjuka) Ja / Nej
Röker du? Ja / Nej
Apfel-score ______
Modifierad Apfel-score ______
Postoperativt: PONV
Data som observeras hos patienten är:
PONV 2 timmar efter operation PONV 4 timmar efter operation
För varje observationstidpunkt gäller frågan hur det varit sedan föregående observationstidpunkt.
Frågor som ställs
Vid varje observationstidpunkt tillfrågas patienten om hur hon/han mått efter den föregående
registreringen. Vi använder oss i fråga 1 och 2 av en validerad modell för att kunna fånga upp varierande modaliteter i PONV.
(Tidpunkt= föregående registrering. Vid första registeringen: tidpunkt = efter operation)
33
Bilaga 2 - Protokoll för datainsamling
2 timmar efter operation
1 ”Har du sedan tidpunkt kräkts eller ulkat?” J/N Om Ja-> ”Hur många gånger?”
2 ”Har du sedan tidpunkt upplevt känsla av illamående? ” J/N
Om Ja-> ”Har ditt illamående påverkat vad du kan göra som att stiga upp ur sängen, röra på sig i sängen, gå normalt eller att äta och dricka?”
Om Ja-> ”Hur ofta har det varit så? Välj mellan ibland, ofta eller mesta delen av tiden eller hela tiden”
3 ”Har du sedan tidpunkt fått dig givet eller själv tagit läkemedel för behandling av illamående?” J/N Om Ja -> patienten får specificera
4 timmar efter operation
3 ”Har du sedan tidpunkt kräkts eller ulkat?” J/N Om Ja-> ”Hur många gånger?”
4 ”Har du sedan tidpunkt upplevt känsla av illamående? ” J/N
Om Ja-> ”Har ditt illamående påverkat vad du kan göra som att stiga upp ur sängen, röra på sig i sängen, gå normalt eller att äta och dricka?”
Om Ja-> ”Hur ofta har det varit så? Välj mellan ibland, ofta eller mesta delen av tiden eller hela tiden”
3 ”Har du sedan tidpunkt fått dig givet eller själv tagit läkemedel för behandling av illamående?” J/N Om Ja -> patienten får specificera
34
Bilaga 2 - Protokoll för datainsamling
Registrering av övriga studiedata
Premedicinering Data fr journal
Läkemedel Dos Tid
[ ] Paracetamol p.o. [ ] 1 g kl:________ [ ] 2 g [ ] __ __g [ ] Etorocoxib p.o. [ ] 90 mg kl:________ [ ] 120 mg [ ] __ mg [ ] Oxycodon p.o [ ] 10 mg kl:________ [ ] 20 mg [ ] __ mg Övrigt
Preparat: _____ Admsätt: ____ Dos: _________ kl:________ Preparat: _____ Admsätt: ____ Dos: _________ kl:________ Preparat: _____ Admsätt: ____ Dos: _________ kl:________
Preoperativt ordinerad Antiemetikaprofylax/TIVA Data ur Journal
[ ] Droperidol [ ] Betamethason [ ] Ondansetron [ ] TIVA
Under operation given antiemetikaprofylax Data ur Anestesijournal
Tid Dos
[ ] Droperidol iv ….:…. [ ] 0.5 mg [ ] 0.625mg [ ] 1 mg [ ] 1.25 mg [ ] ___ mg[ ] [ ] Betamethason iv ….:…. [ ] 4 mg [ ] ____mg
[ ] Ondansetron iv ….:…. [ ] 4 mg [ ] ____mg [ ] Annat: ____________ ….:…. ………
35
Anestesimetod Data ur Anestesijournal
[ ] Generell anestesi [ ] Huvudsakligt gas [ ] Intub [ ] Adjuvant spinal [ ] Huvudsakligt TIVA [ ] LMA [ ] Aktiverad EDA
[ ] Mask [ ] Plexus [ ] Regional bedövning [ ] Spinal [ ] Sederad m Propofol
[ ] Aktiverad EDA [ ] Sederad m Fentanyl [ ] Oaktiverad EDA [
[ ] Annan blockad:____________ (
Behandling av etablerat illmående Data ur journal
Läkemedel Tid Dos
……… ….:…. ……… ……… ….:…. ……… ……… ….:…. ……… ……… ….:…. ……… ……… ….:…. ……… ……… ….:…. ……… ……… ….:…. ……… Tider Anestesistart ……..:………. Anestesislut ……..:………. Opstart ……..:…….. Opslut ……..:……..
36